Clear Sky Science · tr
Granzyme B’yi taklit eden nanozim, nanovesikül hedefli antikanser uygulamalar için
Vücudun Kanser Katillerini Yeniden Tasarlamak
Bağışıklık sistemimiz kanseri avlayıp yok edebilen özelleşmiş hücrelere sahiptir, ancak birçok solid tümörde bu hücreler içeri girmekte zorlanır, çabuk yorulur veya yanlış hedeflere saldırır. Bu çalışma, bağışıklık sisteminin en güçlü silahlarından birini taklit eden ve onu doğrudan tümör hücrelerine taşıyan tamamen yapay, nanoskalalı bir sistemi tanımlıyor. Bu çalışma önemlidir çünkü yaşayan bağışıklık hücreleri gibi davranan, ancak narin insan hücreleri yerine kararlı ve kontrol edilebilir malzemelerden yapılmış kanser tedavilerine işaret ediyor.
Doğal Bir Katili Şablona Dönüştürmek
Sitotoksik T hücreleri, bir tür beyaz kan hücresi, granzyme B adlı bir enzim kullanarak tehlikeli hücreleri yok eder. Hedefi tanıdıklarında zarında küçük delikler açar ve granzyme B’yi enjekte ederler; bu da hücre içindeki intihar programlarını başlatır. Bu strateji, bazı kanserleri iyileştirebilen CAR-T hücreleri gibi modern terapilerin temelini oluşturur. Ancak solid tümörlerde CAR-T hücreleri genellikle tümörün tüm bölgelerine erişememek, tükenmek veya sağlıklı dokulara yanlışlıkla saldırmak gibi nedenlerle başarısız olur. Yazarlar, yaşayan T hücrelerine bağlı kalmadan granzyme B’nin temel işlevini—hücrenin kendini yok etme mekanizmasını çalıştırmayı—yeniden üretebilen cansız, nanoskalalı bir aygıt inşa edip edemeyeceklerini sordular.
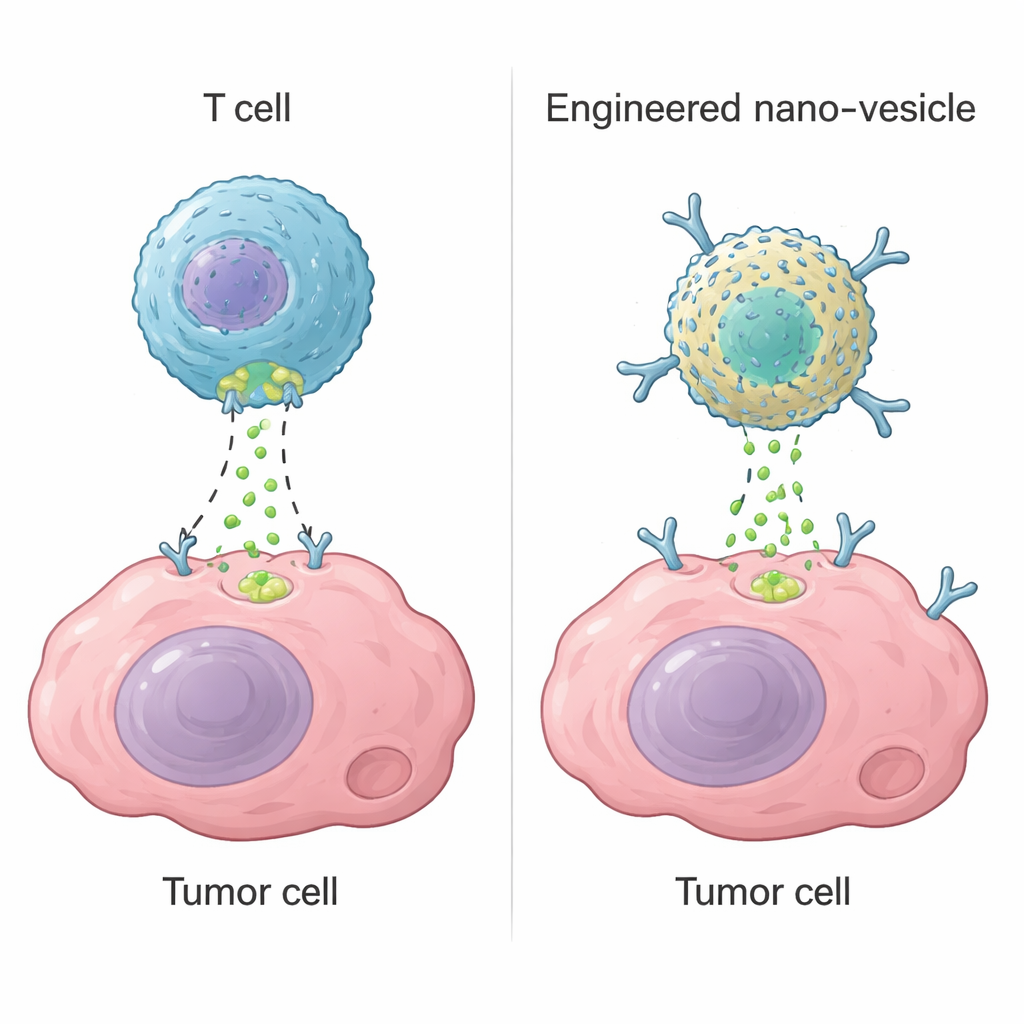
Minik Yapay Bir Enzim Tasarlamak
Ekip, boş nanokaflar oluşturan ve büyük miktarlarda üretmesi kolay doğal bir protein olan ferritin’den başladı. İnsan ferritinine palladyum iyonları bağlayarak enzim benzeri davranış gösteren bir “nanozim” yarattılar. Dikkatli yapısal çalışmalar, iki palladyum atomunun protein yüzeyindeki belirli bir ceplere yerleştiğini; bunların kükürt ve azot içeren aminoasitler ile su molekülleri tarafından yerinde tutulduğunu ortaya koydu. Bu çift çekirdekli metal merkezi, granzyme B tarafından hedef alınan kısa diziyi tanıyan yapay bir kesme bölgesi gibi davranıyor; hedef olarak kritik bir protein olan caspase-3 üzerindeki aynı kısa diziye odaklanıyor. Laboratuvar testlerinde nanozim, caspase-3’ü doğru konumdan etkili biçimde kesti ve onu aktive etti; yakın ilişkili proteinleri ise ihmal etti. Yapay enzim doğal granzyme B’den biraz daha az verimliydi, ancak sıcaklık ve asidite açısından çok daha geniş bir aralıkta belirgin şekilde daha kararlıydı.
Nanozimi Tümör Hücrelerine Kaçırmak
Granzyme B gibi enzimler yalnızca tümör hücrelerinin içine ulaştıklarında işe yarar. Bunu başarmak için araştırmacılar, palladyum–ferritin nanozimlerini lipid nanovesiküller—yağ benzeri moleküllerden yapılmış küçük, yumuşak kabarcıklar—içine paketlediler. Ardından bu vezikülleri, meme ve mesane kanseri hücrelerinde sıkça aşırı üretilen bir protein olan HER2’yi tanıyan antikor parçacıklarla kapladılar. Bu kamufle veziküller HER2 zengini hücrelerle karşılaştığında sıkı bağlanır ve hücre zarıyla kaynaşır; böylece nanozim yükü, hücresel geri dönüşüm bölgelerinde sıkışıp sindirilmek yerine doğrudan sitoplazmaya kayar. Mikroskop görüntüleri veziküllerin hücre yüzeyinde beklediğini, nanozimin ise içeri doğru yayıldığını gösterdi; bu da hücre içinden kontrollü bir intiharı başlatmak için uygun bir durum yarattı.
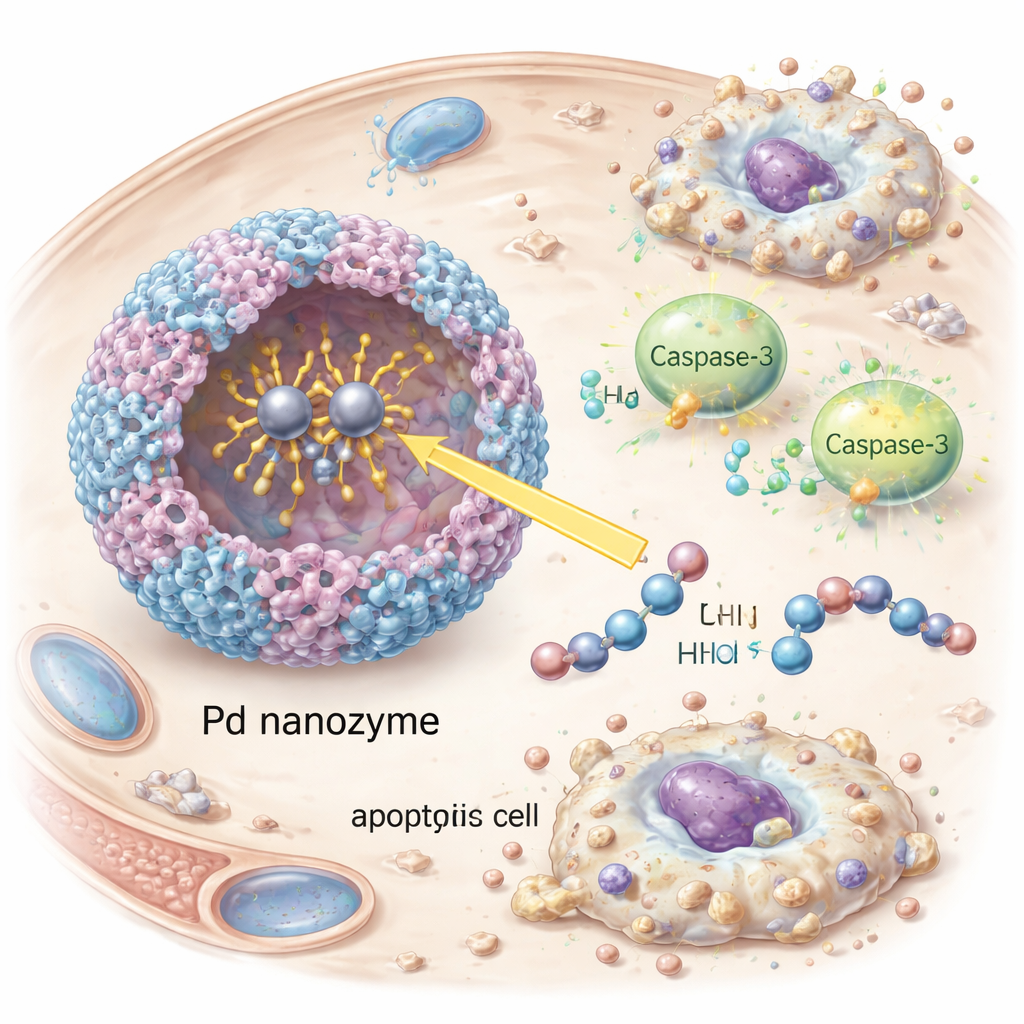
Kansere Karşı Hassas Hücre İntiharı Tetiklemek
Nanozim kanser hücrelerinin içine girdikten sonra programlı hücre ölümünün merkezi idamcısı olan caspase-3’ü aktifleştirdi. Araştırmacılar aktifleşmiş caspase-3’ün ve onun aşağı akış hedefi PARP’nin ortaya çıkışını, ayrıca kültürdeki HER2-pozitif tümör hücrelerinde hücrelerin küçülmesi ve parçalanması gibi belirgin apoptoz belirtilerini gözlemlediler. Caspase-3’ü RNA interferansı ile susturmak hücre ölümünü dramatik şekilde azalttı; bu da etkinin spesifik olmayan hasardan ziyade bu yolak üzerine bağlı olduğunu doğruladı. HER2-pozitif tümör taşıyan farelerde, antikorla süslenmiş veziküller kan dolaşımında daha uzun süre kaldı, tümörlerde daha güçlü birikim gösterdi ve hedefleyici antikorlar ya da nanozim yükünden yoksun veziküllere göre tümör büyümesini daha etkili biçimde yavaşlattı. Önemli olarak, tedavi edilen hayvanlarda belirgin bir kilo kaybı, kan anormallikleri veya başlıca organlarda doku hasarı gözlenmedi; bu da bu erken testlerde uygun bir güvenlik profiline işaret ediyor.
Geleceğin Kanser Bakımı İçin Anlamı
Uzman olmayanlar için temel mesaj şudur: Araştırmacılar, bağışıklık sistemimizin kanser öldürücü mekanizmasının önemli bir parçası gibi davranan, çok küçük, cansız bir aygıt inşa ettiler. Yaşayan T hücrelerini mühendisleştirmek yerine, tümör hücreleri içindeki aynı intihar anahtarını aktive eden kararlı bir nanoenzim tasarladılar ve bunu belirli kanserlere yönelen akıllı bir taşıma kabuğuna sardılar. İnsan kullanımına gelmeden önce hâlâ çok iş yapılması gerekse de, bu yaklaşım esnek bir platform sunuyor: prensipte antikor kaplaması farklı tümör belirteçlerine yöneltilecek şekilde değiştirilebilir ve yapay enzim daha da optimize edilebilir. Çalışma, dikkatle tasarlanmış nanomalzemelerin—yaşayan bağışıklık hücreleri yerine—solid tümörleri avlayıp yok etmek için kullanılabileceği hücresiz immünoterapiye yönelik ümit verici bir yol gösteriyor.
Atıf: Hu, X., Liu, Q., Kang, H. et al. Granzyme B-mimetic nanozyme for nanovesicle targeted anticancer applications. Nat Commun 17, 2031 (2026). https://doi.org/10.1038/s41467-026-68773-x
Anahtar kelimeler: kanser nanomedisini, immünoterapi, granzyme B, nanozim, HER2-pozitif tümörler