Clear Sky Science · tr
Boronato-kaplı dihidrotetrazinler ile mümkün kılınan, reaktif oksijen türleri tarafından aktive edilen bioortogonal kimya canlı sistemlerde
Hücre Stresini Kesin Bir Anahtara Çevirmek
Kanserden kalp rahatsızlıklarına kadar birçok hastalık, oksidatif stres altındaki hücrelerle ve hidrojen peroksit gibi yüksek düzeyde reaktif oksijen türleri üretimiyle karakterizedir. Bu çalışma, kimyacıların bu stresi yalnızca gerektiğinde güçlü tedavileri açan dahili bir anahtar olarak nasıl kullanabileceğini gösteriyor. Sadece bu stresli ortamlarda reaksiyona giren ilaç bileşenleri tasarlayarak, araştırmacılar sağlıklı dokuları korurken tümör hücrelerini öldürmeyi veya zararlı proteinleri yok etmeyi hedefliyor.
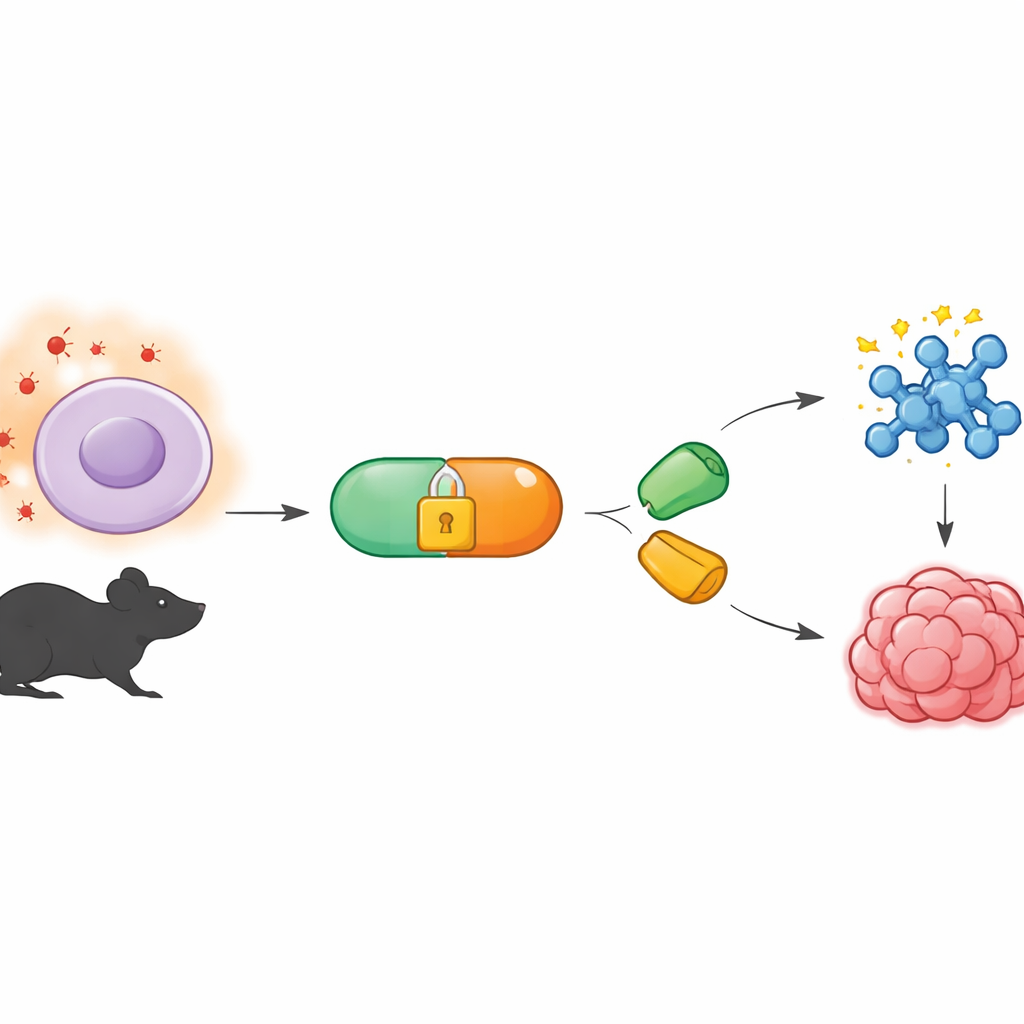
Arka Planda Sessiz Çalışan Bir Kimyasal Araç
Çalışma, normal biyolojiyi bozmadan canlı organizmalar içinde çalışabilen reaksiyonlar geliştiren bioortogonal kimya alanına dayanıyor. Popüler bir versiyon, hücrenin kalabalık iç ortamında bile bir araya gelen özel molekül çiftlerini kullanıyor; bir ortak, tetrazin olarak adlandırılan molekül, eşleşen “halkalı” partner yani dienofil ile çok hızlı reaksiyona giriyor. Şimdiye dek bu reaksiyonların çoğu ışıkla tetiklenerek veya enzim eklenerek kontrol ediliyordu. Yazarlar ise bunun yerine vücudun kendi kimyasal sinyallerini dinleyen —özellikle tümörlerde ve diğer hastalıklı dokularda bulunan olağandışı yüksek reaktif oksijen türü düzeylerini— kullanan bir sistem istediler.
ROS’a Duyarlı Bir Kimyasal Tetik İnşa Etmek
Bunu yapmak için ekip, BTz adını verdikleri tetrazin öncüleri yarattı; bunlar kimyasal olarak “kafeslenmiş” halde kalarak normal dokularda sessiz duruyor. Kafes, boronato grubundan ve indirilmiş tetrazin formuna bağlı bir yapıdan oluşuyor. Hidrojen peroksit az olduğunda BTz sulu çözeltilerde ve hücre kültüründe saatlerce kararlı kalıyor. Ancak hidrojen peroksit bol olduğunda—tümörlerde ölçülen düzeylere benzer seviyelerde—boronato grubu okside oluyor ve kendi kendini yok etme dizisiyle parçalanarak aktif tetrazini ortaya çıkarıyor. Deney tüpü deneylerinde hidrojen peroksit konsantrasyonunun adım adım artırılması, açığa çıkan aktif tetrazin miktarında matching bir artışa yol açtı; bu da reaksiyonun seçici ve güçlü bir doz bağımlılığı gösterdiğini doğruluyor.
Hücre Stresini Kanser Sürücü Bir Proteini Yok Etmek İçin Kullanmak
Araştırmacılar önce bu anahtarı hedefe yönelik protein yıkımı olarak bilinen modern ilaç stratejisini kontrol etmek için kullandı. BTz’yi, proteinleri imha için etiketleyen enzim kompleksini cezbedebilen küçük bir molekül olan talidomide bağladılar. Kanser hücrelerinde bu BTz–talidomid, hidrojen peroksit düzeyleri yükseltilene kadar pasif kaldı; o anda kafes açılarak aktif tetrazin oluştu. Bu tetrazin daha sonra BRD4 bağlayan bir ilaca bağlı eşleşen partnerle hızla birleşerek, kanserle ilişkili protein BRD4’ü hücrenin atık mekanizmasına çeken daha büyük bir “şimeera” oluşturdu. Akciğer ve serviks kanser hücre hatlarında, BRD4 seviyeleri yalnızca tüm parçalar mevcut ve hidrojen peroksit sağlandığında keskin şekilde düştü; reaktif oksijen türlerini engellemek bozunmayı önledi ve sürecin gerçekten stresle aktive olduğunu vurguladı.
Zehirli Bir İlacı Sadece Gerektiği Yere Teslim Etmek
Sonra ekip aynı kimyayı, güçlü ama kalp için zararlı olan doksorubisin için hassas bir teslimat sistemine dönüştürdü. Doksorubisini, inaktif bir proilaç formunda kilitli kalması için gergin bir halka partnerine bağladılar. Bu proilaç, BTz ile hidrojen peroksit açısından zengin bir ortamda karşılaştığında, yeni oluşan tetrazin halkayla “tıkla‑ve‑serbest bırak” sürecinde reaksiyona girerek parçaları birleştirdi ve serbest doksorubisini fırlattı. Laboratuvarda yetiştirilen kolon kanseri hücrelerinde, bu iki adımlı sistem serbest ilaç kadar hücreleri neredeyse aynı etkinlikle öldürdü, ancak yalnızca hidrojen peroksit varlığında; yokluğunda hücreler büyük ölçüde zarar görmedi. Daha basit bir hidrojen peroksit‑duyarlı doksorubisin proilaçı bu testlerde daha az etkili ve daha az seçiciydi; bu da algılama ile salımı iki koordine adıma ayırmanın avantajını ortaya koyuyor.
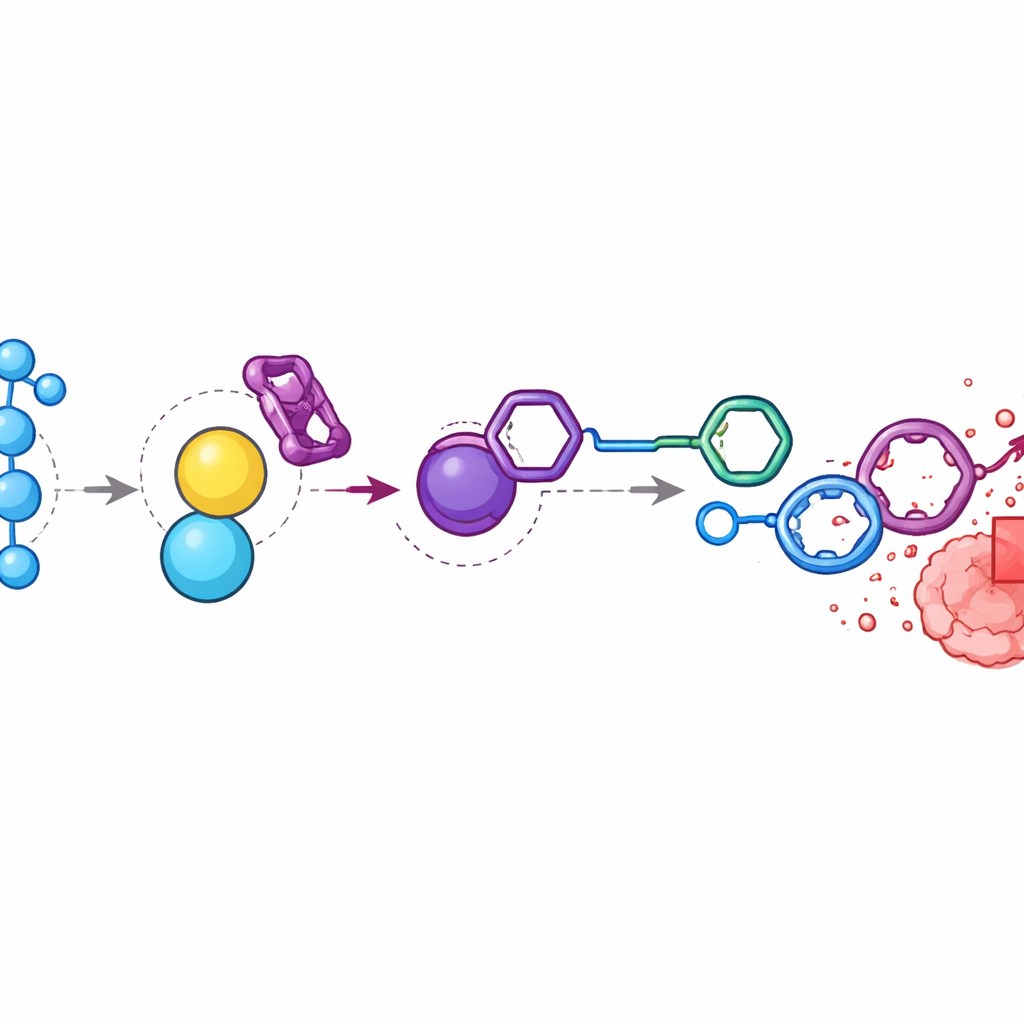
Kemoterapiyi Tümör İçine Odaklamak
Kolon tümörü taşıyan farelerde araştırmacılar tümörlerdeki hidrojen peroksit düzeylerinin çevredeki kas dokusuna göre neredeyse dokuz kat daha yüksek olduğunu buldu. Doksorubisin proilaç ve BTz’yi zamanlanmış bir sırayla enjekte ettiler, böylece her ikisi de tümör yakınında birikti. Kimyasal analiz, bileşenlerin büyük ölçüde kan dolaşımından ve organlardan kaybolduğunu ancak tümör içinde yüksek düzeyde serbest doksorubisin üretildiğini gösterdi. Standart doksorubisin verilen hayvanlarla karşılaştırıldığında, aktive edilmiş sistemle tedavi edilenlerde benzer veya daha iyi tümör küçülmesi görüldü; buna karşın vücut ağırlıkları stabil kaldı ve yüksek ilaç dozlarında görülen şiddetli toksisite önlendi. Ekip hidrojen peroksit sinyalini kaldırmak için katalaz enzimini enjekte ettiğinde, ilaç salımı ve tümör‑seçici birikim büyük ölçüde azaldı; bu da tümör bölgesindeki oksidatif stresin kilit sürücü olduğunu doğruladı.
Stres Sinyalinden Kesinliğe Dayalı Terapilere
Toparlanmış halde, bu çalışma hastalığın bir belirteci olan aşırı reaktif oksijeni, canlı sistemler içinde güçlü reaksiyonları kontrol eden hassas bir ayar düğmesine çeviren çok yönlü bir kimyasal platformu gösteriyor. Reaktif tetrazin kolunu hidrojen peroksite kadar kilitli tutarak, yaklaşım araştırmacıların vücut içinde yalnızca ihtiyaç duyulan yerde karmaşık tedaviler inşa etmelerine olanak tanıyor; ister kanseri teşvik eden bir proteini sökmek, ister bir tümör içinde zehirli bir ilacı serbest bırakmak olsun. Oksidatif stres aynı zamanda yaşlanma, iltihap, diyabet ve nörodejeneratif bozukluklarda da rol oynadığından, benzer stres‑duyarlı reaksiyonlar kesinlik ve güvenliğin ön planda olduğu birçok durumda nihayetinde uyarlanabilir.
Atıf: Ming, D., Zhang, J., Mu, B. et al. Reactive oxygen species-activated bioorthogonal chemistry in living systems enabled by boronate-caged dihydrotetrazines. Nat Commun 17, 2568 (2026). https://doi.org/10.1038/s41467-026-68771-z
Anahtar kelimeler: bioortogonal kimya, reaktif oksijen türleri, tetrazin ligasyonu, hedefe yönelik ilaç teslimatı, PROTAC