Clear Sky Science · tr
Homo-tipik membran kaynaklı elektrokimyasal mikroakışkan analizi ile ekztraselüler veziküllerin hassas kanser tanısı
Kanserin Kendi Zırhını Tanı Aracına Dönüştürmek
Kanser hücrelerini çevreleyen membranlar ayırt edici moleküler “işaretlerle” doludur. Bu çalışma, bilim insanlarının bu zırhı soyup küçük altın yüzeylere yayabildiğini ve ardından kan içinden belirleyici partikülleri yakalamak için kullanabildiğini gösteriyor. Sonuç, yalnızca meme kanserinin varlığını değil, aynı zamanda hangi alt tür olduğunu da ortaya koyabilen son derece duyarlı bir kan testi — bu bilgi doğru tedaviyi seçmek için kritik önemde.
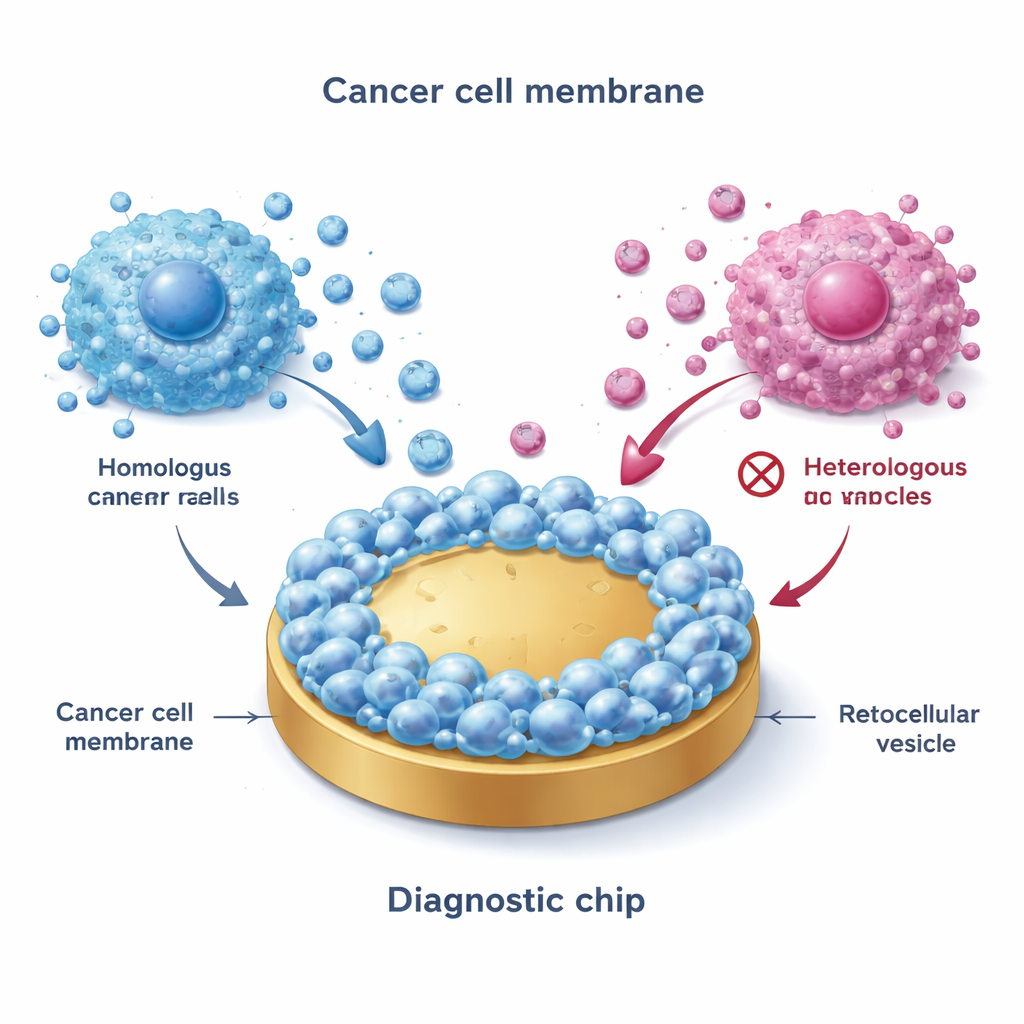
Meme Kanseri Alt Türünün Neden Önemi Var
Meme kanseri tek bir hastalık değildir. Tümörler östrojen reseptörü pozitif (ER+), HER2-pozitif ve üçlü negatif gibi alt türlere ayrılır ve her biri hormon tedavisine, hedefe yönelik ilaçlara veya kemoterapiye farklı yanıt verir. Günümüzde doktorlar genellikle alt türü tümör dokusundan alınan biyopsiyle belirler. Bu işlem invazivdir, sık yapılamaz ve hastalık ilerledikçe ortaya çıkan değişiklikleri gözden kaçırabilir. Zaman içinde bu alt tür imzalarını izleyebilen kan temelli bir test, hekimlerin tedaviyi daha erken ve daha isabetli şekilde ayarlamasına olanak tanır.
Kanda Yüzen Küçük Haberciler
Kanser hücreleri sürekli olarak ekztraselüler vezikül (EV) adı verilen nanoskaladaki kabarcıkları kana salar. EV’ler ana hücrelerinin proteinlerini, yağlarını ve genetik materyalini taşır; bu nedenle “sıvı biyopsi” için çekici adaylardır. Ancak bir zorluk vardır: farklı meme kanseri alt türlerinden gelen EV’ler, sadece bir veya iki proteine odaklanılırsa birbirine çok benzer görünebilir. Mevcut testler ya alt türleri ayırt etmeyi zorlaştıran ortak belirteçleri hedefler ya da yavaş ve yanıltıcı olabilen karmaşık genetik analizlere dayanır. Yazarlar, EV yüzeylerindeki daha eksiksiz moleküler parmak izini basit ve sağlam bir şekilde okumayı amaçladılar.
Biyomimetik Bir Ağ İnşa Etmek
Ekip, başlıca alt tipleri temsil eden kültürlenmiş meme kanseri hücrelerinden membranlar toplayarak işe başladı: ER+ (örneğin MCF-7), HER2-pozitif ve üçlü negatif. Bir dondurma–çözme süreci kullanarak hücreleri parçaladılar, dış membranları izole ettiler ve ardından bu membranları düz altın yüzeylere füze ettiler. Bu, orijinal kanser hücrelerinin dış yüzeyini yakından taklit eden bir “biyomimetik arayüz” yarattı. Dikkat çekici biçimde, EV’ler bu kaplı yüzeylerin üzerinden akıtıldığında, yalnızca eşleşen veya yakından ilişkili kanser alt tiplerinden gelen veziküller güçlü şekilde yapıştı — buna homotipik bağlanma deniyor. Gelişmiş görüntüleme ve elektriksel ölçümler, membran kaplı yüzeylerin daha pürüzlü, daha hidrofilik ve çıplak altına göre özgül olmayan yapışmaya çok daha az yatkın olduğunu doğruladı; bu da kan gibi karmaşık sıvılarda temiz ölçümler için uygun olduklarını gösteriyor.
Vezikül Yakalamayı Elektriksel Bir Sinyale Dönüştürmek
Bağlanmayı okunabilir bir sinyale çevirmek için araştırmacılar EV yüzeyindeki bol bulunan bir protein olan CD47’yi hedef aldı. CD47 antikorlarını kısa bir DNA köprüsü kullanarak gümüş nanoparçacıklara bağladılar ve küçük elektroaktif etiketler oluşturdular. Membran kaplı yüzey tercih ettiği EV’leri yakaladıktan sonra bu etiketler, bağlı veziküller üzerindeki CD47’ye tutundu. Asitli bir solüsyona maruz bırakıldığında ve ardından elektrokimyasal olarak ölçüldüğünde, gümüş keskin ve kolayca nicelendirilebilir bir akım üretti. Bu sinyalin gücü, yüzlerce vezikül/mL düzeyine kadar çok geniş bir EV konsantrasyonu aralığında doğru bir doğrusal artış gösterdi — ELISA kitleri veya nanoparçacık izleme gibi yaygın yöntemlerden çok daha duyarlı. Her kanser membran türü, diğer alt tiplerden gelen veziküllerin, trombositlerin veya ilgisiz hücrelerin varlığında bile yalnızca kendi eşleşen EV’leriyle güçlü bir sinyal üretti.
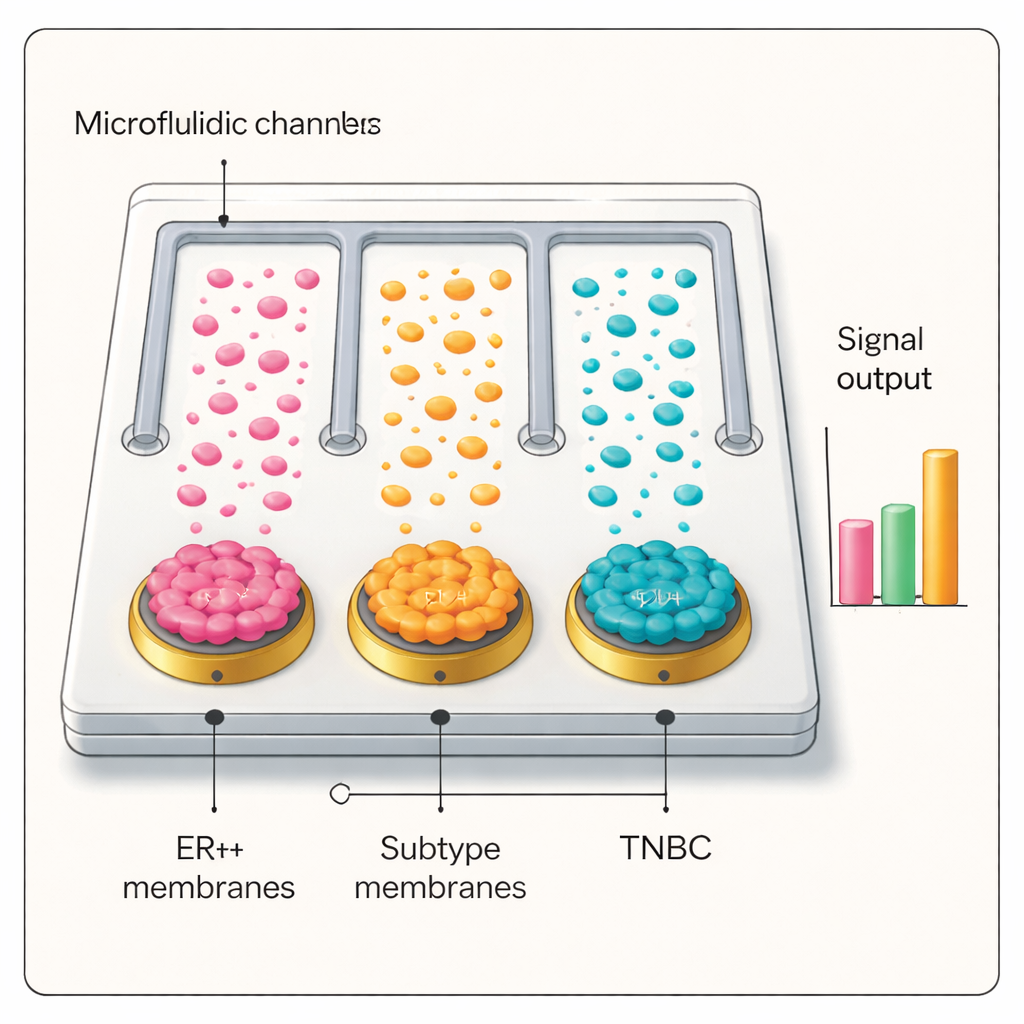
Laboratuvar Tezgâhından Hasta Kan Örneklerine
Bu seçici ve hassas arayüzle, ekip her biri farklı bir meme kanseri hücre membranıyla kaplı paralel kanallar ve bir kaplanmamış kontrol içeren bir mikroakışkan çip geliştirdi. Hastalardan alınan plazma çipten geçirildiğinde ve gümüş–antikor etiketlerle probalandığında, yalnızca membranı hastanın tümör alt türüyle eşleşen kanal yüksek elektriksel sinyal verdi. ER+ ve üçlü negatif meme kanseri hastaları, iyi huylu meme hastalığı olan bireyler, akciğer kanseri hastaları ve sağlıklı gönüllüler dahil onlarca kişinin yer aldığı kör testlerde, platform kanseri kanser olmayan durumdan doğru şekilde ayırdı ve meme kanseri alt tiplerini doğru olarak tanımladı. Tanısal performans birçok durumda standart patolojiyle eşdeğer veya daha iyiydi ve hastalığın evrelemesi ile ilerlemenin izlenmesi için umut vaat etti.
Geleceğin Kanser Bakımı İçin Anlamı
Basitçe söylemek gerekirse, araştırmacılar kanserin kendi dış kabuğunu tümörün kana saldığı küçük partiküller için son derece seçici bir yem haline getirdiler. Hangi kanalın “ışık verdiğinin” elektriksel imzasını okuyarak, doktorlar bir gün yalnızca bir kan örneğiyle hem kanserin varlığını hem de türünü belirleyebilir. Sistem hâlâ daha fazla belirteç ve daha fazla membran türü eklenmesi, akıllı veri analizinin entegre edilmesi gibi iyileştirmelere ihtiyaç duysa da, rutin, minimal invaziv kan testlerinin kişiselleştirilmiş kanser tedavisini yönlendirdiği ve tümörlerin zaman içindeki değişimini izlediği bir geleceğe işaret ediyor.
Atıf: Zou, Z., Jin, X., Yu, X. et al. Homotypic membrane-powered electrochemical microfluidic analysis of extracellular vesicles for precise cancer diagnosis. Nat Commun 17, 1953 (2026). https://doi.org/10.1038/s41467-026-68770-0
Anahtar kelimeler: meme kanseri alt tipleri, sıvı biyopsi, ekztraselüler veziküller, mikroakışkan tanı, hücre membranı sensörleri