Clear Sky Science · tr
Golgi görüntüleme ve bozulması için döngüsel moleküler düzenekler
Hücrenin gönderi merkezini stratejik bir hedefe dönüştürmek
Her hayvan hücresinin içinde, binlerce proteini ve yağı tamamlayan, paketleyen ve sevk eden yoğun bir ayırma istasyonu olan Golgi aygıtı bulunur. Birçok kanser hücresi, büyüme sinyallerini değiştirip çevrelerini şekillendiren faktörleri salgılamak için bu merkeze büyük ölçüde bağımlıdır. Bu makale, Golgi’ye yönelen, hızlı görüntüleme için onu aydınlatan ve yeniden tasarlandıklarında belirli sağlıklı hücreleri göreli olarak korurken kanser hücrelerinin işlevini seçici olarak tıkayabilen küçük tasarım moleküllerini tanıtıyor.
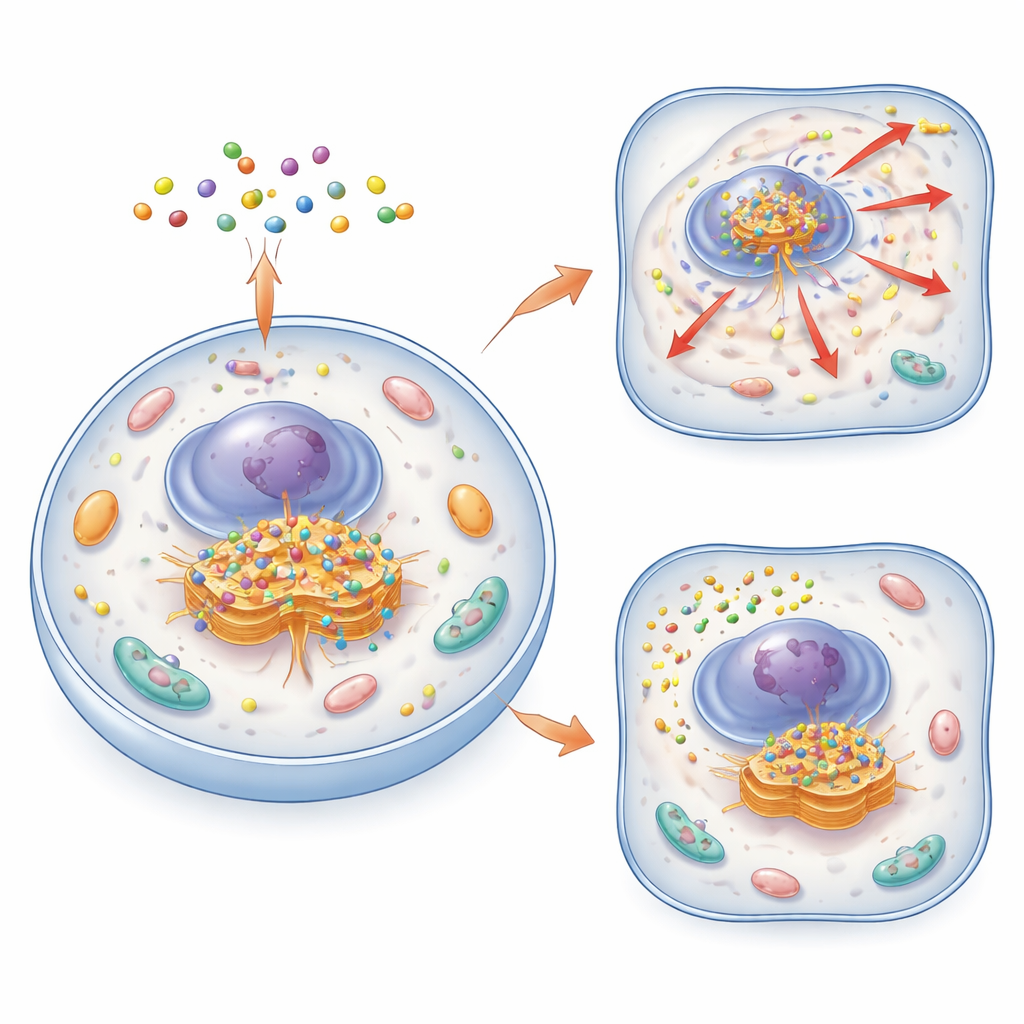
Golgi’yi bulmak ve izlemek için yeni bir yol
Yazarlar, döngüsel moleküler düzenekler (CyMA) adı verilen küçük, akıllı bir molekül ailesi geliştirdiler. Bu moleküller, hem hücre zarlarından geçebilen hem de küçük kümeler halinde birbirine yapışabilen kısa peptidlerden inşa edilmiştir. "Görüntüleme" versiyonunda (CyMA‑i), peptidler bir araya geldiklerinde parlak şekilde ışıldayan bir floresan boya taşır. Hücre içine girdikten sonra, enzimler CyMA öncüsünün koruyucu kapağını keser ve reaktif bir tutamaç açığa çıkarır. Golgi'ye yerleşik enzimler daha sonra bu tutamaça bir yağ zinciri ekleyerek molekülleri çok daha yapışkan hale getirir ve tam olarak Golgi’de kendiliğinden bir araya gelmeye eğilimli kılar. Bu süreç hızlıdır ve doğal hücresel makineleri kullandığı için araştırmacılar, canlı hücrelerde çok düşük problar konsantrasyonlarında bile birkaç dakika içinde Golgi’nin şeklini çizebilirler.
Molekülleri Golgi’ye sabitleyen nafile döngü
CyMA'lar sadece etiket değildir; Golgi’de bir "nafile döngü"ye katılacak şekilde tasarlanmışlardır. Bir enzim grubu peptide yağ zincirleri eklerken, başka bir grup bunları söker. Hücre bu zincirleri sürekli ekleyip çıkardıkça, modifiye peptidler oldukları yerde bir araya gelip ayrışmaya devam eder. Bu sürekli gidip gelme, Golgi zarlarında katıya benzer bir çekirdek kümelenmeyi tuzağa düşürür, ancak bireysel moleküller döngüye devam eder. Hücre, bu döngüyü sürdürmek için kendi yağ-asidi yapı taşlarını sürekli harcamak zorunda kalır; bu da düzenekleri besler ve onların kalıcılığına katkıda bulunur. Aynı zamanda, ek enzimler CyMA içindeki belirli bir ester bağını yavaşça kesebilir ve onları daha suda çözünen parçacıklara dönüştürerek uzaklaşmalarını sağlar. Bazı sağlıklı hücreler—örneğin karaciğer hücreleri ve belirli bağışıklık hücreleri—bu tür esterleri kesen enzimler bakımından zengin olduğundan, CyMA’yı doğal olarak daha iyi sökebilirler ve bu nedenle daha az etkilenirler.
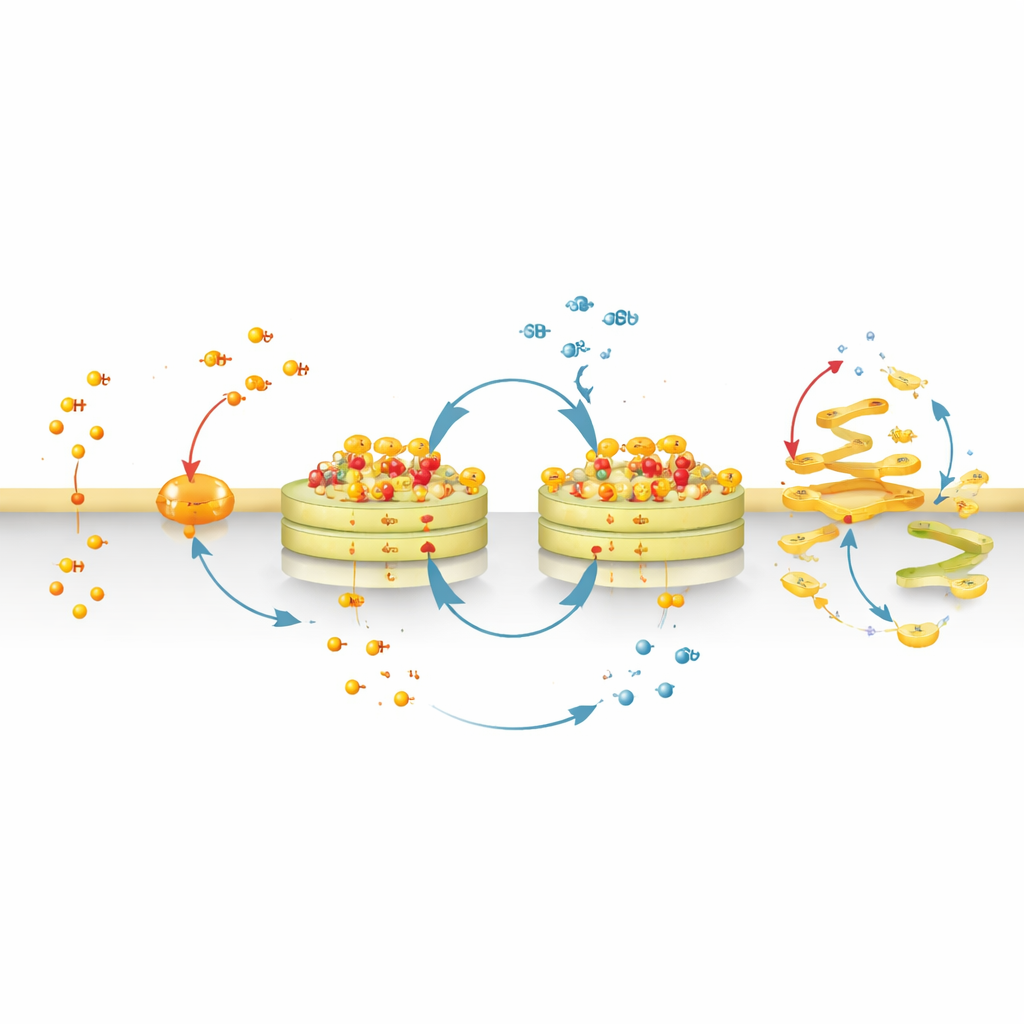
Hafif bir görüntüleme aracından Golgi bozucuya
Floresan boyayı daha güçlü zar‑çekici bir kimyasal grupla değiştirerek ekip, CyMA‑i’yi artık ışıldamayan ama hâlâ Golgi’de dönen ve kümelenen bozar sürüm CyMA‑d’ye dönüştürdü. Bu düzenekler Golgi yapısını ve ona giden ve ondan gelen vezikül akışını fiziksel olarak bozar. Normalde endoplazmik retikulumdan Golgi’ye ve oradan hücre yüzeyine giden proteinler sıkışır veya yanlış yönlendirilir. Hücre yüzeyinden Golgi’ye veya Golgi’den diğer organellere gelen yollar da bloke edilir. Sonuç olarak, önemli yüzey reseptörleri ve sinyal molekülleri ya varış noktalarına ulaşamaz ya da hücre içinde yanlış yerlerde birikir.
Hücre sinyallerini ve salgı mesajlarını karıştırmak
Birçok proteinin şeker zincirleri ve yağ kuyrukları gibi hayati son dokunuşları Golgi’de yapılır. CyMA‑d düzenekleri, Ras ve büyük reseptör tirozin kinazları gibi tanınmış kanser sürücülerini de içeren çok sayıda proteinin uygun lipidasyonunu ve glikozilasyonunu azaltır. Bu değişiklikler AKT ve mTOR gibi büyümeyi teşvik eden yolakları sekteye uğratır. Aynı zamanda hücrenin salgı çıktısı azalır: tümörlerin bağışıklığı bastırmak ve kan damarı büyümesini uyarmak için kullandığı TGF‑β1 ve VEGF gibi önemli faktörler artık verimli şekilde salınamaz. Bu bozulmanın yol açtığı stres, karışık endoplazmik retikulum ağları, değişmiş mitokondriler, durma noktasına gelen otofaji (hücrenin geri dönüşüm sistemi) ve artan hasarlı, ubiquitin ile etiketlenmiş proteinler gibi etkiler yaratır; bunlar birlikte kanser hücrelerini ölüme doğru iter.
Tümörler üzerinde seçici baskı ve tedavi vaadi
CyMA‑d, birçok kanser hücresinin aşırı kullandığı ortak bir enzim ve metabolit setine bağlı olduğundan, çok düşük dozlarda ilaç‑dirençli over kanseri modelleri de dahil geniş bir tümör tipini öldürebilir. Bununla birlikte belirli esterase düzeyleri yüksek olan hücreler CyMA‑d’yi daha kolay parçalayarak daha az zarar görür; bu durum doğal bir seçicilik yolu sunar. Üç boyutlu tümör sferoidlerinde, hastadan türetilmiş kültürlerde ve fare modellerinde CyMA‑d tümörleri küçültür, metastazları azaltır ve karın içi sıvı birikimini keser. Bağışıklık kontrol noktası terapileriyle birleştiğinde tümör kontrolünü ve hayatta kalımı daha da artırırlar. Özetle, bu çalışma Golgi içinde dinamik malzemeler inşa etmenin—tek bir proteini hedeflemek yerine—aynı anda birden fazla kanser‑kritik süreci kapatabileceğini gösteriyor.
Gelecekteki tedaviler için anlamı
Uzman olmayan biri için kilit fikir, yazarların Golgi’yi pasif bir seyirci olmaktan çıkartıp aktif bir terapötik hedef haline getirdikleridir. Hücrenin kendi enzimlerini bu merkezi merkezde küçük molekülleri bir araya getirmek ve geri dönüştürmek için kullandırarak, ya onu zararsız biçimde vurgulayabilir ya da kademeli olarak işlevini aşırı yükleyip bozulmasını sağlayabilirler. Bu çift kullanımlı platform, tek bir proteine yönelik tek bir ilaç tasarlamak yerine, hücrelerin kendi içsel dönüşümüyle kendiliğinden örgütlenen malzemelere dönüşen küçük öncüler mühendislik ederek kanserlerin büyüme ve yayılma için kullandığı iletişim ve taşıma ağlarını bütünüyle bozabilecek yeni bir tedavi türünü işaret ediyor.
Atıf: Tan, W., Zhang, Q., Liu, Z. et al. Cycling molecular assemblies for Golgi imaging and disruption. Nat Commun 17, 2102 (2026). https://doi.org/10.1038/s41467-026-68768-8
Anahtar kelimeler: Golgi aygıtı, moleküler düzenekler, protein taşınımı, kanser tedavisi, organel hedefleme