Clear Sky Science · tr
1032 beyin metastazının proteogenomik atlası, moleküler alt tipleri, immün manzaraları ve terapötik açıklıkları tanımlıyor
Neden kanserler beyne yayılır
Kanser bakımı ilerledikçe, daha fazla insan tümörlerinin akciğer, meme, deri, kolon gibi başlangıç yerlerinden yeni bölgelere, aralarında beyin de olmak üzere, yayılması için yeterince uzun süre yaşamaya başladı. Bu beyin metastazları artık yaygın ve sıklıkla yıkıcı bir komplikasyon; yine de doktorlar bunları çoğunlukla kanserin nereden başladığına göre tedavi ediyor—beyazı yerine kanserin beyinde nasıl uyum sağladığına göre değil. Bu çalışma, binin üzerindeki beyin metastazının gizli biyolojisini, beyin hücreleri ve bağışıklık sistemiyle nasıl etkileştiğini ve yeni tedavi fırsatlarının nerede olabileceğini anlamak için ayrıntılı bir “atlas” oluşturdu.
Beyin tümörlerinin devasa bir haritasını oluşturmak
Araştırmacılar, farklı primer kanserlerden kaynaklanmış 1.032 beyin metastazı ile eşleşen onlarca primer tümör ve karşılaştırma için bazı agresif primer beyin tümörlerinden veri topladı. DNA ve RNA dizilemesi, geniş ölçekli protein ve metabolit ölçümleri, tek hücre ve mekansal haritalama, ve laboratuvarda yetiştirilen hasta kaynaklı mini organoidler gibi birkaç ileri teknoloji yaklaşımı birleştirdiler. Bu katmanların tümünü bütünleştirerek amaçları yalnızca genleri listelemek değil, beyin metastazları içinde bütün biyolojik sistemlerin nasıl davrandığını görmektir.
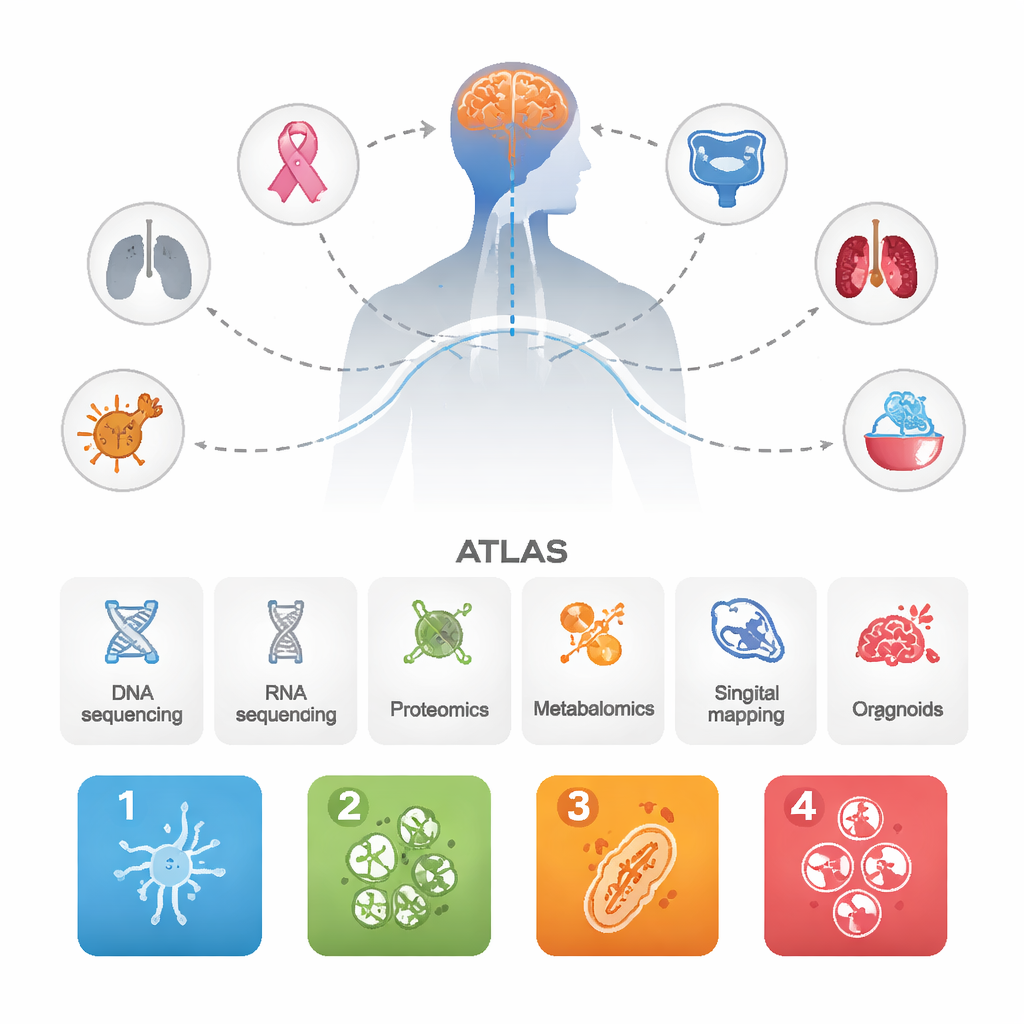
Beyin metastazlarının dört tekrarlayan “kişiliği”
Kaynaklandıkları organlar farklı olsa da beyin metastazları tekrar tekrar dört ana moleküler alt tipe ayrıldı. BrMS1 olarak adlandırılan birinci grup “nöral-benzeri” görünüyor: tümör hücreleri ve çevre doku birçok beyin ve sinir hücresi programı ifade ediyor ve nispeten aktif immün gözetim gösteriyor. BrMS2 “immün-infiltre”; özellikle T hücreleriyle dolu ve hücre bağlarını gevşeten ve yerel çevreyi yeniden şekillendiren epitel–mezenkimal geçiş programını gösteriyor. BrMS3 “metabolik”; yağ asidi metabolizması ve oksidatif fosforilasyon gibi yolları etkinleştirerek enerji kullanımını yeniden düzenleyen yüksek aktiviteli kanser hücreleri tarafından domine ediliyor. BrMS4 “proliferatif”; hızlı hücre bölünmesi, kök hücre benzeri özellikler ve yüksek genomik instabilite ile karakterize ama dikkat çekici biçimde az immün hücre içeriyor.
Tümörün çevresinin ortaya koydukları
Tek hücre ve mekansal çözünürlükte yakınlaştırma yaparak ekip, her alt tipin beyinde farklı bir mahallede yaşadığını gösterdi. BrMS1 lezyonları astroglia ve nöronlar gibi beyin destek hücreleri açısından zengin olup tümörün normal beyin dokusunu taklit edip ona ortak hale geldiğini düşündürüyor. BrMS2 tümörleri ise yoğun T hücresi kümeleriyle dolu; bunların arasında PD-1 gibi kontrol noktası moleküllerini ifade eden birçok “tükenmiş” T hücresi ve aktive olmuş kan damarları ile inflamatuvar sinyaller bulunuyor. BrMS3 lezyonları metabolik olarak yoğun bölgelerde yer alırken, BrMS4 lezyonları nispeten immün fakir bölgeyle çevrili hızlı bölünen hücre adacıkları oluşturuyor. Genel olarak çalışma, beyin metastazlarında—primer tümörlerde değil—epitel–mezenkimal geçişin güçlü aktivasyonunun genellikle daha yüksek T hücresi infiltrasyonu ile el ele gittiğini buldu; bu da bu programın immün hücrelerin giriş yolunu açmaya yardımcı olabileceğine işaret ediyor.
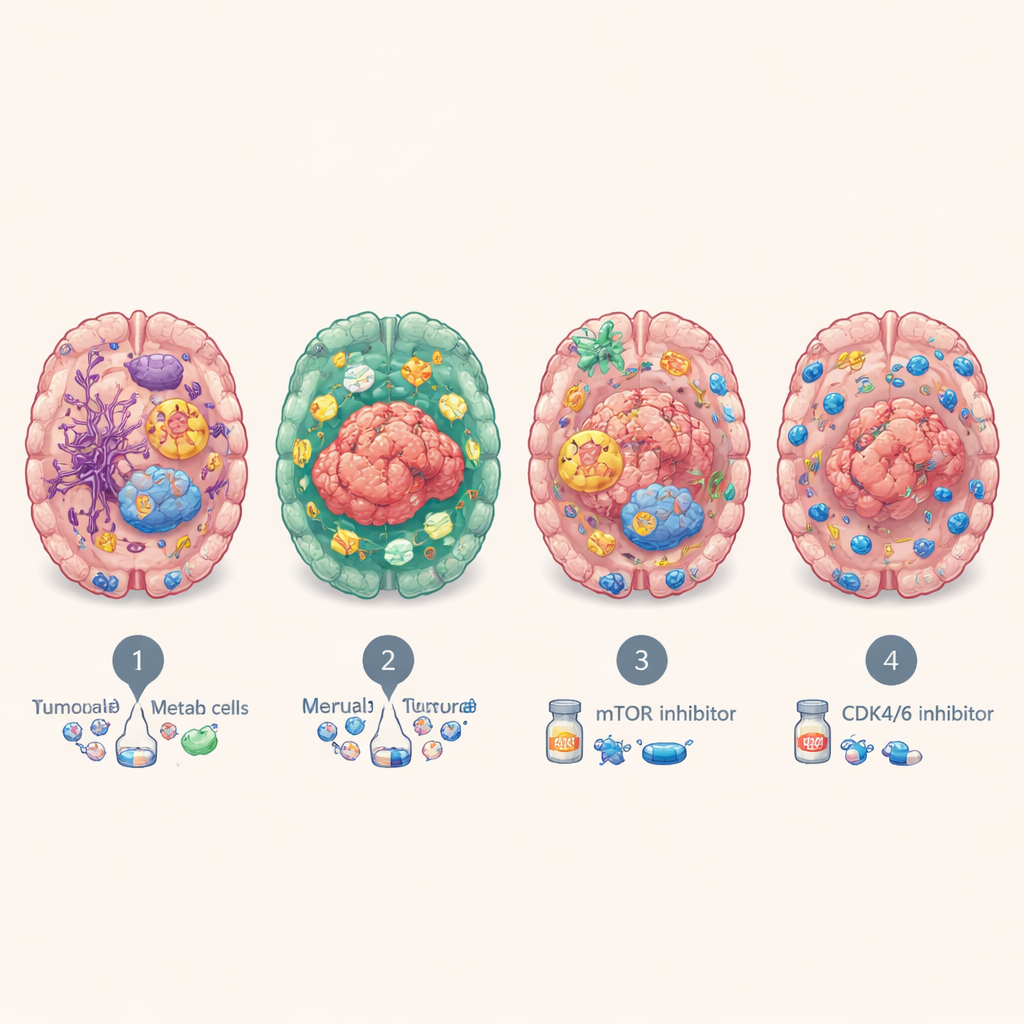
Tedavi ve hasta sonuçlarına dair ipuçları
Bu moleküler kişilikler yalnızca akademik değildi. Immün-infiltre BrMS2 alt tipine sahip hastalar, proliferatif BrMS4 alt tipine sahip olanlara göre genellikle daha uzun yaşadı; BrMS4 ise tutarlı şekilde en kötü sonuçlara sahipti. Hasta kaynaklı organoidlerde ilaç testleri yaparak ekip, metabolik BrMS3 tümörlerinin hücre büyümesi ve metabolizmayı kontrol eden mTOR sinyal yolunun engellenmesine özellikle duyarlı olduğunu, hızlı bölünen BrMS4 tümörlerinin ise hücre döngüsünü yavaşlatan CDK4/6 inhibitörlerine karşı daha savunmasız olduğunu buldu. Ayrı analizler BrMS1 tümörlerinin radyoterapiye daha iyi yanıt verebileceğini, BrMS2’nin ise inflamatuvar, kontrol noktası zengin ortamı sayesinde tükenmiş T hücreleri canlandıran immünoterapilerden fayda görme olasılığının daha yüksek olabileceğini öne sürdü—ancak bunun beyin metastazı olan hastalarda doğrudan doğrulanması gerekiyor.
Beyin metastazı olan kişiler için bunun anlamı
Bu atlas, kanser hücreleri beyine ulaştığında, geldikleri yere bakılmaksızın birkaç ortak biyolojik duruma doğru eğilim gösterdiklerini ortaya koyuyor. Bir kişinin beyin metastazının nöral-benzeri, immün-zengin, metabolik veya yüksek proliferatif olup olmadığını anlamak, nihayetinde radyoterapi, immünoterapi veya metabolizma ve hücre bölünmesini hedef alan ilaçlar arasında daha kişiselleştirilmiş tedaviler seçilmesine yol gösterebilir. Bu çalışma henüz standart bakımı değiştirmiyor olsa da, bu moleküler açıklıkları daha iyi, daha kesin tedavilere dönüştürmeyi amaçlayan gelecekteki araştırmalar ve klinik denemeler için ayrıntılı bir yol haritası sunuyor.
Atıf: Yang, Z., Wei, S., Duan, H. et al. A proteogenomic atlas of 1032 brain metastases identifies molecular subtypes, immune landscapes, and therapeutic vulnerabilities. Nat Commun 17, 2038 (2026). https://doi.org/10.1038/s41467-026-68748-y
Anahtar kelimeler: beyin metastazı, tümör alt tipleri, tümör mikroçevresi, kanser immünoterapisi, kanser metabolizması