Clear Sky Science · tr
Tek diziden işlev modellemesi kullanarak tek hücreli ATAC-seq atlaslama teknolojilerini değerlendirme
Hücrenin kullanım kılavuzunu okumak
Vücudunuzdaki her hücre aynı DNA’yı okur, ancak beyin hücreleri, kas hücreleri ve bağışıklık hücreleri çok farklı davranır. Bu makale, bu çeşitliliğin ardındaki temel bilmecelerden birine odaklanıyor: enhancer adı verilen kısa DNA dizilerinin belirli hücre tiplerinde genleri açıp kapatmak için nasıl anahtar gibi davrandığı. Yazarlar, daha yeni ve ucuz laboratuvar teknolojilerinin, DNA dizilerini okuyup hangi enhancer’ların hangi hücrelerde etkin olduğunu tahmin eden modern derin öğrenme modellerini eğitmek için gereken büyük veri kümelerini üretebildiğini gösteriyor; bu da genomun düzenleyici “dilbilgisini” gerçekten çözmeye daha da yaklaştırıyor.
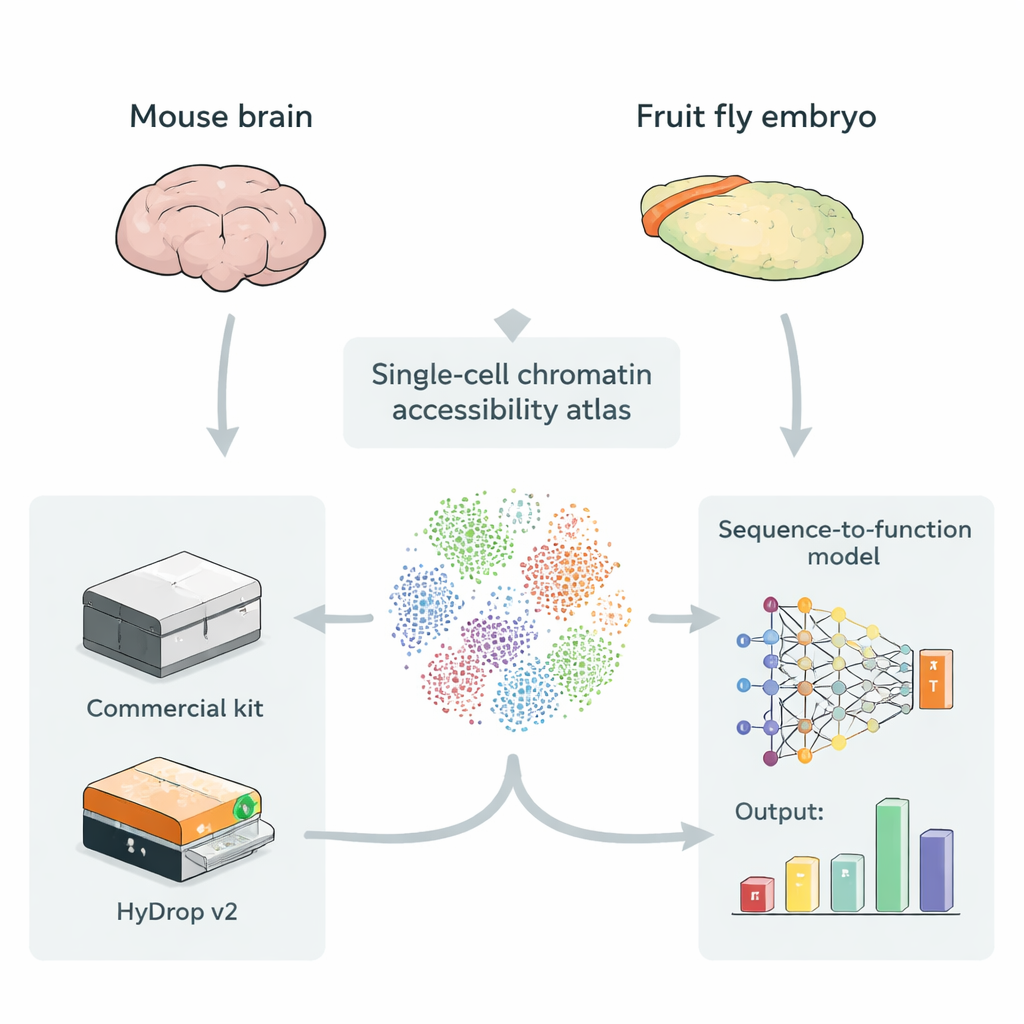
Tek hücrede açık DNA’nın haritalarını çıkarma
Enhancer’lar genellikle daha açık ve erişilebilir DNA bölgelerinde yer alır; bu, düzenleyici proteinlerin bağlanmasını kolaylaştırır. Tek hücre ATAC-seq adlı bir teknik, binlerce ila yüzbinlerce bireysel hücrede genomun hangi bölümlerinin açık olduğunu eşzamanlı olarak ölçer ve birçok hücre tipinde erişilebilir DNA’nın bir “atlasını” oluşturur. Bu atlaslar, ham DNA dizisini girdi olarak alan ve her küçük bölgenin her hücre tipinde ne kadar güçlü enhancer işlevi gördüğünü tahmin etmeyi öğrenen derin öğrenme modelleri için ideal veridir. Ancak şimdiye dek çoğu böyle atlas pahalı ticari cihazlara dayanıyordu; bu da düşük maliyetli, açık kaynak yöntemlerin bu modeller için eşdeğer eğitim verisi sağlayıp sağlayamayacağı sorusunu gündeme getiriyordu.
Ticari platformlara açık kaynaklı bir alternatif
Yazarlar, bireysel hücreleri barkodlamak için özel hidrojelle boncuklar kullanan geliştirilmiş damlacık tabanlı bir tek hücre ATAC-seq yöntemi olan HyDrop v2’yi tanıtıyor. HyDrop v2’yi yaygın kullanılan bir ticari kit ile karşılaştırmak için iki çok farklı sistemden büyük atlaslar oluşturarak kıyaslama yapıyorlar: yetişkin fare motor korteksi ve geç dönem meyve sineği embriyoları. HyDrop v2, aynı ana hücre tiplerini ve çok benzer erişilebilir DNA bölgesi setlerini geri kazanarak karşılaştırılabilir veri kalitesi üretiyor; üstelik fare beyni örneği başına maliyeti yaklaşık on dört kat daha az. Önemli olarak, HyDrop v2 deneylerinden elde edilen veriler ticari verilerle sorunsuz şekilde entegre oluyor; bu da araştırmacıların çok büyük atlaslar oluştururken platformları karıştırıp eşleştirebilecekleri anlamına geliyor.
Enhancer mantığını okumak için derin öğrenme modellerini eğitmek
Daha ucuz verilerin gelişmiş modelleme için yeterli olup olmadığını test etmek amacıyla ekip, sequence‑to‑function derin öğrenme modellerini ya ticari ya da HyDrop v2 atlasları üzerinde eğitiyor. Bu modeller, her bölgenin her hücre tipinde ne kadar erişilebilir olduğunu tahmin etmek için doğrudan DNA dizisinden öğreniyor ve muhtemelen belirli düzenleyici proteinlerin bağlanma bölgelerine karşılık gelen kısa dizi desenlerini vurgulayabiliyor. Fare korteksinde HyDrop v2 verileriyle eğitilmiş modeller, genel doğruluk ve daha önce canlı hayvanlarda doğrulanmış bilinen enhancer “anahtarlarını” geri kazanma yeteneği bakımından ticari veri modelleriyle eşleşiyor. Sinek embriyosunda her iki platform da, 2.000 baz çiftlik bölgeleri yakınlaştırıp dokuya özgü enhancer etkinliğini gerçekten sürükleyen yaklaşık 500 baz çiftlik çekirdek segmentleri belirleyebilen modelleri destekliyor; örneğin nöroblast veya kas gen ifadesini kontrol eden bölgeler gibi.
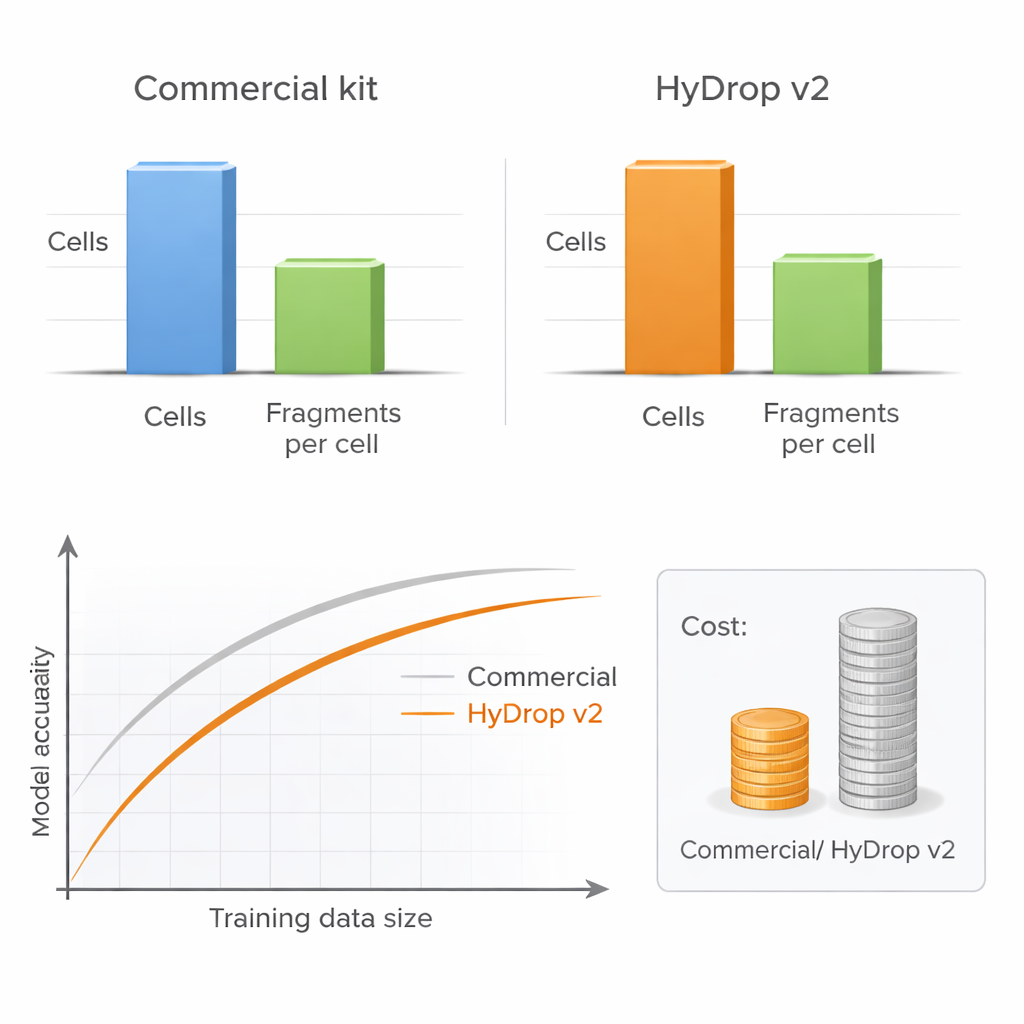
Daha fazla hücre, daha derin okumadan üstün olabilir
Her laboratuvar için pratik bir ana soru, her hücreyi çok derin dizilemek mi yoksa daha düşük derinlikte daha fazla hücreyi profillemek mi olduğu. Hücre sayısı ile hücre başına DNA fragmanı sayısını sistematik olarak değiştirerek, yazarlar model performansının yeterli sayıda hücre bulunduğu sürece orta seviyeye düşürülen dizileme derinliğinde neredeyse zarar görmediğini gösteriyor. Buna karşılık, hücre sayısının azaltılması model doğruluğunu belirgin şekilde olumsuz etkiliyor; özellikle aynı anda birçok hücre tipi arasında performans ölçülürken. HyDrop v2 hücre başına çok daha ucuz olduğundan, araştırmacılar kolayca onlarca bin ekstra hücre ekleyebilir ve maliyetin küçük bir kısmıyla ticari tabanlı modellerin performansını yakalayabilir veya hatta aşabilirler.
DNA üzerinde protein ayak izlerini görmek
Araştırma ayrıca farklı laboratuvar platformlarının ATAC‑seq enziminin DNA’yı nasıl kestiğine dair ince önyargılar getirip getirmediğini inceliyor; bunlar proteinlerin genomda nerede oturduğunu çıkarmaya çalışan modelleri yanıltabilir. Enzim tercihlerini düzelten ayrı bir sinir ağı aracını kullanarak yazarlar, HyDrop v2 ve ticari kitlerin fare ve sinek hücrelerinde neredeyse aynı enzim aktivite desenlerini ürettiğini gösteriyor. Düzeltme sonrası her iki veri seti de düzenleyici proteinlerin ve nükleozomların DNA’yı kesilmekten koruduğu ince ölçekli “ayak izleri” açığa çıkarıyor ve bu ayak izleri sequence‑to‑function modellerinin vurguladığı dizi desenleriyle örtüşüyor. Bu uyum, açık kaynaklı ve ticari platformların proteinlerin DNA ile nasıl etkileştiğinin ayrıntılı çalışmalarına eşit derecede uygun olduğunu öne sürüyor.
Genomu çözümlemek açısından bunun önemi
Uzman olmayanlar için temel mesaj şu: artık tek tek hücrelerde DNA’nın nasıl kullanıldığına dair çok büyük, uygun maliyetli haritalar oluşturabilir ve bu haritalar üzerinde güçlü derin öğrenme modelleri eğitebiliriz; bunun için yalnızca maliyetli tescilli donanımlara bağımlı olmamız gerekmiyor. HyDrop v2, yeterince hücre profillendiği takdirde enhancer tahmini, dizi desenlerinin yorumlanması ve protein bağlanma ayak izleri için önde gelen ticari yöntemlerle eşdeğer veriler sunuyor. Bu, sağlıklı ve hasta organizmaların düzenleyici öğelerinin organizma çapında atlaslarını oluşturmanın yolunu açıyor; genomun düzenleyici talimatlarını okumaya ve araştırma ile gelecekteki tedaviler için yeni, hassas hedefli genetik anahtarlar tasarlamaya yönelik çalışmaları hızlandırıyor.
Atıf: Dickmänken, H., Wojno, M., Mahieu, L. et al. Evaluating single-cell ATAC-seq atlasing technologies using sequence-to-function modeling. Nat Commun 17, 1951 (2026). https://doi.org/10.1038/s41467-026-68742-4
Anahtar kelimeler: tek hücre ATAC-seq, enhancer'lar, derin öğrenme modelleri, gen düzenlenmesi, açık kaynak genomik