Clear Sky Science · tr
Kininürenin, kemoterapi kaynaklı bağırsak toksisitesini bağırsak mikrobiyotası yoluyla düzenleyerek aracılık ediyor
Kemoterapi gören kişiler için neden önemli
Kemoterapi hayat kurtarıyor, ancak çoğunlukla bağırsakta şiddetli yan etkilerle birlikte gelir—ağrı, ishal, kilo kaybı—ve bu durum doktorları dozları azaltmaya veya tedaviyi erken sonlandırmaya zorlayabilir. Bu çalışma, kan dolaşımındaki bir kimyasal, bağışıklık hücreleri ve bağırsak mikropları arasında gizli bir zincir reaksiyonunu ortaya koyuyor; bu, yaygın bir kanser ilacı olan oksaliplatinin bağırsaklar üzerinde neden bu kadar yıpratıcı olabildiğini açıklamaya yardımcı oluyor ve hastaları kanserle mücadelede zayıflatmadan korumanın yeni yollarına işaret ediyor.
Tedavi ile bağırsak hasarı arasında kimyasal bir bağlantı
Araştırmacılar işe oksaliplatin bazlı kemoterapi gören kolorektal kanser hastalarından başladı. Şiddetli bağırsak yan etkileri geliştirenlerle tedaviyi daha iyi tolere edenlerin kan örneklerini karşılaştırdılar. Hedefe yönelik kimyasal profilleme kullanarak, amino asit triptofana ait birkaç parçalanma ürününün yüksek toksisite grubunda daha fazla olduğunu ve L‑kinurenin adlı bir molekülün en belirgin şekilde yükseldiğini buldular. Kanda daha fazla L‑kinurenin bulunan hastalar aynı zamanda daha fazla inflamasyon belirtisi ve daha düşük beyaz kan hücresi sayıları gösteriyordu; bu da bu molekülün tedaviyle ilişkili hasarla doğrudan bağlantılı olabileceğine işaret ediyordu.
Farelerde nedenselliği kanıtlamak
Korelasyonun ötesine geçmek için ekip fare modellerine yöneldi. Sağlıklı farelere yüksek doz oksaliplatin verildiğinde, klasik bağırsak hasarı belirtileri gelişti: kilo kaybı, kısalmış kolonlar, bağırsak duvarında şişlik, daha az bölünen hücre ve bağırsak yüzeyinde daha fazla hücre ölümü. Bu farelerde kan L‑kinurenin düzeyleri de insan verilerini yansıtarak keskin biçimde arttı. Araştırmacılar oksaliplatin tedavisi gören farelere ek L‑kinurenin verdiğinde bağırsak hasarı daha da kötüleşti—ancak ilacın tümörlere karşı kanser öldürücü etkisi bozulmadı. Tam tersine, triptofandan L‑kinurenine dönüştürülmesinde görevli IDO1 enzimini kaldırıp bloke ettiklerinde, fareler bağırsak toksisitesine karşı çok daha dirençli oldu ve yine de kemoterapiden yarar gördü.
Hedefteki bağışıklık hücreleri ve bağırsak mikropları
Daha derine inerken bilim insanları, tedavi sırasında fazla L‑kinurenin üretiminden hangi hücrelerin sorumlu olduğunu sordular. Oksaliplatinin belirli bağışıklık hücrelerini (CD8 T hücreleri) interferon‑gamma adlı haberci proteini salmaya teşvik ettiğini, bunun da yakındaki miyeloid hücrelerde—bir tür beyaz kan hücresi—IDO1’i açtığını buldular. Sadece miyeloid hücrelerinde IDO1 olmayan şekilde tasarlanmış fareler çok daha az L‑kinurenin üretti ve bağırsak hasarından korundu; oysa yalnızca bağırsak örtü hücrelerinde IDO1’i silmek neredeyse etkisiz kaldı. Aynı zamanda bağırsak mikrobiyotasının bileşimi değişti. Normal farelerde oksaliplatin ve yüksek L‑kinurenin düzeyleri, yararlı bir bakteri olan Lactobacillus johnsonii’nin kaybıyla ilişkilendirildi. Buna karşılık L‑kinurenin düzeyi azaltılmış farelerde L. johnsonii daha yüksek seviyelerde korundu. Bağırsak bakterileri antibiyotiklerle silindiğinde, düşük L‑kinureninin koruyucu etkisi ortadan kalktı; ve düşük‑kinurenin farelerinden alınan bakteriler normal farelere nakledildiğinde, bu alıcılar oksaliplatinin bağırsak hasarına karşı daha dayanıklı hale geldi.
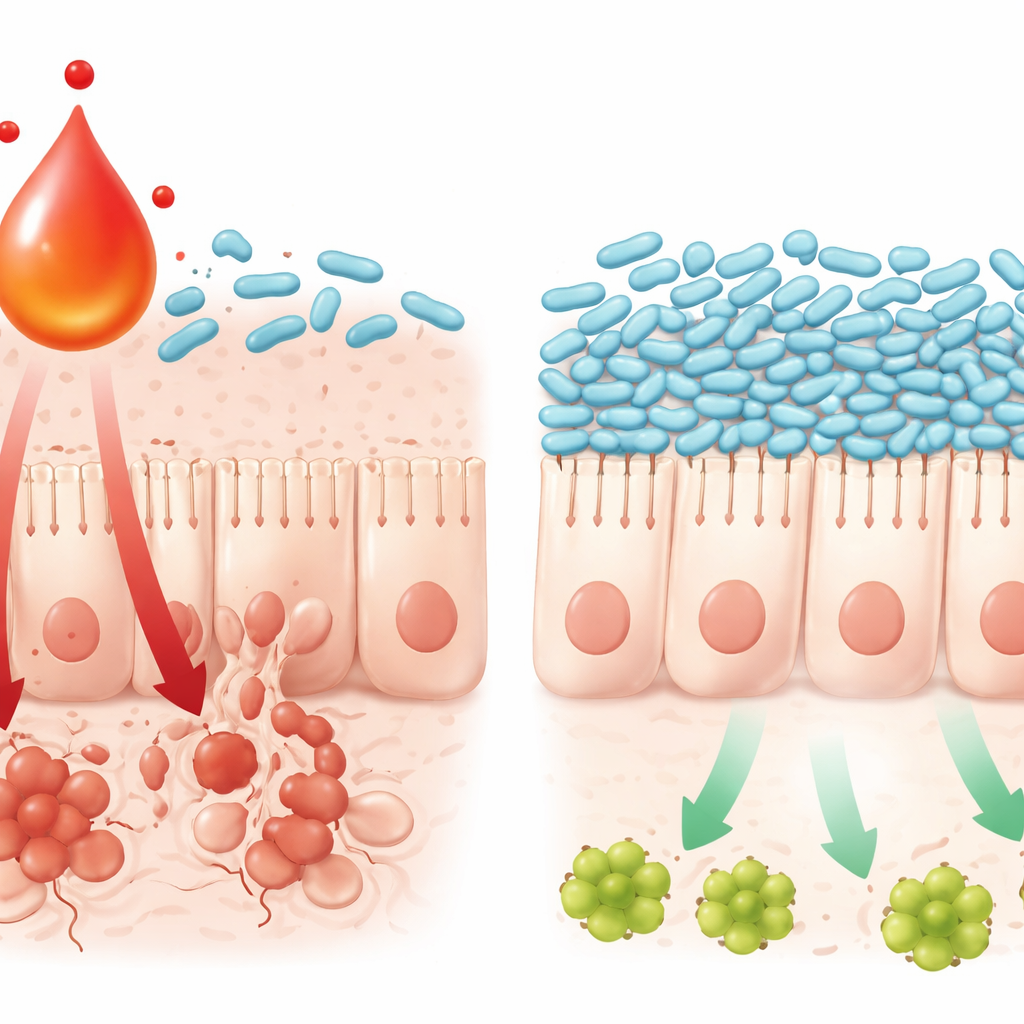
Tek bir metabolit bağırsakta hücre ölümünü nasıl tetikliyor
Çalışma ayrıca bu kimya–mikrop etkileşiminin bağırsak örtüsünü nasıl yaraladığını izledi. Yüksek L‑kinurenin düzeyleri, bağırsak dokusunda iyi bilinen inflamatuar bir yol olan TNFα/JNK yolunun artmış aktivitesiyle ilişkilendirildi; bu yol hücreleri programlı ölüme yönlendiriyor. Hücre kültüründe oksaliplatin ile L‑kinurenini birlikte uygulamak, bağırsak hücrelerinde bu yolun daha kolay aktive olmasına ve hücre ölümüne yol açtı; oysa L. johnsonii bakterisini eklemek sinyali zayıflattı ve hücre hayatta kalmasını korudu. L‑kinurenin kendi başına da laboratuvar şartlarında L. johnsonii’nin büyümesini yavaşlatabiliyor ve hayatta kalma mekanizmalarını zayıflatabiliyordu; bu, metabolit birikince bakterinin neden kaybolduğunu açıklamaya yardımcı oluyor. Birlikte ele alındığında, bulgular kendini güçlendiren bir döngüyü özetliyor: kemoterapi bağışıklık sinyalini tetikliyor, bağışıklık hücreleri L‑kinurenini artırıyor, bu dost bakteriler gibi türleri bozuyor ve değişen mikrobiyal topluluk da bağırsaktaki hücreleri öldüren inflamatuar sinyalleri güçlendiriyor.
Tedavi sırasında hastaları korumanın yeni yolları
Ümit verici olarak çalışma pratik stratejilere de işaret ediyor. IDO1’i inhibe eden Epacadostat adlı bir ilaçla fareleri tedavi etmek, L‑kinurenin düzeylerini düşürdü ve oksaliplatin kaynaklı bağırsak hasarını belirgin şekilde azalttı; üstelik tümör kontrolünü zayıflatmadı. Tamamlayıcı bir yaklaşımda, ekip bağırsağa L‑kinurenini parçalayan bir enzimi aşırı üretecek şekilde zararsız bir E. coli suşunu genetik olarak tasarladı. Bu mühendislikli bakteriler verilen fareler de benzer şekilde bağırsak toksisitesinden korundu ve yine kemoterapinin kanser karşıtı etkisine zarar gelmedi. L. johnsonii’nin kendisini takviye etmek de semptomları hafifletti ve bağırsak yapısını korudu.
Kanserli insanlar için bunun anlamı
Toparlanacak olursa, bu çalışma tek bir tedavi kaynaklı metabolit olan L‑kinureninin kemoterapi, bağışıklık sistemi, bağırsak mikropları ve bağırsak yaralanması arasında önemli bir aracı olarak davrandığını ortaya koyuyor. Üretimini engellemenin, yıkımını artırmanın veya koruyucu bakterileri geri getirmenin kemoterapinin bağırsak üzerindeki etkisini hafifletebileceğini göstererek, araştırma hastaların kanserle mücadele ederken daha güçlü ve daha rahat kalmalarını sağlayacak ek tedavilere doğru bir yol açıyor.
Atıf: Xie, H., Yang, J., Wu, J. et al. Kynurenine mediates the chemotherapy-induced intestinal toxicity through modulation of gut microbiota. Nat Commun 17, 2087 (2026). https://doi.org/10.1038/s41467-026-68741-5
Anahtar kelimeler: kemoterapi yan etkileri, bağırsak mikrobiyomu, triptofan metabolizması, L-kinurenin, kolorektal kanser