Clear Sky Science · tr
Tümör kaynaklı özellikler, öncü durumdan semptomatik multipl miyeloma geçişine kadar T hücresi farklılaşmasını şekillendiriyor
Bu araştırma neden önemli
Multipl miyelom, kemik iliğinde oluşan bir kanserdir ve neredeyse her zaman tam hastalığa dönüşebilecek veya dönüşmeyebilecek daha sessiz, erken aşama durumlar tarafından önceden takip edilir. Birçok insan bu öncüllerle yıllarca yaşar ve ilerleyip ilerlemeyeceklerinden emin olamaz. Bu çalışma çağdaş bir soruyu gündeme getiriyor: miyelomun nasıl geliştiğini, tedaviye nasıl yanıt verdiğini ve kimin ilerleme riski en yüksek olduğunu anlamak için bağışıklık sisteminin—özellikle T hücrelerinin—“ruh halini” ve geçmişini okuyabilir miyiz?
Vücudun kanserle savaşan keşif birimleri
T hücreleri, kanserler de dahil olmak üzere anormal hücreleri tanıyıp yok edebilen çok yönlü bağışıklık hücreleridir. Akciğer veya deri kanserleri gibi katı tümörlerde uzun süreli uyarı, T hücrelerini etkisiz hale getiren bir tükenme durumuna itebilir; modern immünoterapiler bu durumu tersine çevirmeye çalışır. Yazarlar, multipl miyelomlu kişiler, onun öncü evreleri (MGUS ve sönümlü miyelom) ve kanser olmayan kontrollerin kemik iliği ve kanından bir milyondan fazla hücreyi içeren büyük bir tek hücre haritası derlediler. Hem gen aktivitesini hem de her T hücre klonunu tanımlayan benzersiz reseptör dizilerini okuyarak T hücrelerinin nasıl organize olduğunu, ne kadar “yaşlı” veya “deneyimli” göründüklerini ve tümörle ne kadar yakın ilişki içinde olduklarını yeniden kurguladılar.
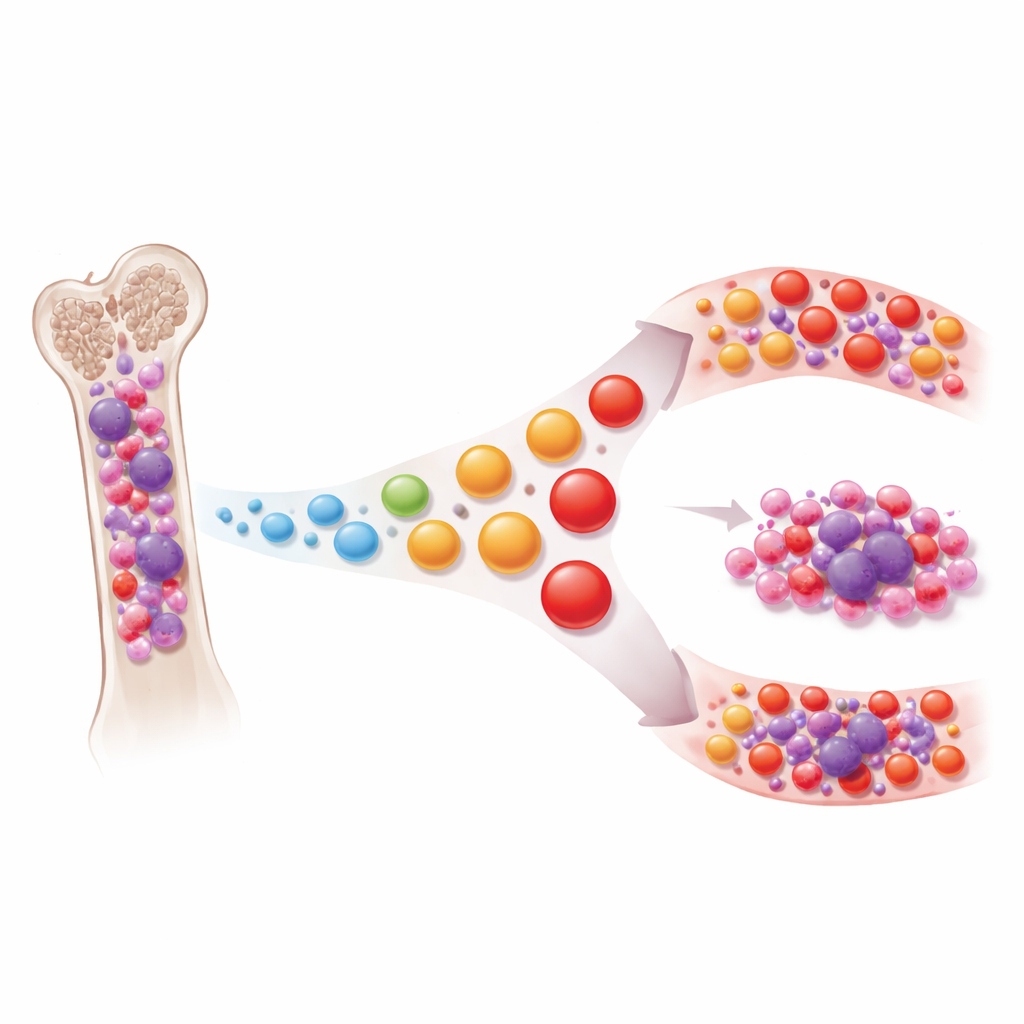
Yorgun değil, ama erken yaşlanmış
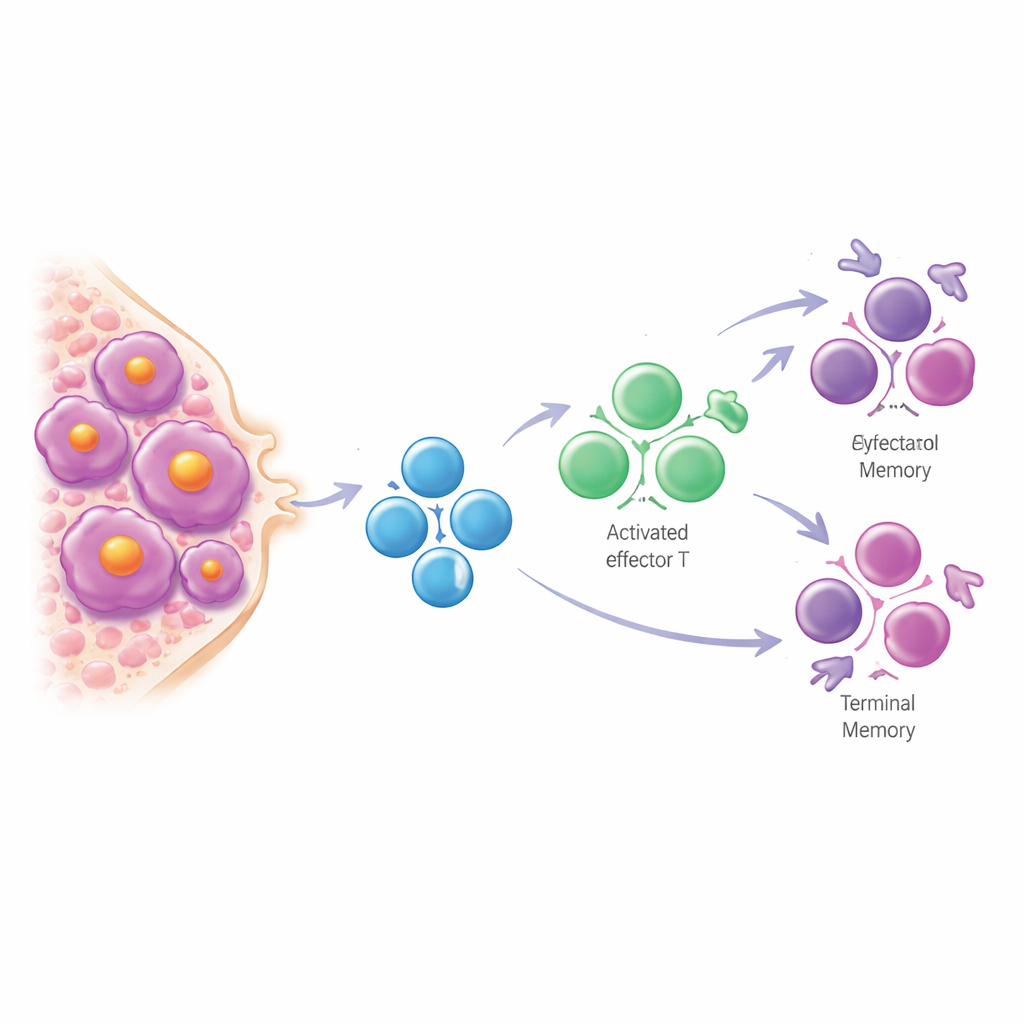
Birçok katı kanserde görülenin aksine ekip, miyelomda T hücrelerinin nadiren gerçekten tükenmiş olduğunu buldu. Klasik tükenme belirteçlerini taşıyan hücreler büyük ölçüde tek bir sıra dışı hastayla sınırlıydı. Bunun yerine, sönümlü ve semptomatik miyelom hastalarının kemik iliğindeki T hücreleri, naif, erken evre hücrelerden uzaklaşıp yaşlı bireylerde görülenlere benzeyen yüksek deneyimli “terminal bellek” tiplerine kaydı. T hücresi kayması olarak adlandırılan bu desen, bağışıklık sisteminin doğal yaşlanmasını yansıttı ancak hastalarda abartılı görünüyordu; sanki T hücreleri vücudun geri kalanından daha hızlı yaşlanmıştı. Hastalık ne kadar ilerlemiş ve tümör yükü ne kadar yüksekse, geç evre bellek hücrelerine doğru bu kayma o kadar güçlüydü ve benzer değişiklikler kana da yansıyordu.
T hücresi parmak izlerinden ipuçları
Her T hücresi benzersiz bir reseptör taşır ve aynı reseptör dizisini paylaşan hücreler, bir tetikleyiciye yanıt olarak genişlemiş bir klona aittir. Bu reseptörleri izleyerek araştırmacılar, miyelom iliğinin güçlü öldürücü hücre özellikleri gösteren birçok genişlemiş T hücre klonuna sahip olduğunu gösterdi. Bu klonlar ağırlıklı olarak yaygın virüsleri tanımıyordu. Bunun yerine güçlü sitotoksik mekanizmalarla ilişkili, belirgin bir “viral olmayan” gen imzasına sahiptiler ve miyelomlu kişilerde öncü evrelere kıyasla zenginleşmişti. Yüzeylerinde protein parçalarını sunma konusunda daha yetkin olan tümörler—antijen sunumu genlerinin daha yüksek aktivitesi yoluyla—genellikle bu viral olmayan, yüksek derecede farklılaşmış T hücreleriyle ilişkiliydi. Tümörleri bu daha güçlü immün etkileşimi gösteren hastalar genel olarak daha iyi sağkalıma sahipti; bu da bu T hücrelerinin en azından kısmen gerçekten tümöre karşı etkili olduğunu düşündürüyor.
Tedavi, nüks ve erken uyarı işaretleri
Çalışma ayrıca otolog kök hücre nakli geçiren hastaları da izledi; bu yaygın bir yoğun tedavidir. Nakilden sonra T hücre reseptör repertuarı birkaç büyük klon tarafından daha fazla domine edildi. Bu genişleyen klonların birçoğu, tedaviden önce zaten var olan ve aynı viral olmayan, miyelomla ilişkili imzayı taşıyan terminal farklılaşmış CD8 T hücrelerine kadar izlenebiliyordu. Nakil sonrası hâlâ rezidüel kansere sahip olan hastalar özellikle klonal, eğilimli T hücre repertuarlarına sahip olma eğilimindeydi; bu, güçlü ama yaşa benzer bir T hücresi yanıtının hastalığı tamamen temizlemekte başarısız olabileceğini öne sürüyor. Hastalığın daha erken dönemlerine bakıldığında, daha sonra aktif miyeloma ilerleyen sönümlü hastaların genellikle düzenleyici CD4 T hücrelerinde düşüş gösterdiği bulundu—bu hücreler normalde bağışıklık yanıtlarını ve kemik iliği ortamını dengede tutmaya yardımcı olur. Bu hücrelerin düşük seviyeleri, mevcut klinik risk puanlarından bağımsız olarak daha hızlı ilerlemeyi öngörüyordu.
Bu hastalar için ne anlama geliyor
Miyelom ve onun öncül evreleriyle yaşayan kişiler için bu çalışma, bağışıklık sisteminin kanserle nasıl etkileştiğine dair çerçeveyi yeniden kuruyor. T hücreleri basitçe tükenmek yerine, miyelomda T hücreleri tümör hücreleriyle süregelen mücadeleler nedeniyle kronik olarak geç, yaşlı bir duruma itiliyor gibi görünüyor. Bu eğilimli, klonal T hücresi manzarası tümör yükünü yansıtıyor, nakil ve T hücresi hedefli ilaçlar gibi tedavilere yanıtı şekillendiriyor ve düzenleyici T hücre kaybı durumunda sönümlü hastalardan semptomatik hastalığa ilerleme riski yüksek bireyleri işaret edebiliyor. Uzun vadede bu bulgular, T hücrelerini tazeleyip yönlendiren yeni immünoterapilere rehberlik edebilir ve klinisyenlerin izlemeyi ve erken müdahaleyi zamanlamak için bağışıklık özelliklerini geleneksel belirteçlerle birlikte daha kesin kullanmalarına yardımcı olabilir.
Atıf: Foster, K.A., Rees, E., Ainley, L. et al. Tumour-intrinsic features shape T cell differentiation through precursor to symptomatic multiple myeloma. Nat Commun 17, 2400 (2026). https://doi.org/10.1038/s41467-026-68718-4
Anahtar kelimeler: multipl miyelom, T hücreleri, bağışıklık yaşlanması, tek hücre dizilemesi, kanser immünolojisi