Clear Sky Science · tr
Escherichia coli'de moleküllerin birikimini tıklama tabanlı belirleme
Neden küçük ilaçlar tehlikeli bakterilere ulaşmakta zorlanıyor
Modern tıp antibiyotiklere dayanıyor, ancak en tehlikeli bakterilerden bazıları artık birçok ilacı dışarıda tutan sağlam dış duvarlarla korunuyor. Escherichia coli gibi Gram-negatif bakteriler özellikle etkili bir dış zar bariyerine sahip olup, gerçekten hücre içine girip hedeflerine ulaşan ilaçlar tasarlamayı zorlaştırıyor. Bu makale, CHAMP testi adı verilen yeni bir laboratuvar yöntemini tanıtıyor; bu yöntem bilim insanlarının binlerce farklı küçük molekülün bu savunmaları ne kadar kolay aşabildiğini ve canlı E. coli hücrelerinin içinde ne ölçüde biriktiğini hızla ölçmesine olanak sağlıyor.
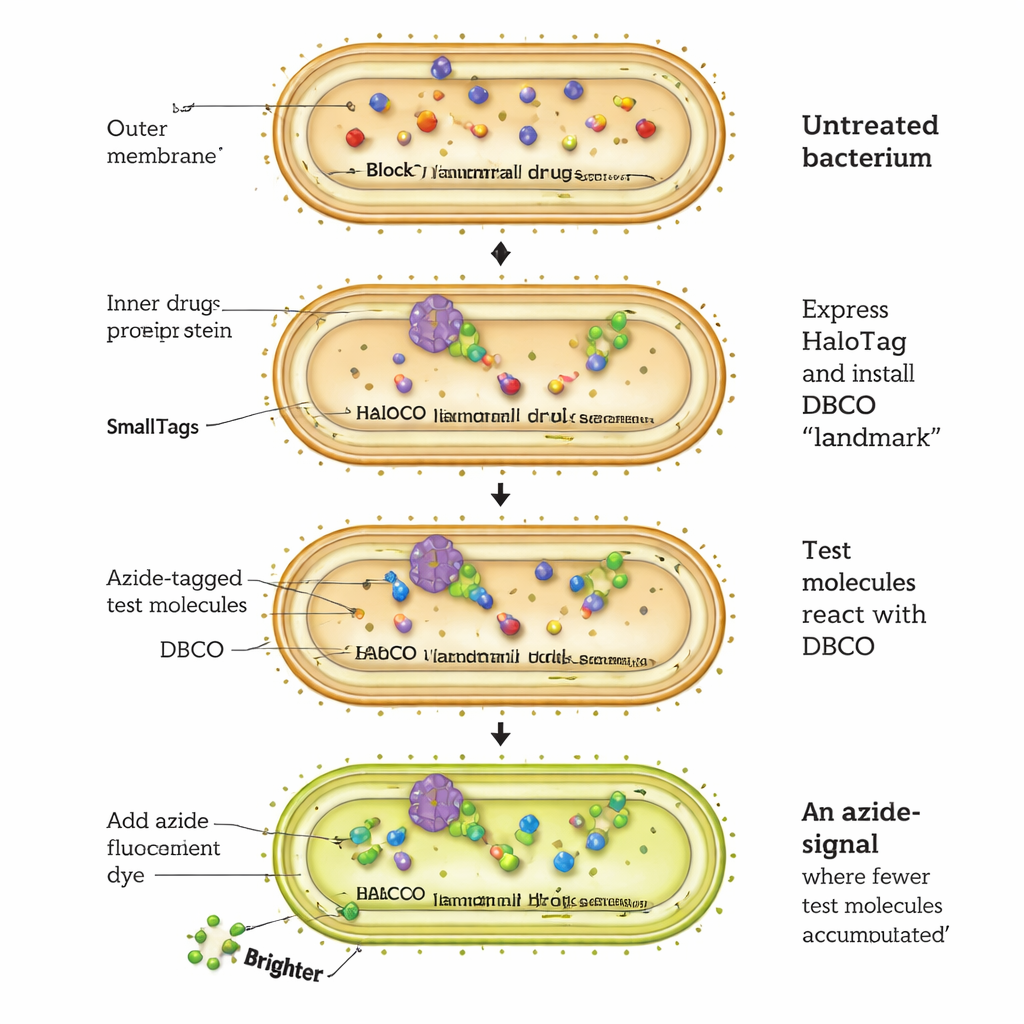
İlaçların bakteri hücrelerine girişini izlemenin yeni yolu
Geleneksel antibiyotik keşfi, doğal olarak bulunan bileşiklere ve bakterilerin yaşayıp ölmediğini gösteren basit büyüme testlerine dayanıyordu. Bu testler, ilacın gerçekten hücre içine ne kadar girdiğini veya içeri girdikten sonra nereye gittiğini ortaya koymaz. Yazarlar, ilaç girişini bakteriyel sitozole — birçok antibiyotik hedefinin bulunduğu sıvı içeriğe — doğrudan ve yaygın şekilde kullanılabilecek bir yöntemle izlemeyi hedeflediler. Amaçları, ilaç alımı, hedef bağlanması ve sonraki biyoloji etkilerini karıştıran minimum inhibitör konsantrasyonu gibi kaba göstergelerin ötesine geçip, hücre içi birikimin temiz bir ölçümünü elde etmekti.
Bakterileri küçük kimyasal kayıt cihazlarına dönüştürmek
CHAMP testi, HaloTag adlı bir bakteri proteinini bir tür moleküler iniş pisti haline getirecek şekilde yeniden düzenleyerek çalışır. E. coli hücreleri sitozollerinde HaloTag üretmeleri için genetik olarak değiştirilir. Araştırmacılar önce kısa bir kloroalkane bağlayıcı kullanarak HaloTag'e "gerilmiş" bir alkin olan DBCO adlı özel bir kimyasal tutamaç bağlar. Ardından, her biri çok küçük bir azid etiketi taşıyan test moleküllerine bakterileri maruz bırakırlar. Yalnızca dış zarı geçen, iç zarı aşan ve sitozole ulaşan test molekülleri, yüksek seçicilikte bir "click" reaksiyonuyla DBCO tutamaç ile reaksiyona girerek HaloTag'i kalıcı olarak işaretler. Son olarak, hücrelere kalan boş DBCO'ya bağlanabilen azid-etiketli bir floresan boya uygulanır. Floresans ne kadar parlaksa, sitozole o kadar az test molekülü ulaşmıştır; daha sönük hücreler ise daha iyi birikimi gösterir.
Kimya ve biyolojinin ilaç girişini nasıl şekillendirdiğini araştırmak
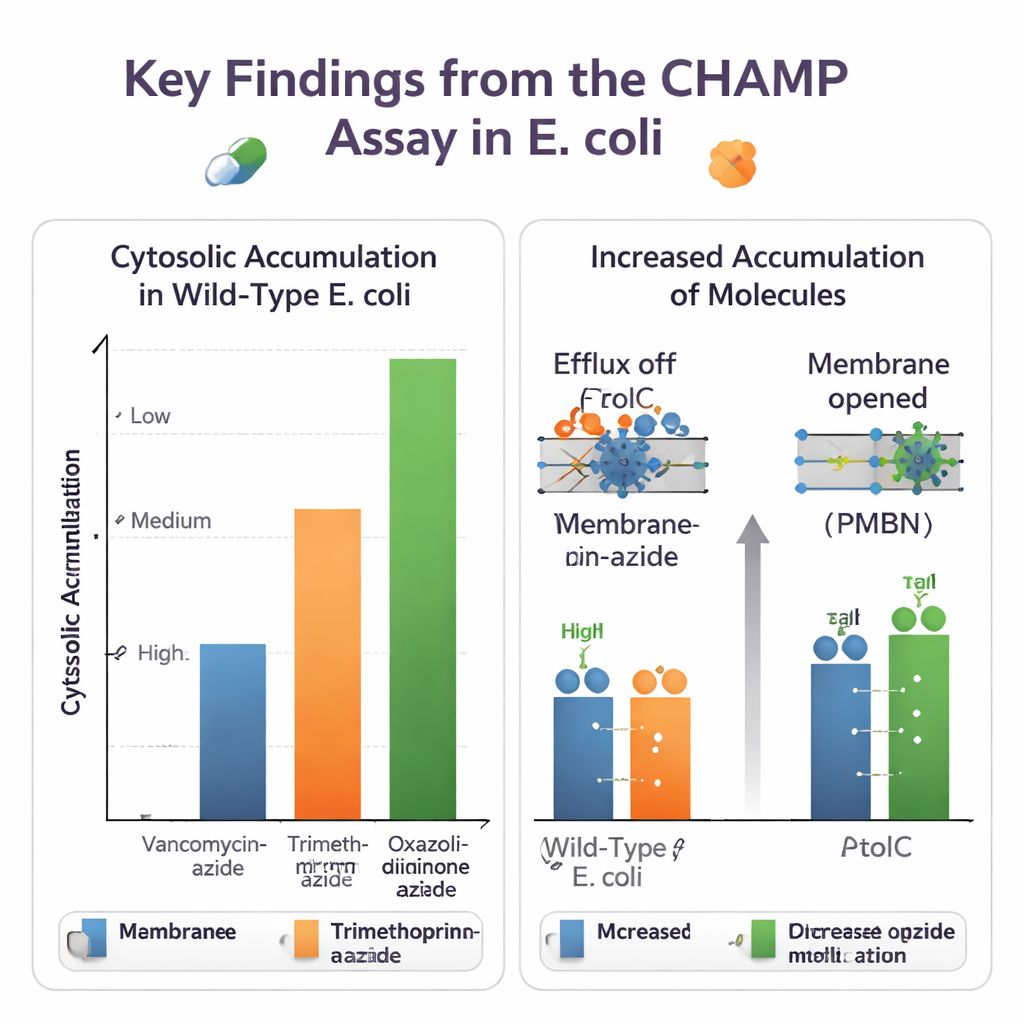
CHAMP kullanılarak ekip önce HaloTag ifadesini, DBCO bağlayıcısının miktarını ve güvenilir geniş bir sinyal penceresi elde etmek için floresan boyaların seçimlerini hassaslaştırdı. Ardından, kimyasal ince ayarların girişe nasıl etki ettiğini görmek için birbirine yakın küçük molekül setleri kullandılar. Karboksilik asitleri amidlere dönüştürmek ve bazik amino gruplar eklemek veya çıkarmak, sitozolik düzeyleri belirgin şekilde değiştirebiliyordu. Birçok durumda primer aminler birikimi artırdı; bu, diğer gruplar tarafından geliştirilen bağımsız "eNTRy kuralları"yla uyumlu sonuçlar verdi. Test, azid-etiketli gerçek antibiyotik versiyonlarını da işleyebildi ve büyük farklılıkları ortaya koydu: vankomisin gibi hacimli ilaçlar neredeyse hiç sitozole ulaşamazken, trimethoprim türevleri ve bazı oksazolidinonlar gibi daha küçük antibiyotikler çok daha kolay girdi.
İlaçları geri pompalayan bakteriyel savunmaları ortaya çıkarmak
Yöntem canlı, genetik olarak programlanabilir bakterilerde çalıştığı için farklı hücresel savunmaların rollerini ayırmak mümkün oluyor. Yazarlar normal E. coli'yi, büyük çoklu ilaç sürükleme pompasının kilit bir bileşeni olan TolC'yi eksik bırakan suşlarla veya küçük moleküllü bir TolC inhibitörüyle muamele edilmiş hücrelerle karşılaştırdı. Novobiocin ve birkaç diğer azid-etiketli antibiyotik için CHAMP, TolC devre dışı bırakıldığında net şekilde daha yüksek sitozolik birikim gösterdi ve bu bileşikleri sürükleme substratları olarak doğruladı. Ayrıca dış zar bariyerini gevşetme yollarını, peptid PMBN ile kimyasal olarak veya geniş açık bir porin kanalını fazla eksprese ederek genetik olarak test ettiler. Önceden zayıf biriken birçok molekül, zar geçirgenliği artırıldığında büyük kazançlar gösterdi; bu da giriş ve sürüklemenin iç ilaç düzeylerini birlikte belirlediğini vurguluyor.
Desenler ve kurallar için binlerce moleküle ölçeklemek
Gerçek yüksek verimliliği göstermek için araştırmacılar, ticari 404 azid-etiketli bileşiklik bir set ve 1.152 azid taşıyan molekülden oluşan özel bir kütüphaneyi taradılar. Birikimi, işlenmemiş hücreler, PMBN ile muamele edilmiş hücreler, hiperporine olmuş hücreler ve TolC eksik hiperporine hücreler dahil olmak üzere çeşitli bakteriyel bağlamlarda ölçtüler. Aynı molekülü bu koşullar arasında karşılaştırarak hangi değişikliklerin click reaksiyon hızının tuhaflıklarından ziyade hücre biyolojisinden kaynaklandığını ayırt edebildiler. CHAMP verilerini hesaplamalı analizle birleştirerek, polar yüzey alanı, hidrojen-bağlama kapasitesi ve belirli halka iskeletleri gibi bazı fizikokimyasal özelliklerin TolC-tabanlı sürükleme tarafından daha güçlü tanınmayla bağlantılı olduğunu gösterdiler. Bu tür büyük ölçekli profilleme, pompalardan kaçan veya porinleri daha etkili kullanan moleküller tasarlamak için kuralları çizmeye başlıyor.
Gelecek antibiyotikleri için bunun anlamı
Basitçe söylemek gerekirse, bu çalışma E. coli'yi birçok ilaç hedefinin bulunduğu hücre bölgesine ne kadar test bileşiği girdiğini rapor eden yüksek verimli bir sensöre dönüştürüyor. CHAMP bakterilerin öldürülüp öldürülmediğini test eden yöntemlerin yerini almıyor, ancak "içeri girmek" ile "zarar vermek" arasındaki kritik boşluğu dolduruyor. Farklı mutant veya kimyasal olarak değiştirilmiş suşlarda binin üzerinde molekülü günler içinde ölçebilme yeteneğiyle araştırmacılar artık hangi kimyasal özelliklerin girişi teşvik ettiğini, sürüklemeyi azalttığını veya zararı bozucu ortaklardan yarar sağladığını sistematik olarak öğrenebilir. Bu bilgi, Gram-negatif patojenlerin zorlu savunmalarını aşabilecek yeni antibiyotiklerin ve yardımcı ilaçların tasarımını, direnç daha fazla antibiyotik cephanesini ele geçirmeden hızlandırmalıdır.
Atıf: Ongwae, G.M., Liu, Z., Feng, S. et al. Click-based determination of accumulation of molecules in Escherichia coli. Nat Commun 17, 2008 (2026). https://doi.org/10.1038/s41467-026-68717-5
Anahtar kelimeler: antibiyotik direnci, Escherichia coli, ilaç geçirgenliği, sürükleme pompaları, click kimyası