Clear Sky Science · tr
Hastadan elde edilen R252C mutasyonunun alternatif bir EGFR aktivasyonu kanser ilerlemesini teşvik ediyor
Hücre Antenleri Kontrolden Çıktığında
Bazı kanserler neden kemoterapi ve ileri düzey immünoterapi uygulamalarından sonra bile büyümeye devam eder? Bu çalışma, hem akciğer hem de beyin tümörleri olan bir hastayı izliyor ve hastalığı hücre yüzeyindeki kritik bir "anten" olan EGFR’deki küçük bir değişikliğe kadar geriye götürüyor. Bu tek mutasyonun büyüme sinyallerini nasıl yeniden yapılandırdığını ortaya koyarak araştırmacılar, yalnızca hastanın agresif kanserini açıklamakla kalmıyor, aynı zamanda mevcut bir ilaç olan afatinibin bunu nasıl kontrol altına alabileceğini gösteriyor.
Büyük Sonuçları Olan Nadir Bir Mutasyon
EGFR, hücre zarını geçen ve hücrelerin büyüme uyarılarına yanıt vermesine yardımcı olan bir reseptördür. Birçok akciğer ve beyin kanserinde EGFR’de mutasyonlar bulunur, ancak bilinen değişikliklerin çoğu hücre içinde, enzimi anahtarlayan bölümde yer alır. Burada ekip, EGFR’nin dış tarafında, normalde büyüme faktörlerini yakalayan bölümünde alışılmadık bir değişiklik keşfetti. Hem akciğer kanseri hem de gliomu olan bir hastada, 252. pozisyondaki bir amino asidin arginin’den sisteine değiştiği—EGFR R252C olarak adlandırılan—bulundu. Kanser veritabanları incelendiğinde bu mutasyonun bir grup gliom hastasında görüldüğü, akciğer tümörlerinde ise neredeyse hiç rastlanmadığı ortaya çıktı; bu da onun nadir ama gerçek olduğunu düşündürdü. Yazarlar, bu mutasyonun ne yaptığını test etmek için gen düzenleme araçlarıyla aynı mutasyonu birkaç insan beyin ve akciğer kanseri hücre hattında yeniden yarattılar.
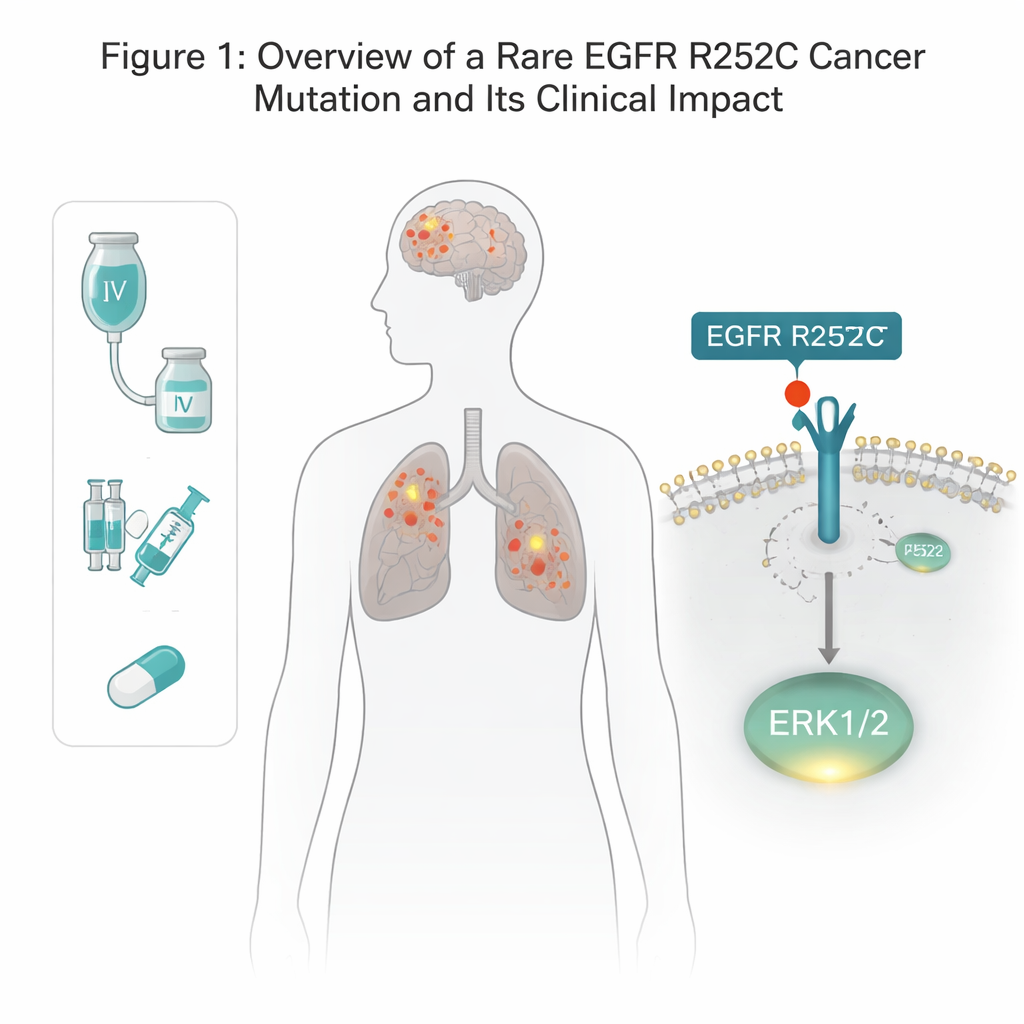
Büyüme Sinyallerine Yeni Bir Kısayol
Normalde EGFR’in etkinleşebilmesi için başka bir kopyayla eşleşmesi ve ardından iç kuyruklarını fosfat gruplarıyla etiketlemesi gerekir, böylece aşağı akıştaki büyüme yolları açılır. İlginç bir şekilde, R252C versiyonu bu alışılmış oto-fosforilasyon görünümünü göstermedi. Bunun yerine, EGFR R252C taşıyan hücreler, AKT ve STAT3 gibi klasik EGFR yollarını büyük ölçüde değiştirmeden, ERK1/2 adlı belirli bir büyüme düzenleyicisini normalden çok daha güçlü şekilde açtı. ERK1/2’yi hedef alan bir inhibitörle bloke etmek, R252C hücrelerinin ek büyüme üstünlüğünü ortadan kaldırdı; bu da ERK1/2’nin bu mutantın tümör sürücü gücünün ana motoru olduğunu kanıtladı.
Reseptörün Sürekli Açık Bir Konuma Kilitlenmesi
Dışsal bir değişikliğin nasıl bu tür seçici bir aşırı etkinleşmeye yol açabildiğini anlamak için araştırmacılar biyokimyasal deneyleri bilgisayar simülasyonlarıyla birleştirdiler. R252C değişimi EGFR’nin dış kısmına yeni bir sistein ekliyor. İki böyle mutant, C252 reziduları arasında bir disülfit bağı—bir tür moleküler zımba—oluşturarak onları birlikte kararlı bir çift halinde kilitleyebilir. Yapısal modelleme, bu bağın reseptörün dışını, liganda bağlı aktif formu yakından taklit eden “V-şeklinde” ve kaymalı bir hizalanmaya zorladığını gösterdi, üstelik herhangi bir büyüme faktörü olmadan. Bu hizalanma, zar boyunca ve zarın hemen içindeki bölümlere iletilerek içteki enzim domainlerini sıradışı bir düzene büküyor: aktif bölgeler hücre içine dönük ama birbirlerini verimli biçimde fosforlayamayacak kadar uzak tutuluyor. Bunun yerine bu konformasyon ERK1/2 için güçlü bir bağlanma yüzeyi oluşturuyor ve EGFR R252C’nin ERK1/2’yi doğrudan fosforlayarak klasik RAS–RAF–MEK rölesini atlamasına olanak tanıyor.
Fare Modellerinden Tek Bir Hastaya
Yazarlar, EGFR R252C taşıyan beyin ve akciğer kanseri hücrelerinin kültürde daha hızlı büyüdüğünü ve normal EGFR taşıyan hücrelere kıyasla farelere implante edildiğinde daha büyük, daha agresif tümörler oluşturduğunu gösterdiler. Ardından birkaç nesil EGFR-engelleyici hapı test ettiler. Sadece ikinci nesil bir inhibitör olan afatinib, tutarlı şekilde ERK1/2 aktivasyonunu kapattı ve tümör hücresi büyümesini keskin biçimde azalttı. R252C tarafından sürülen beyin ve akciğer tümörlerinin fare modellerinde afatinib tümör büyümesini yavaşlattı ve sağkalımı uzattı. Kritik olarak, orijinal hasta—hastalığı kemoterapi, damar-hedefli bir ilaç ve immünoterapiye rağmen kötüleşen—afatinibe geçirildiğinde, hem akciğer hem beyin taramalarında tümör yükünde belirgin küçülme görüldü ve hasta birkaç yıl progresyonsuz bir dönem yaşadı.
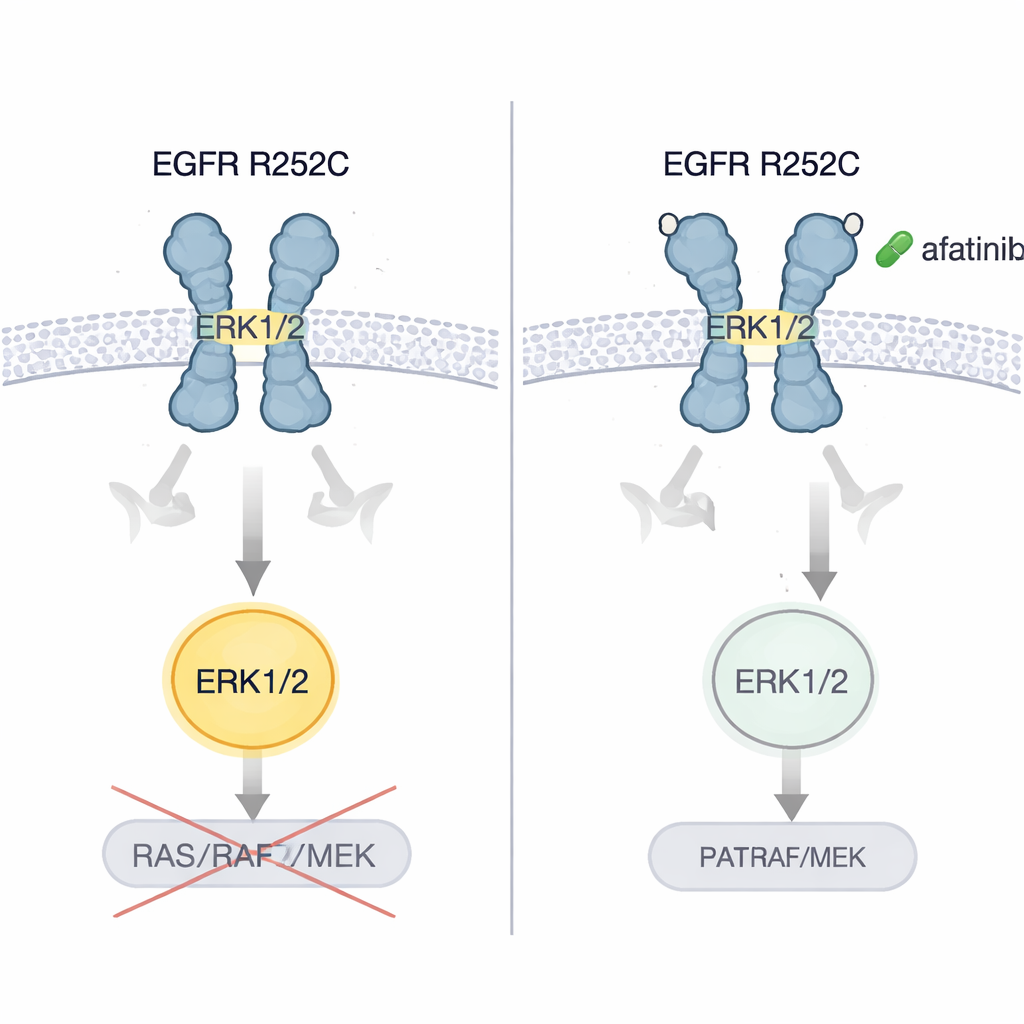
Bu Hastalar İçin Ne Anlama Geliyor
Bu çalışma, kansere yol açan bir EGFR mutasyonunun daha önce tanınmamış bir şekilde çalışabileceğini ortaya koyuyor: iki reseptörü hücrenin dışında zımbalayarak, onları ERK1/2’yi doğrudan açan aktif bir pozisyona bükmek ve böylece ders kitaplarındaki sinyal zincirini izlememek. Uzman olmayanlar için ana çıkarım, aynı gendeki tüm mutasyonların aynı davranmadığı ve nadir değişikliklerin bazı mevcut ilaçlara özellikle duyarlı olabileceğidir. EGFR R252C, afatinibe özellikle hassas tümörler yaratıyor gibi görünüyor. Bu sonuca şu anda tek bir ayrıntılı hasta vakası ve kapsamlı laboratuvar çalışmaları dayanıyor olsa da, EGFR’nin dış domain mutasyonlarının daha kişiselleştirilmiş testine işaret ediyor ve dikkatle seçilmiş hedefe yönelik tedavilerin zor tedavi edilen beyin ve akciğer tümörü olan seçkin hastalara yeni umutlar sunabileceğini öne sürüyor.
Atıf: Zhang, Y., Fei, Q., Li, Y. et al. An alternative EGFR activation by patient-derived R252C mutation promotes cancer progression. Nat Commun 17, 1902 (2026). https://doi.org/10.1038/s41467-026-68699-4
Anahtar kelimeler: EGFR mutasyonu, gliom, akciğer kanseri, ERK sinyallemesi, afatinib