Clear Sky Science · tr
β-Arrestin 1 ile Gαs veya Gαi1 arasındaki etkileşimlere ilişkin işlevsel ve yapısal bulgular
Sağlık ve tıp açısından önemi
Günümüz ilaçlarının çoğu—alerji haplarından kalp ilaçlarına ve psikiyatrik tedavilere kadar—hücere yüzeyindeki geniş bir protein ailesi olan G proteini–bağlı reseptörleri (GPCR’ler) hedef alır. Bu reseptörler hücreye mesaj iletmek için iki temel yardımcı kullanır: G proteinleri ve beta-arrestin adı verilen proteinler. Bu çalışma, bir beta-arrestin (beta-arrestin 1)’in hücre içinde iki tip G proteiniyle nasıl doğrudan etkileştiğini inceliyor. Bu gizli konuşmanın anlaşılması, sinyallerin hücre içinde akışını ince ayarlayarak daha hedefe yönelik ve yan etkileri daha az olan ilaçların tasarlanmasına yardımcı olabilir.
Hücre içindeki iki ana haberci
Bir hormon veya ilaç hücre yüzeyindeki bir GPCR’ye bağlandığında, iki geniş iletişim yolu tetiklenir. Bir yol G proteinlerini kullanır; bu G proteinleri bir küçük kimyasalı (GDP) başka bir kimyasalla (GTP) değiştirerek moleküler zamanlayıcılar gibi açılıp kapanırlar. Diğer yol ise beta-arrestinleri kullanır; beta-arrestinler hem G protein sinyalini kapatabilir hem de kendi sinyal yollarını başlatabilir. Uzun süre boyunca bilim insanları reseptörlerin G proteinlerle ya da beta-arrestinlerle ayrı ayrı nasıl konuştuğunu inceledi. Daha yakın tarihte yapılan çalışmalar, G proteinleri ve beta-arrestinlerin birbirine bağlanabileceğini veya reseptörle birlikte büyük “mega-kompleksler” oluşturabileceğini düşündürdü. Ancak bu proteinlerin nasıl bağlandığı ve bunun sinyal iletimi açısından ne anlama geldiği belirsizdi.
Kim kime bağlanıyor ölçmek
Bu çalışmada araştırıcılar beta-arrestin 1 ve iki G proteini “alfa” alt birimine odaklandı: genellikle hücresel aktiviteyi uyaran Gαs ve genel olarak aktiviteyi azaltan Gαi1. Hassas bir bağlanma tekniği kullanarak, saflaştırılmış beta-arrestin 1 ile her bir G proteininin farklı koşullar altında ne kadar güçlü şekilde bir arada kaldığını test ettiler. Anahtar faktörün G proteininin “açık” veya “kapalı” olması değil, beta-arrestin 1’in daha aktif, esnek bir biçimde olup olmadığı olduğu bulundu. Kuyruğu eksik bir beta-arrestin 1 versiyonu—gevşek, aktif bir şekiller topluluğu gibi davranan—hem Gαs hem de Gαi1’e güçlü şekilde bağlandı. Buna karşılık, dinlenme halindeki beta-arrestin 1 veya reseptör-kuyruğu benzeri bir peptitle kilitlenmiş biçimi zayıf ya da hiç bağlanmadı. Bu, G proteinlerinin reseptör aktivasyonunu takiben ortaya çıkabilecek aktif-benzeri şekilleri örnekleyen beta-arrestin 1’i tercih ettiğini düşündürür. 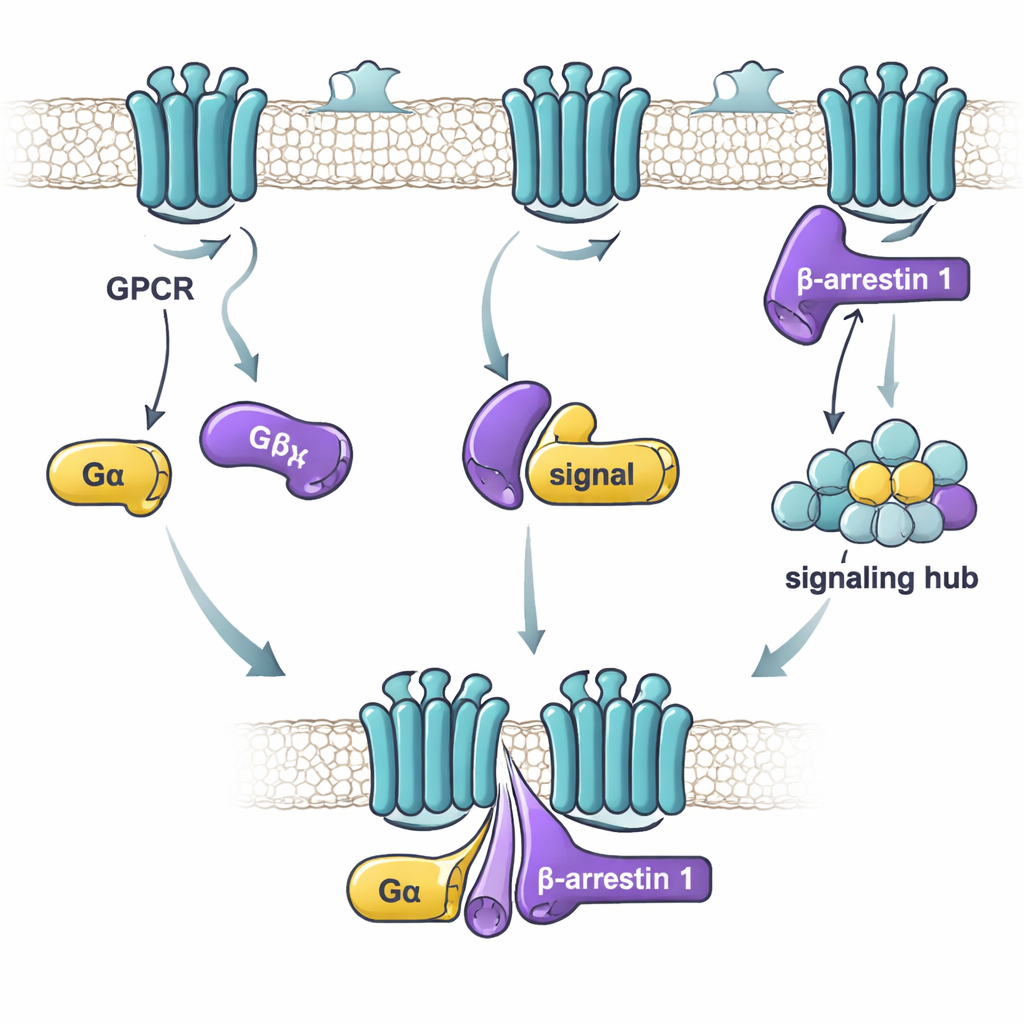
İnce şekil değişikliklerini izlemek
Bağlanmanın protein şeklini nasıl etkilediğini görmek için ekip, protein omurgasındaki hidrojen atomlarının çözücünün ağır hidrojenine ne kadar hızlı değiştiğini izleyen bir yöntem kullandı. Daha yavaş değişim genellikle bir bölgenin daha korunaklı ya da sertleşmiş olduğunu; daha hızlı değişim ise daha esnek veya açığa çıkmış olduğunu gösterir. Aktif-benzeri beta-arrestin 1 fragmanı Gαs veya Gαi1’e bağlandığında, her iki G proteini de birkaç bölgede belirgin desen değişiklikleri gösterdi; bu, kompleks etrafında yeniden şekillendiklerini işaret eder. Buna karşılık beta-arrestin 1’deki değişiklikler yalnızca hafifti ve esas olarak esnek döngülerdeydi. G proteinlerinin izole edilmiş domainleriyle çalışarak, araştırıcılar hem ana katalitik “Ras-benzeri” kısmın hem de çevresindeki alfa-helikal bölümün bağlanmaya katkıda bulunduğunu gösterdiler. Gαs için helikal bölge özellikle güçlü bir rol oynarken; Gαi1 için her iki bölge yaklaşık olarak eşit derecede önem taşıyor gibi görünüyordu.
Ana anahtarı çevirtmeden işlev
Sıradaki soru bu doğrudan temasın G proteinlerin açılma biçimini değiştirip değiştirmediğiydi. Ekip, bir G proteinin GDP’den GTP’ye geçiş yaptığında ışık yayan floresanlı bir GTP taklidi probu kullandı; bu, aktivasyonun standart bir ölçüsüdür. İlginç bir şekilde, beta-arrestin 1 eklenmesi ne Gαs ne de Gαi1 için bu nükleotid değişiminin hızını veya derecesini değiştirdi. Başka bir deyişle, beta-arrestin 1 G proteinler için klasik bir “açma-kapama” enzimi gibi davranmıyor. Bunun yerine etkisi kendi yapısında ortaya çıkıyor. Kuyruk hareketi floresansla izlenebilen zeki tasarlanmış bir beta-arrestin 1 kullanarak, reseptörden türetilmiş bir peptit varlığında aktif Gαs’in, ancak Gαi1’in değil, beta-arrestin’in C-terminal kuyruğunun salınımını hızlandırdığını buldular. Canlı hücrelerde ek görüntüleme ve enerji aktarım sensörleri, hormon uyarımıyla Gαs ile beta-arrestin 1’in birbirine yaklaştığını ve Gαs’in beta-arrestin 1’i daha aktif bir konformasyona itmeye yardımcı olduğunu doğruladı. 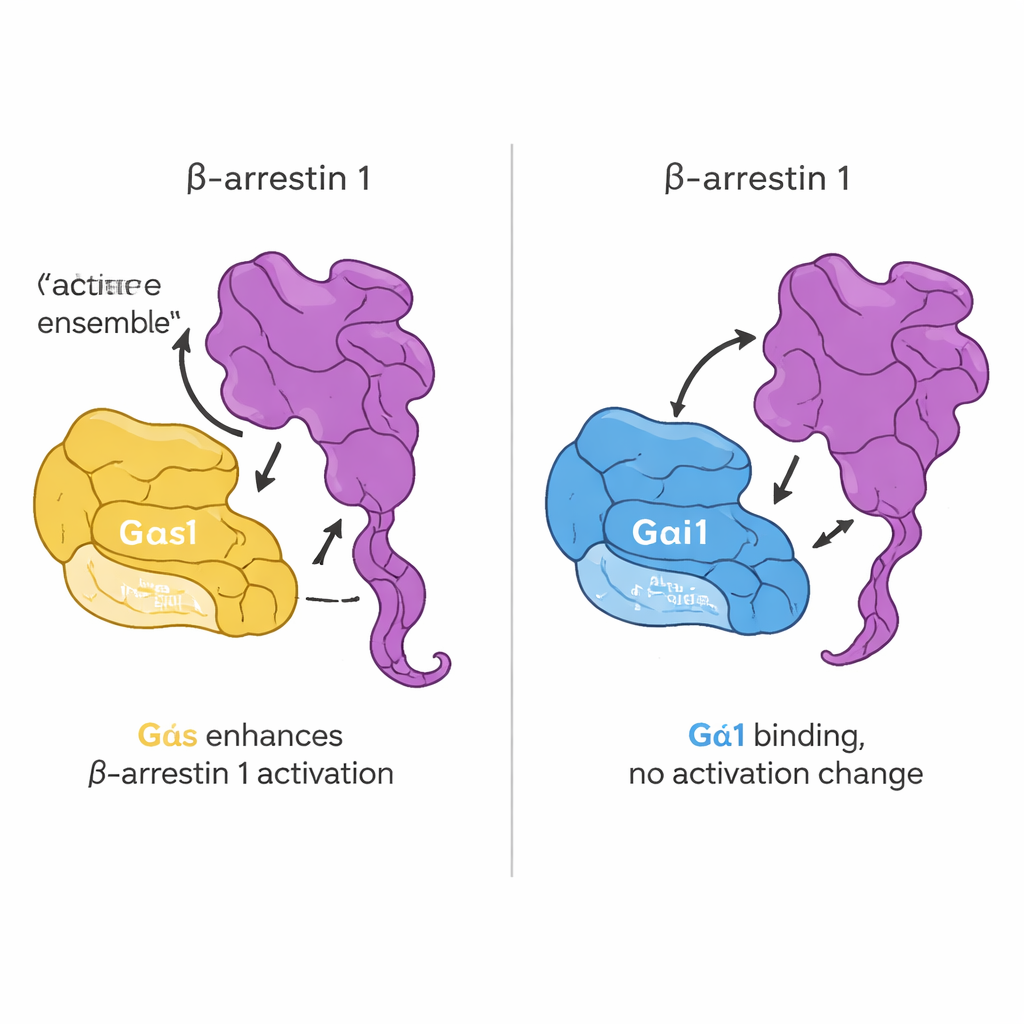
Hücre sinyalinde yeni bir kontrol katmanı
Bu sonuçları bir araya getirdiğimizde, çalışma Gαs ve Gαi1’in beta-arrestin 1’e doğrudan bağlandığını, ancak bunun hafifçe farklı yollarla ve farklı sonuçlarla gerçekleştiğini öne sürüyor. Hiçbir G proteininin ana “açma/kapama” davranışı bu temastan etkilenmiyor. Bunun yerine özellikle Gαs için etkileşim, beta-arrestin 1 üzerinde bir ince ayar düğmesi gibi davranıyor; onu daha aktif, kuyruk-salınımı olan bir forma itiyor veya stabilize ediyor. Bu, GPCR sinyal iletimine daha önce yeterince değer verilmeyen yeni bir katman ekliyor: reseptörler G proteinleri ve beta-arrestinleri koordine edebilirken, G proteinleri ve beta-arrestinler de birbirlerini doğrudan karşılıklı olarak modüle edebiliyor. Uzun vadede, bu ince etkileşimlerin haritalanması, ilaç tasarımcılarının faydalı yolları güçlendirip yan etkilere yol açan yolları atlamasına yardım edebilir.
Atıf: Duan, L., Kim, H., Suh, Y. et al. Functional and structural insights into interactions between β-Arrestin 1 and Gαs or Gαi1. Nat Commun 17, 1879 (2026). https://doi.org/10.1038/s41467-026-68690-z
Anahtar kelimeler: G proteini-kaplı reseptörler, beta-arrestin, G protein sinyalleşmesi, hücre sinyal mekanizmaları, yapısal biyoloji