Clear Sky Science · tr
Epigenom çapında analiz, çocukluk çağı kanseri sağ kalanlarında tedavi kaynaklı kardiyometabolik risklerin DNA metilasyonu aracılıklarını belirliyor
Neden kanserin etkileri vücutta uzun süre kalır
Daha iyi tedaviler sayesinde, kanserli çocukların çoğu artık yetişkinliğe ulaşıyor. Ancak bu sağ kalanların birçoğu on yıllar sonra obezite, yüksek tansiyon ve diyabet benzeri durumlar dahil yeni sağlık sorunlarıyla karşılaşıyor. Bu çalışma önemli bir soruyu soruyor: çocuklukta verilen tedaviler kalp ve metabolizma üzerinde nasıl bu kadar kalıcı gölgeler bırakıyor? Kan hücrelerindeki DNA üzerindeki kimyasal işaretlere bakarak, araştırmacılar geçmiş kemoterapi ve radyasyonun uzun vadede kardiyometabolik riski artıracak şekilde vücudu “yeniden programlayabileceğine” dair ipuçları ortaya koyuyor.
Büyümüş çocukluk çağı sağ kalanlarında gizli riskleri izlemek
Araştırma ekibi, uzun dönem St. Jude Yaşam Boyu Kohortu’nda izlenen yaklaşık 3.000 yetişkin çocukluk çağı kanseri sağ kalanını inceledi. Bu sağ kalanlar çocukken çeşitli kemoterapiler ve beyin ya da gövdeye (göğüs, karın, pelvis) yönelik radyasyon almış, sonra yıllar sonra ayrıntılı sağlık kontrolleri ve kan testleri için geri dönmüştü. Bilim insanları, kalp hastalığı ve erken ölüm riskini artırdığı bilinen beş ana kardiyometabolik soruna odaklandı: obezite, anormal kan şekeri, yüksek trigliseridler, yüksek kolesterol ve yüksek tansiyon. Bu koşullara sahip olanlarla olmayanları karşılaştırarak, genoma yayılmış milyonlarca noktada DNA metilasyonunda—genlerin açılıp kapanmasını kontrol etmeye yardımcı olan küçük kimyasal anahtarlar—fark aradılar.
Tedavinin bir hatırası olarak DNA üzerindeki kimyasal işaretler
Genom genelinde, araştırmacılar metilasyon seviyelerinin en az bir kardiyometabolik durumla ilişkili olduğu yaklaşık 1.900 DNA bölgesi buldu. Bu bölgelerin çoğu tek bir sorunla bağlantılıydı, ancak küçük bir grup birkaç sorunla bağlantılı “merkez” gibi görünüyordu. CPT1A ve LMNA adındaki iki genden yakınında bulunan beş ana bölge tüm beş kardiyometabolik riskle aynı anda ilişkilendirildi. Bu genlerin vücudun yağları nasıl işlediği ve hücrelerin yapısını nasıl koruduğu üzerinde etkisi olduğu biliniyor; bu da tedavinin ortak metabolik ve kardiyovasküler yolları bozabileceğine işaret ediyor. Metilasyon değişikliklerinin birçoğu, özellikle iltihapla ilişkili olanlar, genel popülasyonda daha önce görülen sinyallerle örtüşüyordu; ancak bazıları kanser sağ kalanlarına özgü görünerek tedavinin kendine has biyolojik bir iz bıraktığını düşündürüyor.
Tedavi, DNA değişiklikleri ve hastalık arasında bağlantı kurmak
Sıradaki adım, bu metilasyon değişikliklerinin yalnızca eşlik eden işaretler olmaktan öte, tedavinin daha sonra hastalığa yol açma mekanizmasını gerçekten açıklayıp açıklamadığını test etmekti. Araştırmacılar kan örneği alındıktan sonra yeni gelişen veya kötüleşen kardiyometabolik sorunlara odaklandı; böylece tedaviden DNA değişikliğine, oradan da hastalığa giden zaman çizgisi korunmuş oldu. İstatistiksel aracılık analizleri kullanarak, belirli tedaviler ile sonraki kardiyometabolik sorunlar arasındaki bağlantının birlikte yaklaşık dörtte birine kadarını açıkladığı görülen 24 metilasyon bölgesi tespit ettiler. Beyin ve gövdeye yönelik radyasyon özellikle güçlü desenler gösterdi: metilasyon bölgeleri grupları, bu radyoterapilerin anormal kan şekerine etkisinin yaklaşık %10–20’sini oluşturdu. Özellikle öne çıkan bir bölge, ANTXR2 adlı bir gene yakın olan bölgeydi; buranın gövde radyasyonunun sonraki glukoz sorunları üzerindeki etkisinin yaklaşık %20’sini aracılaştırdığı görüldü.
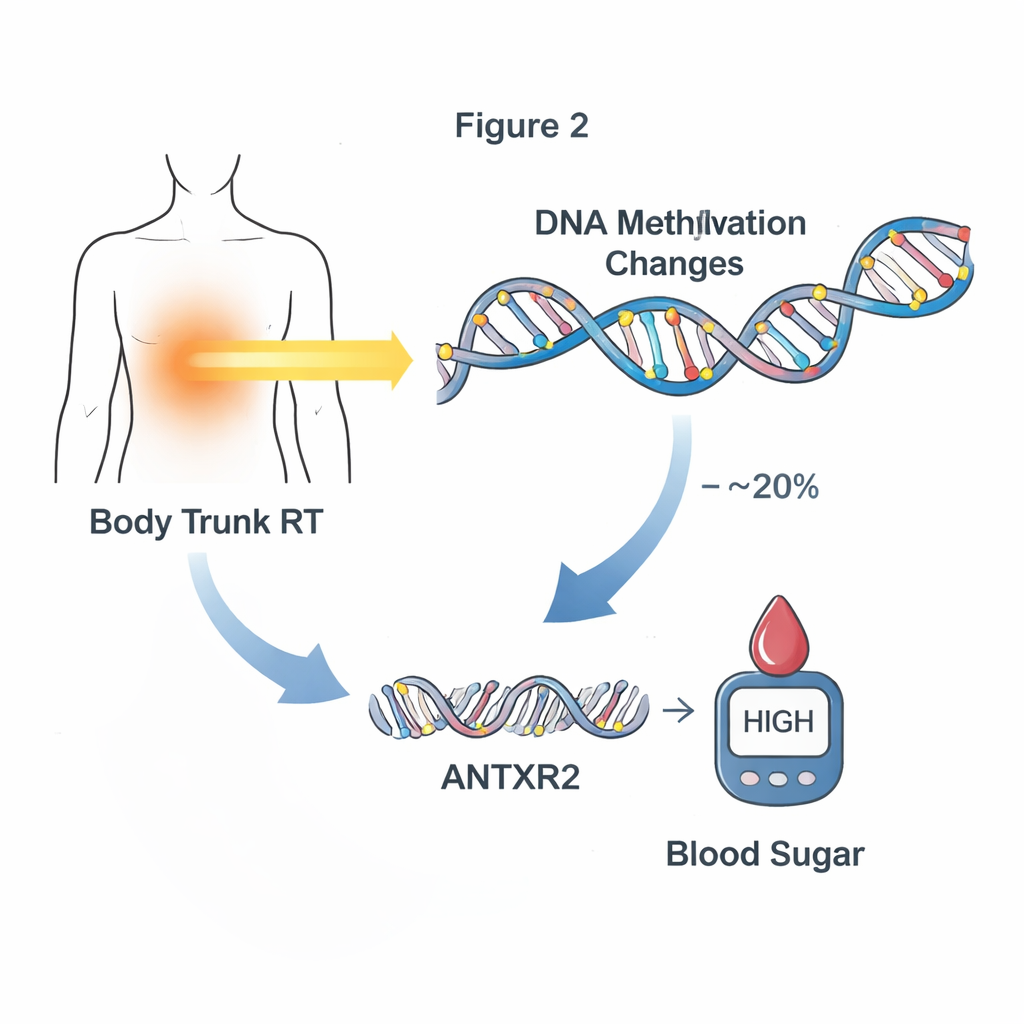
DNA işaretlerinden gen aktivitesine
Bu metilasyon işaretlerinin biyolojiyi nasıl değiştirebileceğini anlamak için ekip, kanlarından hem DNA hem RNA verisi bulunan bir alt grupta gen aktivitesini inceledi. Daha yüksek ya da daha düşük metilasyonun yakınlardaki gen ekspresyonundaki değişikliklerle ilişkili olduğu onlarca metilasyon bölgesi buldular. Bunlar arasında gövde radyasyonunu almış sağ kalanlarda özellikle güçlü bağlantı gösteren ANTXR2 yakınındaki ana aracılık bölgesi de vardı; bu bölgede metilasyon seviyeleri bu genin ne kadar ifade edildiğiyle yakından ilişkiliydi. ANTXR2, kan damarlarını ve çevresindeki doku çerçevesini düzenlemeye yardımcı olur—bunlar glukoz ve insülinin vücutta nasıl hareket ettiğini etkileyen sistemlerdir. Bu desen, radyasyonun metilasyonu değiştirdiği, metilasyonun gen aktivitesini kaydırdığı ve bunun da vücudu anormal kan şekerine doğru itebilecek bir olay zincirini gösteriyor olabilir.
Sağ kalanlar ve gelecekteki bakım için anlamı
Uzman olmayanlar için ana mesaj şudur: çocukluk çağı kanseri tedavileri sadece anlık doku hasarına yol açmaz; on yıllar boyunca sağlığı şekillendiren DNA üzerinde kalıcı “notlar” bırakabilir. Bu çalışmada, bu notların bazıları—DNA metilasyon değişiklikleri—neden belirli sağ kalanların obezite, kandaki yüksek yağlar veya diyabet ve kalp hastalığıyla ilişkili glukoz sorunları geliştirmeye daha yatkın olduğunu açıklamaya yardımcı oluyor. Bu kimyasal işaretler hikayenin yalnızca bir parçası olsa da, sonunda en yüksek riskteki sağ kalanları belirlemek için kan temelli biyobelirteçler olarak kullanılabilir ve yaşam tarzı değişikliklerinin veya yeni tedavilerin bu epigenetik geçmişin bazı bölümlerini güvenli biçimde yeniden yazıp yazamayacağını test etmek için yol gösterebilir. Bu çalışma, yaşam boyu bakımını, geçmiş tedavinin moleküler ayak izlerini kullanarak kalp ve metabolik hastalıkların daha erken ve daha hedefe yönelik önlenmesine doğru bir adım daha yaklaştırıyor.
Atıf: Eulalio, T., Kim, Y., Meng, X. et al. Epigenome-wide analysis identifies DNA methylation mediators of treatment-related cardiometabolic risk in survivors of childhood cancer. Nat Commun 17, 1979 (2026). https://doi.org/10.1038/s41467-026-68689-6
Anahtar kelimeler: çocukluk çağı kanseri sağ kalanları, DNA metilasyonu, kardiyometabolik risk, radyasyon tedavisi, epigenetik