Clear Sky Science · tr
Şaperon fabrikalarında kuaterner yapıların ortak-translasyonla belirlenmesi
Hücre içi “montaj hatları” büyük makineleri nasıl düzgün tutuyor
Hücrelerimizin her birinde, DNA’yı kopyalayan motorlardan diğer RNA’ları üreten fabrikalara kadar, binlerce protein parçası karmaşık moleküler makineler halinde bir araya gelmek zorundadır. Bu çalışma, görünüşte basit ama sonuçları büyük olan bir soruyu soruyor: hücreler, her yeni parça yapılırken hangi yardımcı proteinlerin ona eşlik edeceğine anlık olarak nasıl karar veriyor ve bu süreci hücrenin kaotik sıvısı içinde nasıl düzenli tutuyor?
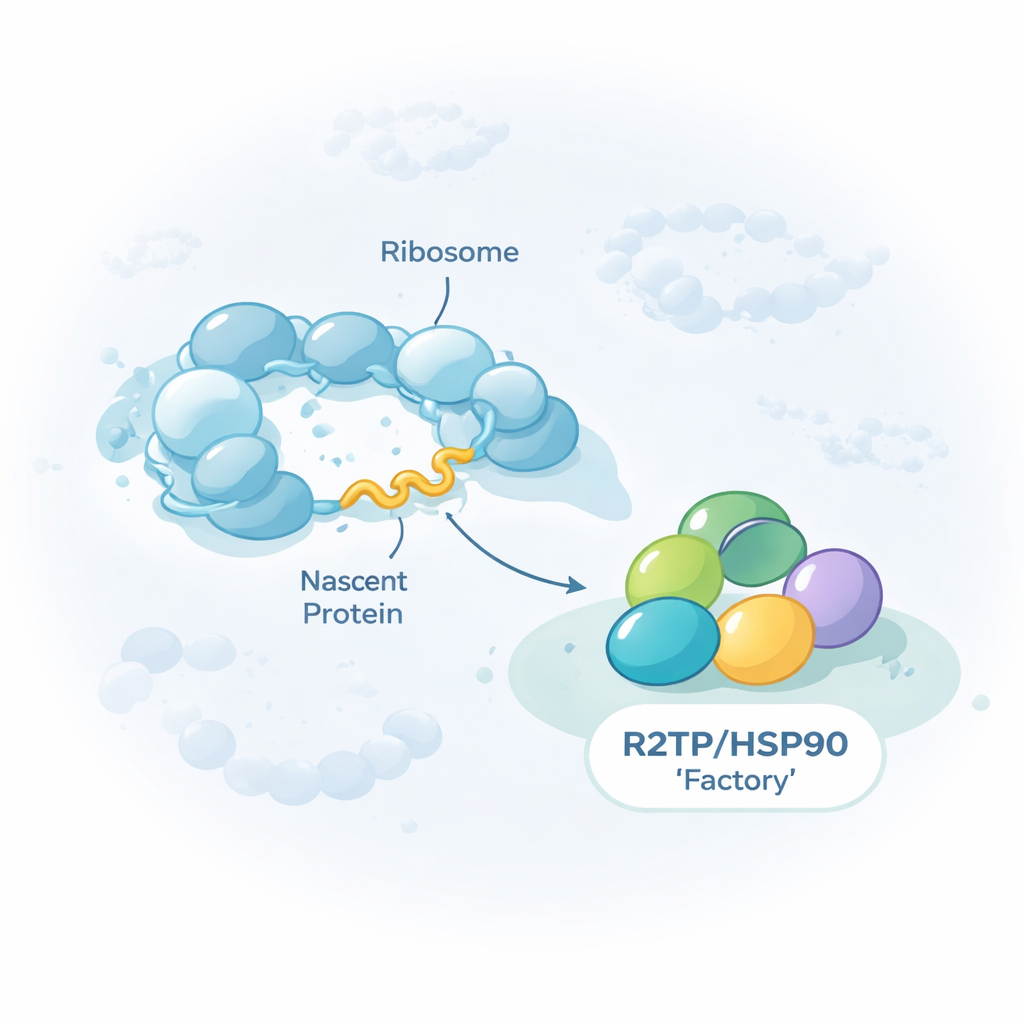
Hücresel mega-makineler için genel amaçlı bir yardımcı
Çalışma, HSP90/R2TP olarak bilinen bir grup yardımcı protein yani şaperona odaklanıyor. Tek bir proteini katlayıp tamamlamaktan ziyade, bu şaperon dev çok parçalı komplekslerin montajında uzmanlaşmıştır; bunlar arasında DNA’yı RNA’ya çeviren üç nükleer RNA polimeraz, belirli RNA–protein partikülleri ve DNA paketlemesini yeniden şekillendiren büyük yeniden modelleme makineleri bulunur. Yazarlar, R2TP’nin bu istemci proteinlerle sadece iş bittikten sonra karşılaşmadığını gösteriyor. Bunun yerine R2TP sıklıkla, her istemci daha yapılırken yani ribozomlarda sentezlenirken bağlanıyor. İnsan hücrelerinden R2TP’yi çektirip onunla gelen RNA’ları dizilediklerinde, çevirileri sırasında R2TP tarafından temas edilen yaklaşık 150 haberci RNA (mRNA) buldular.
Uzayan protein zincirleriyle beraber yol alan yardımcılar
Bu bağlanmanın gerçekten protein sentezi sırasında olup olmadığını test etmek için ekip, translasyonu donduran veya bozan ilaçlar kullandı. Uzayan protein zincirlerini ribozomlardan koparan bileşikler uygulandığında, haberci RNA’ların çoğu R2TP’nin tutuşundan kayboldu. Ancak ribozomları sadece durduran ve yeni sentezlenen zincirlerin bağlı kalmasına izin veren bir ilaç kullanıldığında, R2TP bağlanması arttı. Tasarlanmış raporör RNA’lar bunu doğruladı: eğer translasyon yapay olarak erken durdurulursa, şaperon artık mesaja bağlanmıyordu. Bu bulgular birlikte net bir etkileşim kuralına işaret ediyor: R2TP, istemcilerini esas olarak ribozomdan çıkan ortaya çıkan protein zinciri üzerinden tanıyor, RNA dizisi üzerinden değil.
Belirli mesajları kümeleyen şaperon yapılı “fabrikalar”
Gelişmiş tek-molekül görüntüleme yöntemleri kullanan yazarlar ardından şaşırtıcı bir keşif yaptılar. Birçok farklı istemci mesajının rastgele dağılmış olduğunu görmek yerine, bazı kilit mesajların—özellikle RNA polimeraz II’nin ana alt birimlerini ve PRPF8 adlı büyük bir splicing faktörünü kodlayanlar—genellikle sitoplazmada parlak odaklar halinde toplandığını gözlemlediler. Bu odaklar R2TP ve onun ortağı HSP90 bakımından, ayrıca ribozomal bileşenler ve yapım halinde olan proteinler bakımından zenginleşmişti; bu da bunların aktif translasyon bölgeleri olduğunu gösteriyordu. Translasyon veya R2TP/HSP90’un ATPaz aktivitesi engellendiğinde, bu odaklar çözüldü. Yazarlar bu yapılara “R2TP fabrikaları” adını veriyor: seçilmiş haberci RNA’ların ve şaperonların yoğunlaştığı, ortaya çıkan protein zincirleri ile montaj yardımcıları arasında zamanında ve koruyucu temasları desteklemeye yönelik özelleşmiş yoğunlaşmalar.
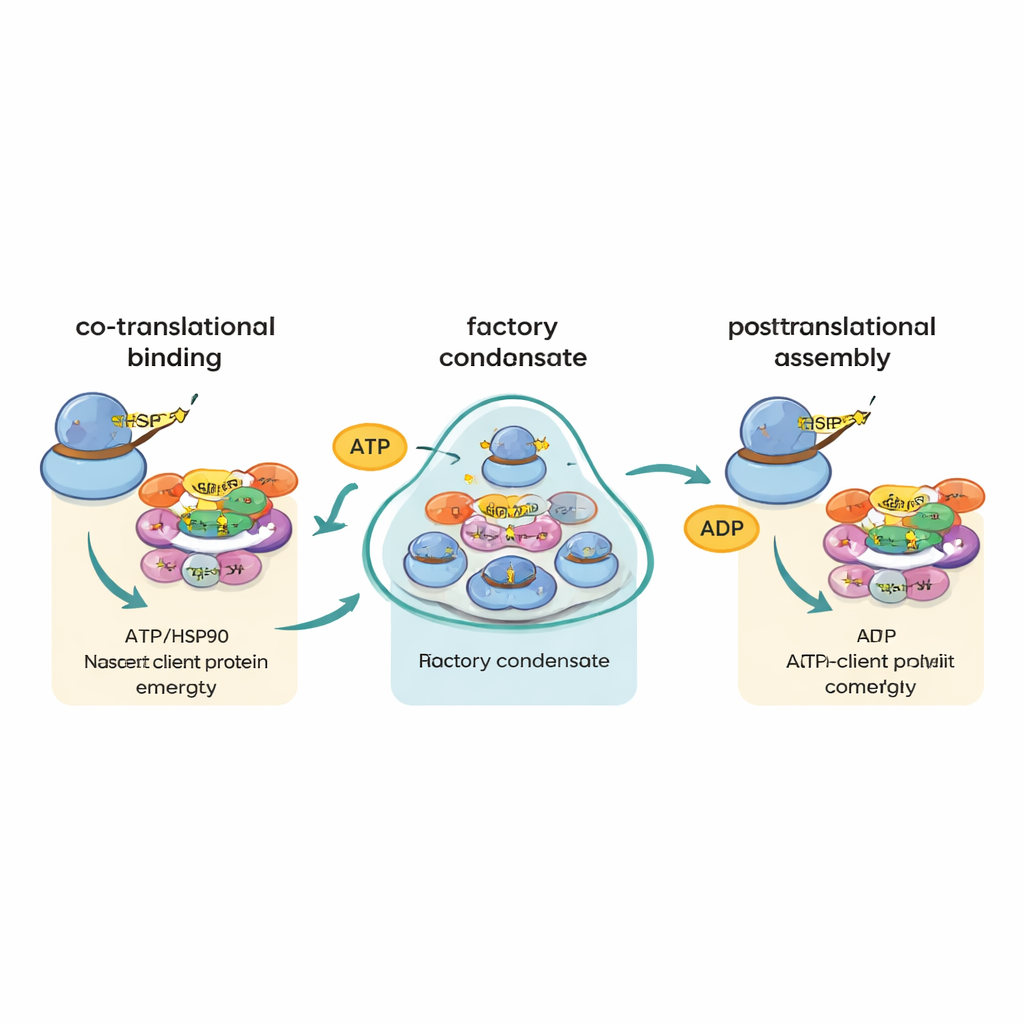
Planlarına uymadan parçaları yönlendirmek
Daha önce öne sürülen bir fikir, aynı kompleksin farklı parçalarını kodlayan mesajların birbirini bulup yan yana çevrilebileceği, böylece protein ürünlerinin hemen bir araya gelebileceğiydi. Yeni çalışma bu “bir arada konumlanmış planaş” modelini büyük ölçüde eliyor. Aynı makinede birleştiği bilinen protein çiftleri için bile, onların haberci RNA’ları nadiren birlikte görüldü. Bunun yerine veriler yazarların “ortak-translasyonel şaperon kanallama” veya kısaca “cha-cha” olarak adlandırdığı farklı bir stratejiyi destekliyor. Bu şemada, her büyük veya montaja eğilimli protein ribozomdan çıkmaya başladıkça R2TP ve HSP90 ona tutunup kaderini belirliyor ve onu montajın sonraki adımlarına yönlendiriyor. Fabrikalar kendileri esasen eşleşen mesajları bir araya getirmiyor; daha çok savunmasız yeni proteinlerin doğru şaperonla çabucak buluşma olasılığını artırıyorlar.
Bu gizli organizasyonun sağlık ve hastalık açısından önemi
R2TP ve HSP90’un kırılgan protein parçalarını korumakla kalmayıp ayrıca bunların nerede ve nasıl tercüme edildiğini şekillendirdiğini ortaya koyarak, bu çalışma hücre içi organizasyonun beklenmedik bir katmanını açığa çıkarıyor. Cha-cha mekanizması, parçaların mesajlarının nadiren aynı adrese sahip olmasına rağmen hücrelerin nasıl güvenilir şekilde devasa moleküler kompleksler inşa ettiğini açıklamaya yardımcı oluyor. Ayrıca şaperonlar veya onların enerji döngülerindeki kusurların RNA polimeraz ve splicing faktörleri gibi hayati makineleri destabilize edebileceğini; bunun da gelişimsel bozukluklardan kansere kadar değişen sonuçlara yol açabileceğini gösteriyor. Özetle çalışma, hücrelerin taze yapılmış parçaları doğru montajlara yönlendirmek ve iç makinelerini verimli ve düzenli tutmak için dinamik şaperon “fabrikalarına” güvendiğini ortaya koyuyor.
Atıf: Philippe, M., Salloum, S., Slimani, F. et al. Co-translational determination of quaternary structures in chaperone factories. Nat Commun 17, 1978 (2026). https://doi.org/10.1038/s41467-026-68687-8
Anahtar kelimeler: protein şaperonları, ortak-translasyonel montaj, moleküler makineler, RNA polimeraz, hücresel kalite kontrolü