Clear Sky Science · tr
AP-4’ün dinamik konformasyonlarının yapısal temeli ve ARF1 ile ilişkisi
Hücreler yüklerini nasıl sınıflandırır ve gönderir
Her hücre, binlerce protein “paketini” doğru hedeflere sürekli olarak sınıflandırıp gönderen hareketli bir depo gibidir. Bu teslimat sistemi sinir hücrelerinde bozulduğunda, sonuç ciddi beyin ve hareket bozuklukları olabilir. Bu çalışma, AP-4 adı verilen temel bir gönderim makinesinin nasıl şekil değiştirdiğini, regülatör bir protein olan ARF1 ile nasıl işbirliği yaptığını, yükleri küçük taşıma keseciklerine nasıl yüklediğini ve esnekliğinin sağlıklı nöronlar için neden bu kadar önemli olduğunu ortaya koyuyor.
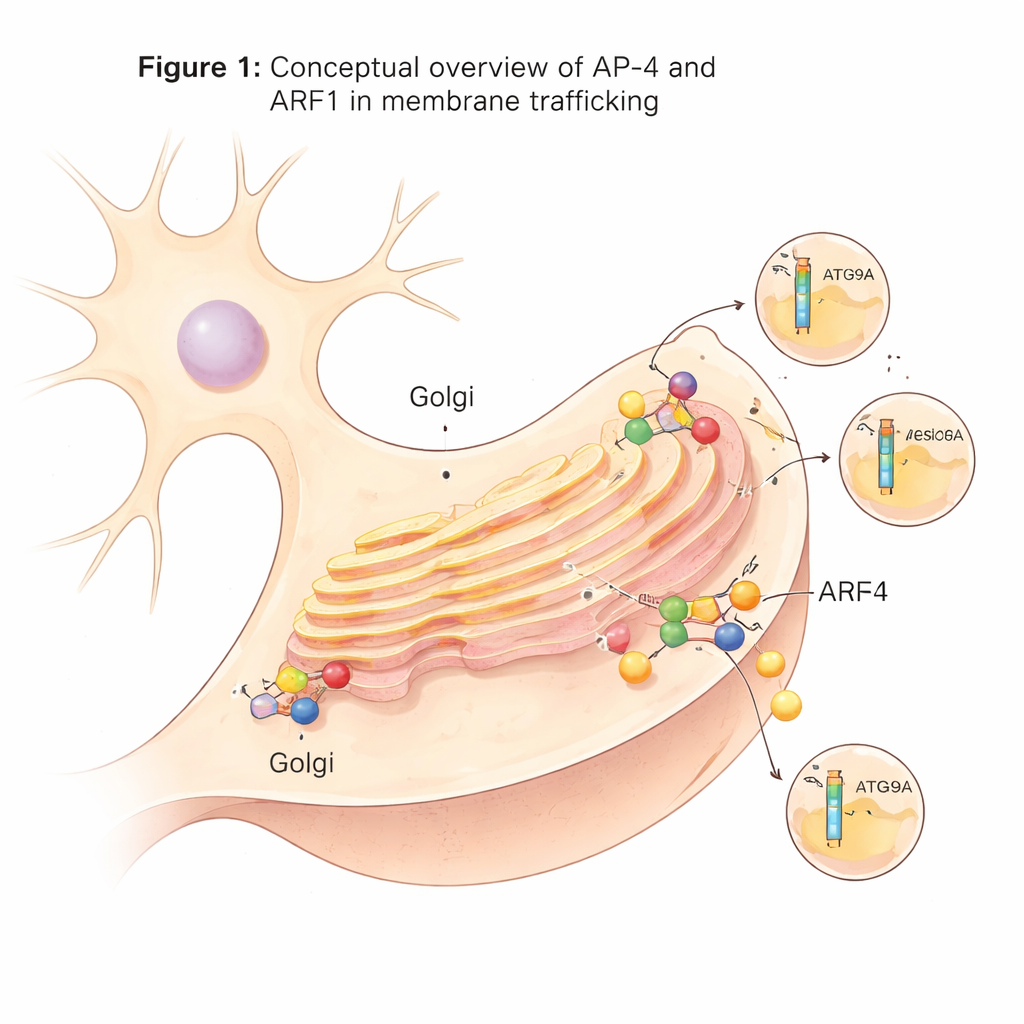
Sinir hücrelerinde özelleşmiş bir gönderim makinesi
Hücre içinde birçok taşıma vezikülü, trans-Golgi ağı olarak bilinen merkezi bir sınıflama istasyonundan tomurcuklanır. Bu veziküller, yük proteinlerini tanıyan ve etraflarına kaplı veziküller oluşmasına yardımcı olan adaptör protein komplekslerine (AP kompleksleri) güvenir. AP-4 bu adaptörlerden biridir ve çoğundan farklı olarak yaygın iskelet proteini klatrin kullanmamasıyla ayırt edilir. AP-4 birçok dokuda üretilse de nöronlarda özellikle önemli bir rol oynar. İnsanlarda AP-4 eksik veya işlevsiz olduğunda, otofaji ile ilişkili ATG9A proteini ve bazı glutamat reseptörleri gibi kritik yüklerin doğru taşınamaması AP-4 yetmezliği sendromu olarak bilinen şiddetli bir nörogelişimsel duruma yol açar.
Dinamik haldeki bir şekil değiştirici kompleks
Yazarlar, büyük protein birleşimlerini görselleştirebilen güçlü bir görüntüleme yöntemi olan kriyo-elektron mikroskopisi kullanarak çözeltideki AP-4 “çekirdek” kompleksinin üç boyutlu yapısını belirlediler. AP-4, birlikte bir kap benzeri yapı oluşturan dört altbirimden meydana gelir. AP-4’ün tek bir sert şekilde durmadığını keşfettiler. Bunun yerine, bir altbirimin (orta altbirimin C-terminus domeni) kâsenin merkezine sokulduğu “kapalı” form ile bu parçanın dışa sallanıp yüksek esneklik kazandığı “açık” form arasında doğal olarak geçiş yaptığı görüldü. Tek moleküllü floresans deneyleri, bu altbirimin aslında kapalı, kısmen açık ve tamamen açık olmak üzere en az üç konumu örneklediğini gösterdi; bu da AP-4’ün membrana bağlanmadan önce bile doğuştan dinamik olduğunu ortaya koyuyor.
ARF1’in rolü: işe alan, anahtar değil
Birçok ilişkili adaptör kompleksi, ARF adı verilen küçük regülatör proteinlere bağlanarak inaktif halden aktif şekle geçer. AP-4 için bunun nasıl işlediğini görmek üzere araştırmacılar, membrana tutunan küçük GTP-bağlayıcı protein ARF1’e bağlı AP-4 yapılarını çözdüler. ARF1’in AP-4’ün N-terminusuna yakın büyük altbirimlerinden birine, diğer AP komplekslerine benzer şekilde bağlandığını buldular. İlginç biçimde, ARF1 bağlanması AP-4’te dramatik bir yapısal yeniden düzenlenme tetiklemedi. Kapalı ve açık şekiller hâlâ bir arada bulundu ve kompleksin genel mimarisi büyük ölçüde değişmedi. Biyokimyasal testler ARF1 ile AP-4 arasındaki belirli temas noktalarının membrana işe alım için elzem olduğunu doğruladı, ancak ARF1 tek başına AP-4’ü tek bir aktif duruma kilitlemiyor.
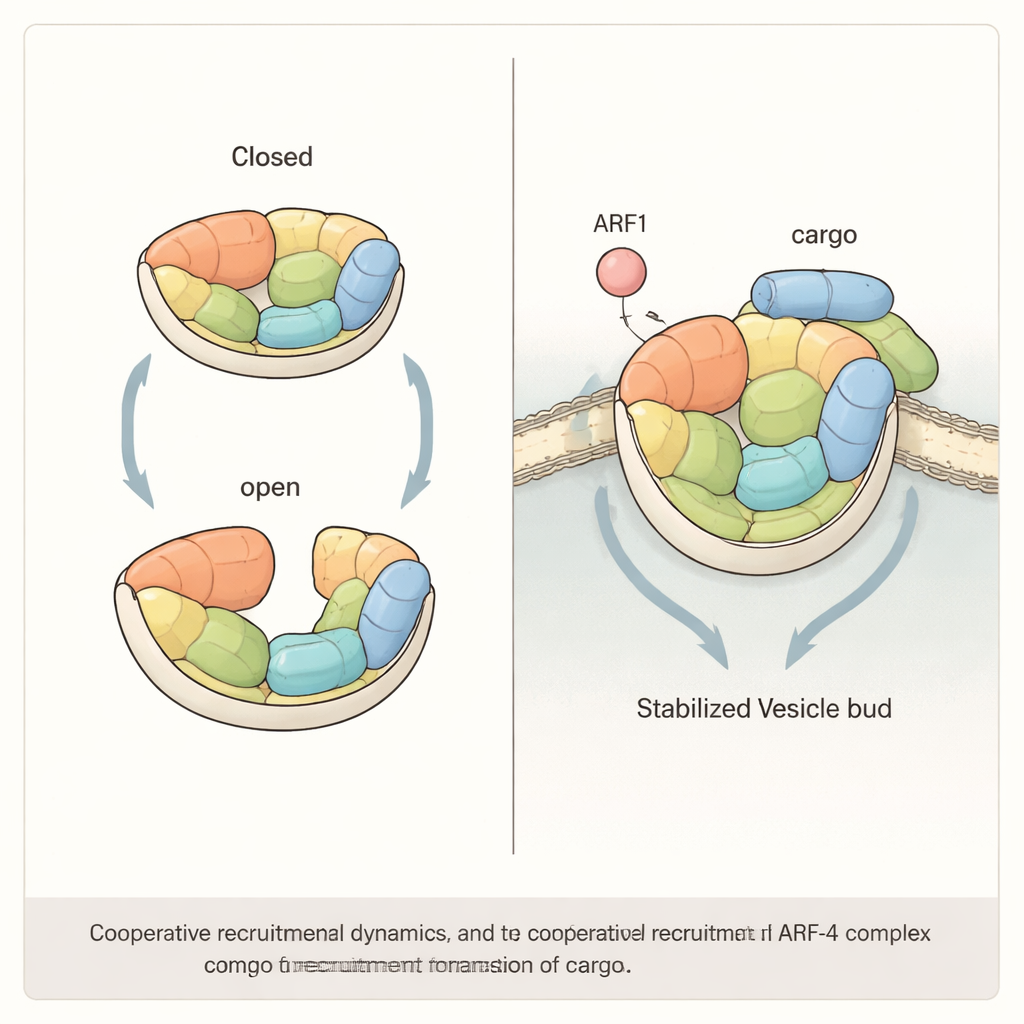
Regülatör ile yük arasında işbirliği
Çalışma ayrıca AP-4’ün membranlara etkin şekilde işe alınmasının muhtemelen ARF1 ile yük proteinlerinin kendileri arasındaki işbirliğine bağlı olduğunu gösteriyor. Sistemi yapay boncuklar ve lipozomlar üzerinde yeniden kurarak, yazarlar ARF1’in veya yük ATG9A’nın kısa bir kuyruğunun tek başına AP-4’ü çekebildiğini, ancak her ikisi birlikte bulunduğunda, bireysel etkilerinin toplamından beklenenden çok daha fazla AP-4 çektiklerini buldular. Araştırmacılar AP-4’ün yapısını sertleştiren—açık ve kapalı durumlar arasında hareket etme yeteneğini azaltan—mutasyonlar tasarladıklarında, bu sinerjistik etkinin kaybolduğu görüldü. Kritik bir AP-4 altbirimi eksik olan insan hücrelerinde, yalnızca böyle “sert” mutant versiyonları geri getirmek Golgi’den ATG9A’nın normal taşınmasını kurtarmaya yetmedi; bu da AP-4’ün esnekliğinin yalnızca bir merak değil, işlevsel bir gereklilik olduğunu vurguluyor.
Esnekliğin beyin sağlığı için önemi
Genel olarak bu çalışma, AP-4’ü çözeltide ve membranlarda birden çok konformasyonu örnekleyen şekil değiştiren bir adaptör olarak tasvir ediyor. ARF1, bir açma-kapama anahtarı olarak değil, membrana dayalı bir işe alımcı olarak görev yapıyor ve vezikül oluşumu için verimli konfigürasyonlarda AP-4’ü stabil hale getirmek üzere yük proteinleriyle birlikte çalışıyor. Bu dengenin bozulması—ARF1 veya yük bağlanmasının zayıflaması ya da AP-4’ün tek bir şekle donması—Golgi’den yük ihracatını bozarak nörogelişimsel hastalığa katkıda bulunabilir. AP-4’ün dinamik davranışının yapısal temelini ortaya koyarak, bu çalışma AP-4 ilişkili bozuklukları anlamak için bir çerçeve sunuyor ve etkilenen nöronlarda doğru taşımayı yeniden sağlama stratejilerine yönelik ipuçları veriyor.
Atıf: Wang, Y., Li, W., Qiu, Y. et al. Structural basis for the dynamic conformations of AP-4 and its association with ARF1. Nat Commun 17, 1897 (2026). https://doi.org/10.1038/s41467-026-68679-8
Anahtar kelimeler: hücre zarı taşıması, AP-4 adaptör kompleksi, ARF1, vezikül oluşumu, nörogelişimsel bozukluk