Clear Sky Science · tr
Sortilinin tiroglobulini moleküler tanıması
Tiroit Hücreleri Hormonu Ne Zaman Salacaklarına Nasıl Karar Veriyor
Tiroid hormonları metabolik “termostatımızı” ayarlamaya yardımcı olur; kalp atış hızından vücut sıcaklığına kadar birçok şeyi etkiler. Bu hormonlar, tiroglobulin adlı devasa bir protein içinde üretilir ve depolanır. Bu çalışma, başka bir protein olan sortilinin tiroit hücrelerinin hangi tiroglobulin formunu hücre içine geri çekip hormonun kana salınmasını sağlayacak şekilde seçmesine nasıl yardımcı olduğunu ortaya koyuyor—bu karar nihayetinde vücudumuzun gördüğü tiroid hormonu miktarını etkiliyor.
İşlenmeyi Bekleyen Bir Depolama Proteini
Tiroglobulin, tiroit hücreleri tarafından üretilen ve kolloid adı verilen jelimsi bir havuza salgılanan devasa, Y şeklinde bir proteindir. Orada hem hammadde hem de depo görevi görür: tiroglobulindeki belirli yapı taşları (amino asitler) iyot ile kimyasal olarak modifiye edilerek hâlâ daha büyük proteinin içinde bulunan tiroid hormonlarına dönüşür. Bu hormonları serbest bırakmak için tiroglobulinin tekrar hücre içine alınması, lizozom adı verilen geri dönüşüm bölmeleri içinde parçalanması ve hormon parçalarının kana taşınması gerekir.
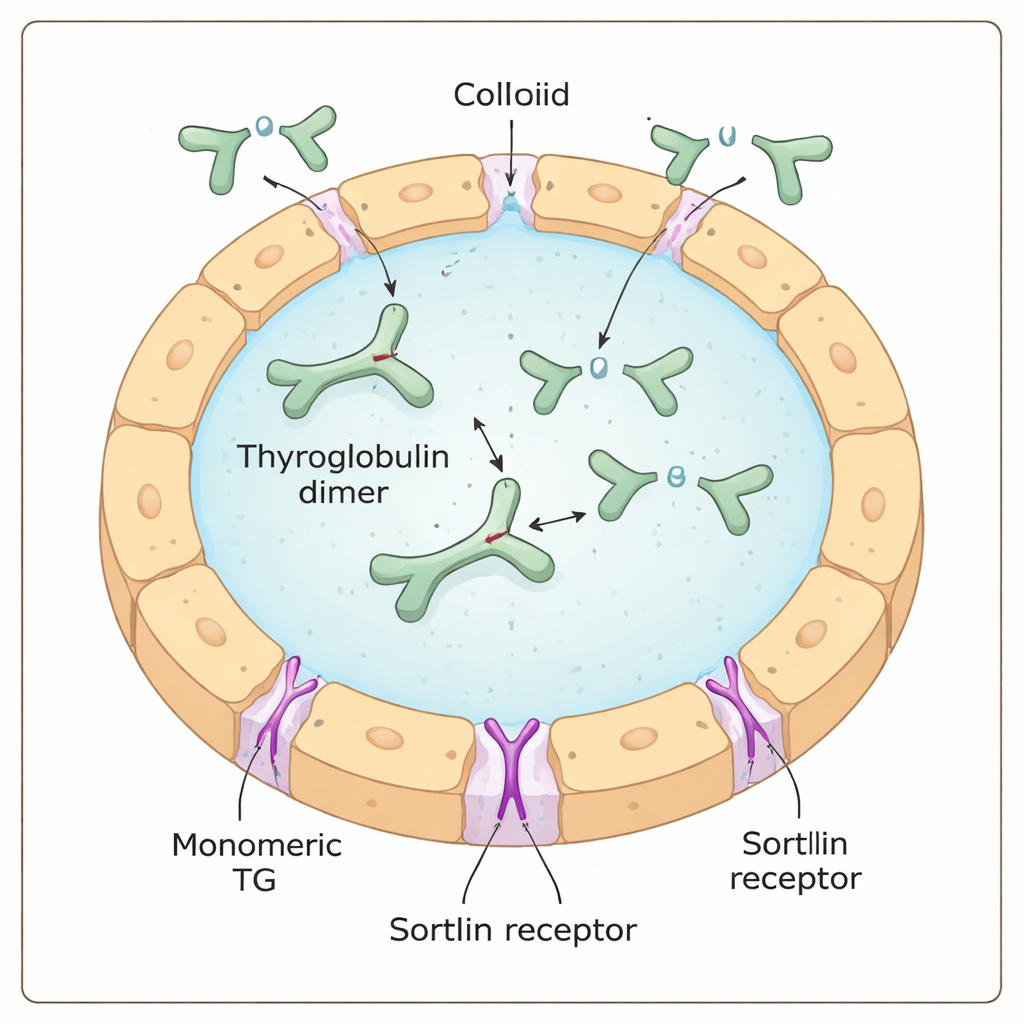
Gizli Bir Tercihe Sahip Hücresel Bir Kapı Bekçisi
Sortilin reseptörünün, tiroglobulini hücre yüzeyinde bağlayıp içeri yönlendiren “kapı bekçilerinden” biri olduğu öne sürülmüştü. Önceki çalışmalar sortilinin yüksek oranda iyotlanmış tiroglobulini tercih ettiğini göstererek reseptörün iyot içeriğini doğrudan algılayabileceğini düşündürmüştü. Yazarlar, biyokimyasal testler, tek molekül kütle ölçümleri ve hücre temelli alım deneylerinin birleşimini kullanarak bunun yerine sortilinin tiroglobulinin daha yaygın eşli (dimerik) formu yerine tek birimlik, yani monomerik formunu güçlü şekilde tercih ettiğini buldu. Bir örnekte daha fazla monomer bulundukça, sortilinle kompleks oluşturma ve tiroit hücreleri tarafından içeri alınma daha verimli oluyordu; bu, taşınan iyot miktarından bağımsızdı.
İletişim Noktasına Yakından Bakmak
Bu tercihi atomik düzeyde anlamak için ekip yüksek çözünürlüklü kriyo-elektron mikroskobu ve çapraz bağlama kütle spektrometrisine başvurdu. Bu yöntemler sortilinin monomerik tiroglobulinin C-terminusundaki (bir uçtaki) kısa, gevşek bir kuyruğu tanıdığını gösterdi. Bu kuyruk, on kanatlı bir pervane şeklindeki merkezi bir boşluğa doğru ilerleyip içerideki iki küçük “sıcak nokta”ya oturuyordu. Çarpıcı biçimde, dimerik tiroglobulinde bu kuyruğun çevresindeki bölgenin bir kısmı sortilinin erişemeyeceği şekilde gömülüydü; bu durum dimerin zayıf bir ortak olmasını açıklıyor. Veriler, tiroglobulinin dış ortamda doğal protein yıkımı yoluyla budanması veya gevşemesinin dimerleri sortilinin yakalayabileceği monomerlere dönüştürmeye yardımcı olduğunu öne sürüyor.
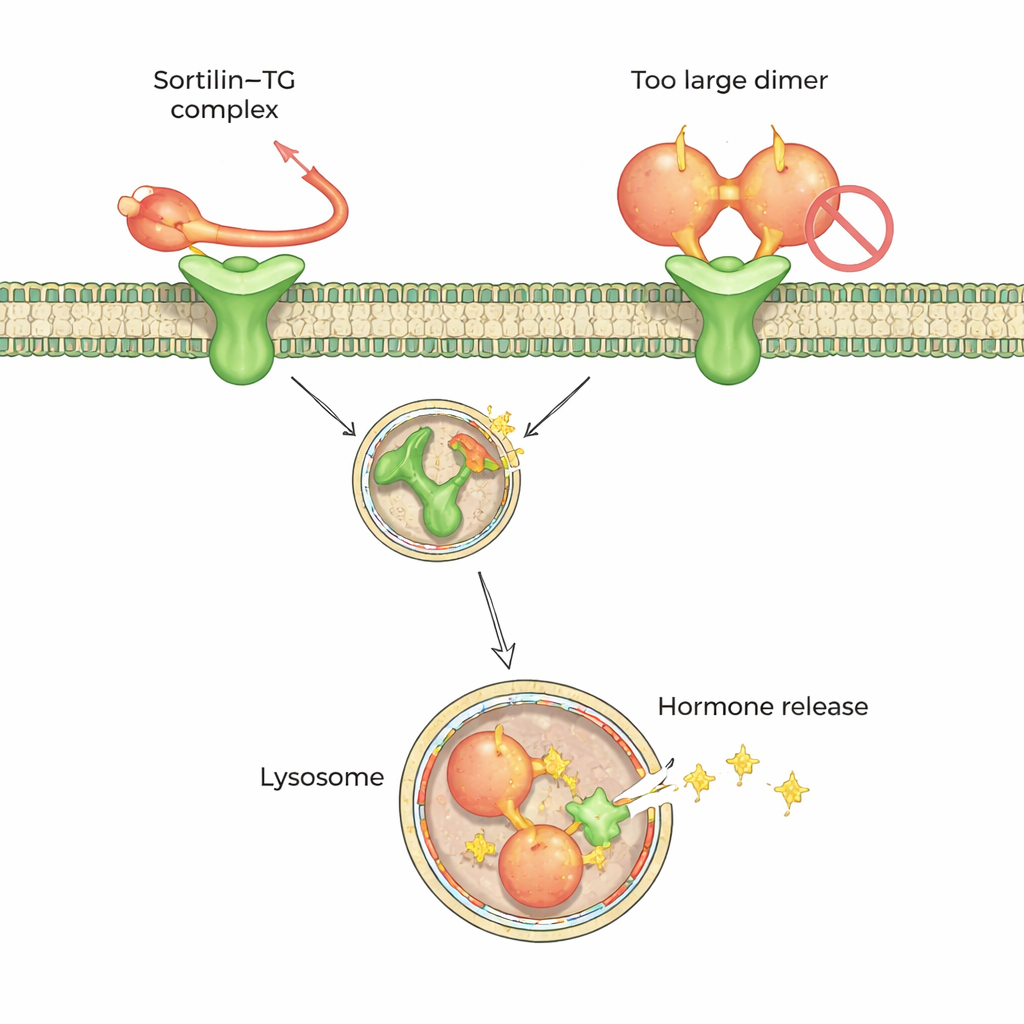
Birçok Yük Proteini İçin Paylaşılan Bir Bağlanma Kodu
Sortilin yalnızca tiroit proteini değildir; kalp hastalığı ve beyin bozukluklarıyla ilişkili faktörler de dâhil olmak üzere birçok farklı molekülün taşınmasına yardımcı olur. Yapısal çalışmalarını AlphaFold ve AlphaPulldown gibi gelişmiş yapı tahmin araçlarıyla birleştirerek araştırmacılar, bilinen düzine sortilin ortağının pervane boşluğuna nasıl bağlanabileceğini karşılaştırdılar. Tekrarlayan bir desen buldular: birçok yük, tiroglobulinin kuyruğuna benzeyen aynı cebe sığan yaklaşık yirmi amino asitten oluşan düzensiz bir peptid segmenti sunuyor; bu segment bazen bilinen bir beyin peptidi olan nörotensinle aynı yönde, bazen ise ters yönde ilerliyor. Ters yönde olsalar bile bu peptitler benzer özellikler paylaşıyor—bir ucunda asidik ya da negatif yüklü bir grup, diğer ucunda hacimli aromatik bir kalıntı ve arada esnek, sıklıkla prolince zengin bir bölüm.
İyotun Şekilden Daha Az Önemli Olmasının Nedeni
Sortilin ile tiroglobulin arasındaki ana temas bu esnek kuyruk olduğundan, yazarlar kuyruğun içindeki hormon oluşturan bir tirosinin ekstra iyotla dekore edilmesinin bağlanmayı değiştirip değiştirmeyeceğini test ettiler. Değiştirmedi: tam oluşmuş bir tiroid hormonu taşıyan sentetik bir peptit, modifiye edilmemiş versiyonla neredeyse aynı davranışı gösterdi. Modellemede iyotlanmış halka çözünürlük içine doğru çıkıyordu ve yeni sıkı temaslar oluşturmuyordu. Alım deneyleriyle birlikte bu bulgular, sortilinin tiroglobulindeki iyot atomlarını “saymadığı” yönündeki revize görüşü destekliyor. Bunun yerine sortilin, proteinin gevşeyip kısmen parçalanarak monomerik formunu ve kuyruğunu doğru şekilde ortaya koyup koymadığını algılıyor.
Bu Tiroit Sağlığı İçin Ne Anlama Geliyor
Uzman olmayanlar için ana mesaj şudur: tiroid hormonu salımı dahili bir iyot sensöründen çok, proteinin şekline ve esnekliğine yönelik mekanik bir kontrolden daha çok etkilenir. Sortilin, hücre yüzeyinde bir tarayıcı gibi davranarak gevşemiş veya budanmış ve monomer hâline gelmiş tiroglobulin moleküllerini arar, ardından nihai hormon salımı ve iyot geri dönüşümü için onları içeri çeker. Bu çalışma tiroid hormon biyolojisindeki kritik bir adımı netleştiriyor ve sortilini engelleyecek şekilde tasarlanmış ilaçların—başka hastalıklar için araştırılanların—bu tanıma adımını bozarak istemeden tiroid hormonu dengelerini değiştirebileceğine işaret ediyor.
Atıf: Boniardi, I., Tanzi, G., Di Ianni, A. et al. Molecular recognition of thyroglobulin by sortilin. Nat Commun 17, 2004 (2026). https://doi.org/10.1038/s41467-026-68658-z
Anahtar kelimeler: tiroid hormonu, tiroglobulin, sortilin, protein trafiği, endositoz