Clear Sky Science · tr
RoboA, planaryanın kök hücre kaderini FoxA ve Anosmin1a aracılığıyla güçlendirir
Solucanlar Organlarını Nasıl Yeniden Büyütür
Bazı yassı solucanlar, beslenme tüplerinden beyinlerine kadar neredeyse herhangi bir eksik vücut parçasını yeniden büyütebilir. Bu olağanüstü yetenek, talep üzerine birçok farklı hücre tipine dönüşebilen erişkin kök hücrelere dayanır. Ancak bu kadar geniş bir serbestlikle, bu hücreler yanlış dokuyu yanlış yerde oluşturmayı nasıl önler—örneğin başta nöronlar yerine mide hücreleri üretmekten? Bu çalışma, rejenerasyon sırasında son derece esnek kök hücreleri doğru yolda tutan küçük bir sinyal setinin nasıl çalıştığını ortaya çıkarmak için planarya yassı solucanını kullanıyor.
Yenilenen Solucan ve Gizli Potansiyeli
Planarya Schmidtea mediterranea, vücut genelinde yaygın bir kök hücre popülasyonuna sahip olduğu için rejenerasyonu incelemek için tercih edilen bir modeldir. Anahtar organlardan biri, solucanın ortasında yer alan ve hayvanın yemesi sırasında dışarıya açılan kaslı bir beslenme tüpü olan farenks (yemek borusu)dir. Önceki çalışmalar, foxA adlı bir genin bu farenksi hasardan sonra yeniden inşa etmek için kritik olduğunu ve yalnızca farenks yakınındaki belirli kök hücrelerin normalde foxA’yı açtığını göstermişti. Yeni çalışma, aldatıcı derecede basit bir soruyu soruyor: diğer bölgelerde—özellikle baş ve beyin bölgesinde—bulunan kök hücrelerin neden farenks kimliğini seçmesini engelleyen şey nedir?
Yönlendirme Kaybolduğunda
Araştırmacılar, kök hücreler de dahil olmak üzere birçok hücre tipinde düşük seviyelerde bulunan RoboA adlı bir reseptör proteine odaklandı. RNA müdahalesi ile RoboA aktivitesini azalttıklarında, hayvanlar kesildikten sonra sık sık ekstra, yanlış yerde farenksler büyüttü. Daha yakından bakıldığında daha ince bir gerçek ortaya çıktı: yaralanmamış solucanlarda bile RoboA’nın azaltılması, beyin bölgesi içinde farenks-benzeri nöronlar ve kasların belirmesine neden oldu. Bu “ektopik farenks nöronları” gen ifadeleri açısından normal farenks hücreleri gibi davrandı, ancak artık yanlış yerdeydiler. Önemli olarak, genel vücut planı ve beyin mimarisi büyük ölçüde korunmuştu; bu da RoboA’nın tüm hayvanı yeniden şekillendirmediğini, bunun yerine yakındaki kök hücrelerin ne olduğuna ince bir ayar yaptığını gösteriyor.
Hücre Kaderi İçin Üç Oyunculu Bir Anahtar
RoboA’nın nasıl çalıştığını anlamak için ekip hücre dışındaki ortakları aradı. Robo proteinleri en iyi Slit adlı bir liganda bağlanmalarıyla bilinse de, Slit’in azaltılması yanlış yerde farenks hücrelerini yeniden üretmedi. Salınan ve membran proteinlerinin büyük bir RNAi taraması bunun yerine Anosmin1a (Anos1a) adlı, Kallmann sendromunda rolü olan insan bir faktöre ilişkili salınan bir proteini işaret etti. Anos1a’nın azaltılması benzer ekstra farenks nöronlarına yol açtı ve birlikte yapılan RoboA–Anos1a baskılamaları aynı yolakta hareket ediyormuş izlenimi verdi. Aynı zamanda moleküler profilleme, transkripsiyon faktörü FoxA’nın kararın merkezinde yer aldığını gösterdi: RoboA bulunduğunda, baştaki kök hücrelerde FoxA kapalı tutuluyor; RoboA sinyallemesi kaldırıldığında FoxA açılıyor ve aynı kök hücreler beyinde otururken bile farenks nöronu kaderini seçebiliyor.
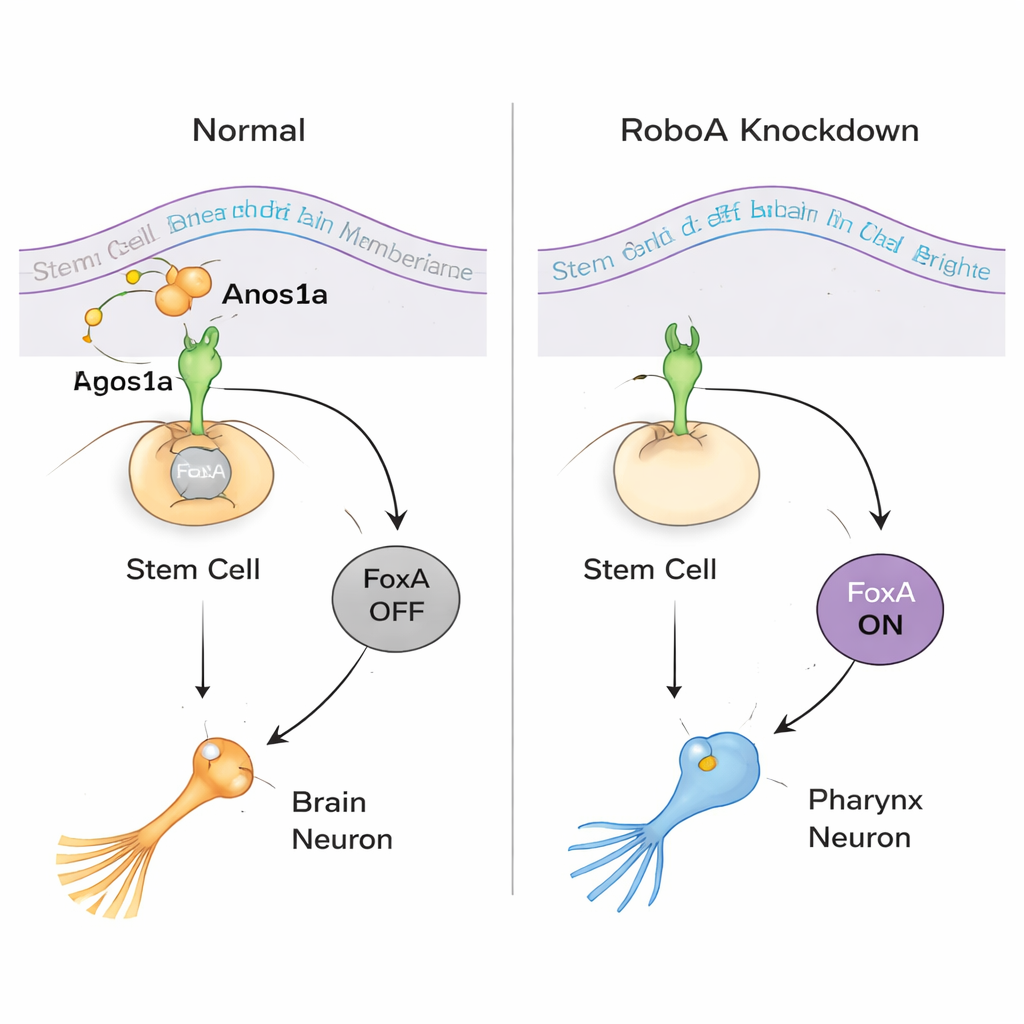
Kök Hücrelerde İki Yönlü Bir Seçimi Ortaya Çıkarmak
Ekip daha sonra bu esnekliğin her iki yönde işleyip işlemediğini sordu. Normal hayvanlarda farenks etrafındaki kök hücreler farenks nöronları ve epitel hücreler olmak için FoxA’ya güvenirken, farenks kasları farklı bir rotayı takip eder. FoxA daha uzun süre bastırıldığında, solucanlar farenkslerini tamamen kaybetti ve vücudun ortasında anormal çıkıntılar büyüdü. Tek hücre RNA dizilemesi ve belirteç analizi, bu çıkıntıların göz hücreleri ve beyne özgü nöronlar dahil olmak üzere normalde başla sınırlı birçok hücre tipi içerdiğini ortaya koydu. Başka bir deyişle, farenksin oluşması gereken yerde FoxA eksik olduğunda, yerel kök hücreler varsayılan olarak beyin-benzeri bir kadere yöneliyor. Bu bulgu, aynı kök hücrelerin hangi sinyalleri aldıklarına bağlı olarak ya “farenks” ya da “beyin” kimliklerine itilme potansiyelinde olduğunu gösteriyor.
Haritayı Yeniden Çizmeyip Rejenerasyonu İnce Ayarlamak
Tüm kanıtları bir araya getirerek yazarlar, planarya rejenerasyonunun iki katmanlı olarak yönlendirildiğini öneriyor. Wnt ve diğer desenleyici moleküller gibi geniş "konum kontrolü" sinyalleri baş, gövde ve kuyruk gibi kaba haritayı kurar. Bunun üzerine, RoboA ve Anos1a gibi yerel "kaderi pekiştiren" genler güvenlik kontrolleri olarak görev yapar ve uygunsuz seçenekleri engeller. Başta, RoboA–Anos1a sinyalleşmesi FoxA’yı kapalı tutarak kök hücrelerin farenks hücresi yerine beyin nöronları üretmesini sağlar; farenks yakınında ise FoxA açılmasına izin verilir ve farenks-spesifik kaderleri sürdürür. Bu katmanlı kontrol, planarya kök hücrelerinin son derece plastik kalmasını sağlarken organları doğru yerde yeniden inşa etmelerine olanak tanır ve sağlam rejenerasyonun katı anatomik düzenle nasıl bir arada var olabileceğine dair bir şablon sunar.
Atıf: Wang, KT., Tsai, FY., Chen, YC. et al. RoboA reinforces planarian stem cell fate through FoxA and Anosmin1a. Nat Commun 17, 1971 (2026). https://doi.org/10.1038/s41467-026-68656-1
Anahtar kelimeler: planarya rejenerasyonu, kök hücre plastisitesi, organ desenlenmesi, RoboA sinyalleşmesi, FoxA transkripsiyon faktörü