Clear Sky Science · tr
NeoPrecis: nitelikli immünojenisite ve klonalliği dikkate alan neoantijen manzaralarının entegrasyonu ile immünoterapi yanıt tahminini iyileştirme
Neden bazı kanserler immünoterapiye cevap verir, bazıları vermez
İmmünoterapi kanser bakımını dönüştürdü, ancak birçok hasta hâlâ fayda görmüyor ve bazıları ciddi yan etkilere maruz kalabiliyor. Önemli bir soru, neden bazı tümörlerin bağışıklık sistemi tarafından fark edilip yok edildiği, bazılarının ise gözden kaçtığıdır. Bu çalışma, tümörlerin bağışıklık sistemine gösterdiği “bayraklara”—neoantijenlere—daha yakından bakan ve bu bilgiyi modern immünoterapilere hangi hastaların yanıt verme olasılığının daha yüksek olduğunu daha iyi tahmin etmek için kullanan NeoPrecis adlı hesaplamalı bir yöntemi tanıtıyor.
Kanser hücrelerindeki yeni işaretler
Kanser hücreleri, ürettikleri proteinleri değiştirebilen DNA mutasyonları biriktirir. Bu değişmiş proteinlerin küçük parçacıkları olan neoantijenler, hücre yüzeyinde sergilenebilir ve T hücreleri—bağışıklık sisteminin katilleri—tarafından yabancı olarak tanınabilir. Yıllardır doktorlar ve araştırmacılar, tümör mutasyon yükü gibi kaba ölçütlere güvenerek bir kanserin immün kontrol noktası inhibitörlerine yanıt verme olasılığını tahmin etmeye çalıştılar. Ancak bu kaba bir araçtır: her mutasyon T hücreleri için görünür veya çekici bir hedef yaratmaz ve tümörler birçok farklı hücre alt tipinin bir karışımı olabilir. NeoPrecis, sadece mutasyonları saymanın ötesine geçerek bunların tüm tümör boyunca gerçekten umut verici hedefler olup olmadığını değerlendirmek için tasarlandı.
Aynı anda üç ana bileşene bakmak
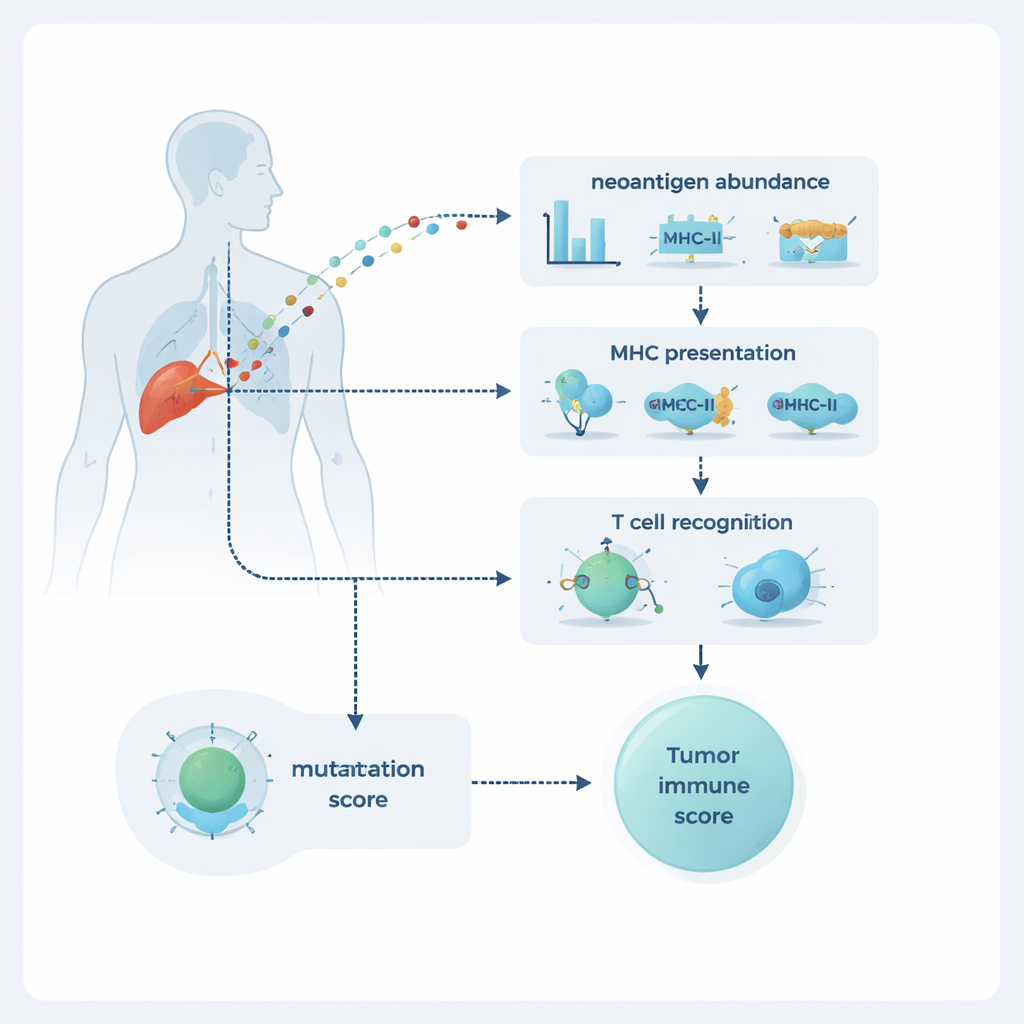
NeoPrecis her mutasyonu üç boyutta değerlendirir: tümörde ne kadar yaygın olduğu, hücre yüzeyinde sergilenme olasılığı ve T hücreleri tarafından fark edilme olasılığı. Yaygınlık, mutasyonun ne kadar yaygın olduğunu ve ne kadar güçlü ifade edildiğini ortaya koyan DNA ve RNA dizilemesinden tahmin edilir. Sergilenme, T hücrelerine protein parçacıklarını gösteren ilan panoları gibi davranan MHC sınıf I ve sınıf II moleküllerine bağlanma yoluyla modellenir. En yenilikçi kısım ise T hücre tanıma bileşeni olan NeoPrecis-Immuno’dur. Bu model, farklı mutasyonlu peptitlerle T hücreleri arasındaki bilinen etkileşimleri içeren büyük veri tabanlarından öğrenerek, bir mutasyona uğramış fragmanın T hücresi tanıması açısından önem taşıyan ölçüde normal karşılığından ne kadar farklı olduğunu değerlendirir ve aynı zamanda her bireyin taşıdığı özgül MHC varyantlarını da hesaba katar.
Bir bilgisayara T hücrelerinin “gördüklerini” öğretmek
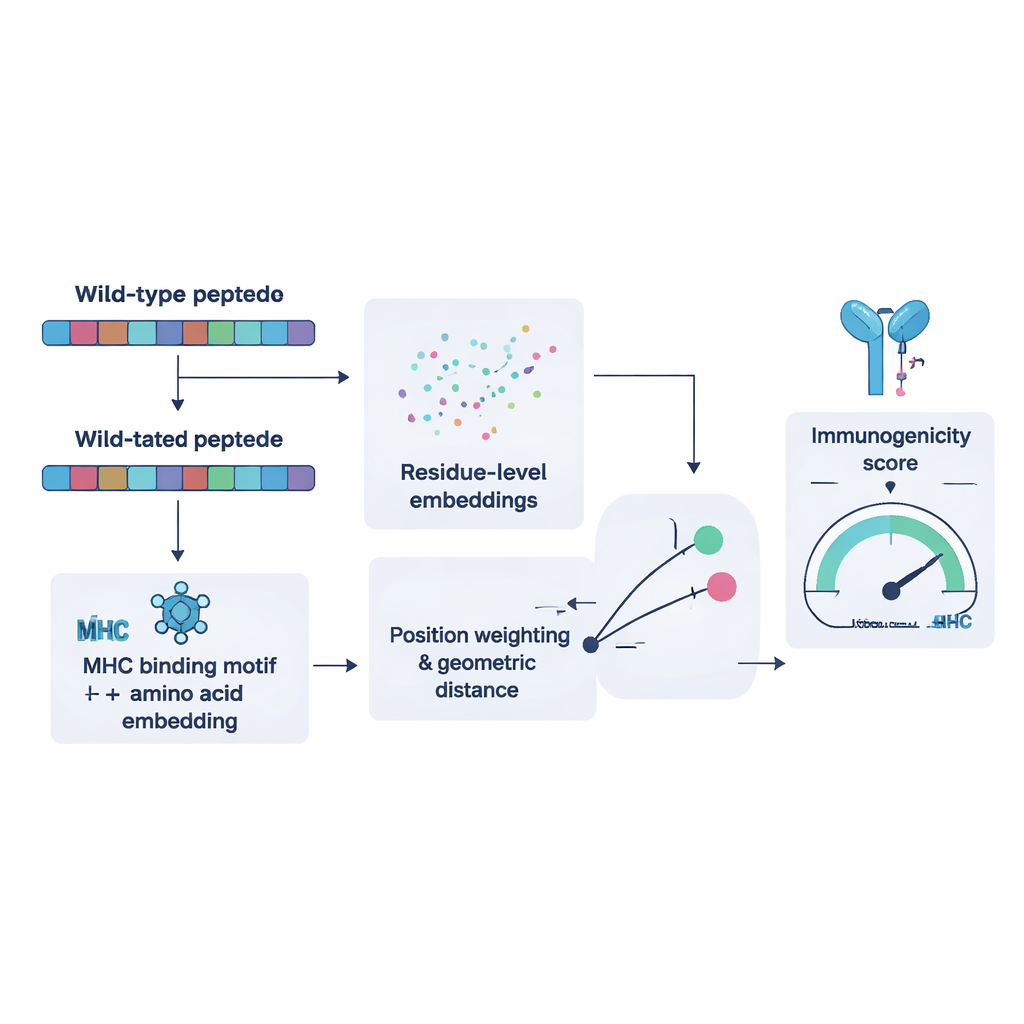
NeoPrecis-Immuno’yu eğitmek için araştırmacılar önce aynı T hücresinin birden çok benzer peptidi tanıdığı ve bazılarını tanımadığı binlerce örneği topladılar. Bunları kullanarak model, normal peptidlere çok benzeyen mutasyonlu fragmanların bağışıklık saldırısı tetikleme olasılığının daha düşük olduğunu öğrendi; çünkü böyle kendine benzer hedefler T hücresi gelişimi sırasında genellikle elenir. Model, her peptidi amino asit dizisi ve kişinin MHC moleküllerinin bağlanma tercihleri tarafından şekillendirilen matematiksel bir alandaki bir nokta olarak temsil eder. Ardından mutasyonlu peptidin orijinalinden ne kadar uzakta olduğunu ölçer. Motif bilgisiyle desteklenen daha büyük uzaklıklar, immünojen olma şansının daha yüksek olmasıyla ilişkilendirilir. Bağımsız kanser veri setleri üzerinde mevcut araçlarla karşılaştırıldığında NeoPrecis-Immuno, özellikle yardımcı T hücrelere sunum yapan MHC sınıf II ile çalışırken eşdeğer ya da daha iyi performans gösterdi.
Tek tek mutasyonlardan tüm tümöre
Bireysel mutasyonlar hikâyenin yalnızca bir parçasıdır; bunların tümör içindeki dağılımı da önem taşır. Bazı mutasyonlar neredeyse her kanser hücresinde bulunan “klonal” iken, diğerleri yalnızca belirli bölgelerde bulunan “subklonal”dır. NeoPrecis, mutasyonlar boyunca immünojenisite puanlarını toplayıp hangi alt klonlara ait oldukları ve bu alt klonların ne kadar yaygın olduğu bilgilerini katmanlayarak bir “neoantijen manzarası” oluşturur. Bu, hem MHC sınıf I hem de sınıf II moleküllerinde sunulabilen ve muhtemelen yardımcı ve öldürücü T hücrelerinin koordineli yanıtlarını tetikleyebilecek güçlü, yaygın neoantijenlere sahip kanserleri vurgulayan tümör düzeyinde puanlar üretir. Checkpoint inhibitörleri ile tedavi edilen melanom ve küçük hücre dışı akciğer kanseri hasta gruplarında, bu NeoPrecis tabanlı puanlar yanıt verenleri yanıt vermeyenlerden standart mutasyon sayımlarından daha doğru şekilde ayırdı ve özellikle karmaşık, heterojen akciğer tümörlerinde faydalı oldu.
Bu hastalar için ne anlama geliyor
Hastalar için NeoPrecis’in vaadi, immünoterapileri en çok fayda görecek olanlarla daha hassas eşleştirmek ve neden bazı tümörlerin tedaviye dirençli olduğunu daha net anlamaktır. Neoantijenlerin niceliğinden ziyade niteliğine ve dağılımına odaklanarak bu çerçeve, benzer mutasyon yüküne sahip tümörlerin neden çok farklı davranabileceğini açıklamaya yardımcı olur. Gelecekte, bir tümörün bağışıklık tarafından görülen manzarasının bu kadar ayrıntılı haritaları, yalnızca checkpoint inhibitörlerinin kullanımına rehberlik etmekle kalmayıp, aynı zamanda her kişinin kanserindeki en güçlü ve en yaygın hedefleri önceliklendiren kişiye özel kanser aşılarının tasarımına da yol gösterebilir.
Atıf: Lee, KH., Sears, T.J., Zanetti, M. et al. NeoPrecis: enhancing immunotherapy response prediction through integration of qualified immunogenicity and clonality-aware neoantigen landscapes. Nat Commun 17, 1966 (2026). https://doi.org/10.1038/s41467-026-68651-6
Anahtar kelimeler: kanser immünoterapisi, neoantijenler, tümör heterojenitesi, checkpoint inhibitörleri, hesaplamalı onkoloji