Clear Sky Science · tr
Entegre bir hesaplamalı-deneysel çerçeve ile verimli genom düzenlemesi için MmeFz2-ωRNA sisteminin mühendisliği
Daha Küçük Gen Makaslarıyla Büyük Tıbbi Sorunlar
Gen düzenleme, hastalıkları inceleme biçimimizi şimdiden değiştirdi; ancak bunu güvenli, uygulanabilir bir tıbba dönüştürmek hâlâ önemli bir zorluk. Büyük engellerden biri, CRISPR-Cas9 gibi bugün en güçlü DNA “makaslarının” fiziksel olarak büyük olması ve hastalarda kullanılan küçücük taşıyıcı paketlerine konmasının zor oluşudur. Bu çalışma, Fanzor2 adlı az bilinen bir enzim ailesinden türetilmiş yeni, kompakt bir gen düzenleyici tanıtıyor ve yapay zekânın bunu gelecekteki gen terapileri için güçlü bir aday hâline nasıl hızlıca yeniden tasarlayabileceğini gösteriyor.
Kompakt Bir Yeni Sınıf Gen Düzenleyici
Cas9 ve Cas12a gibi mevcut genom düzenleyicilerin çoğu, binin üzerinde yapı taşı içeren büyük proteinlerdir. Bu boyut, bunları gen terapilerinin önde gelen taşıma sistemi olan adeno-ilişkili virüslere (AAV) sıkıştırmayı zorlaştırır. Buna karşılık, Fanzor2 proteinleri çok daha küçüktür ve hayvanlar ve insanlar dahil ökaryotlarda doğal olarak bulunur. Yazarlar bu ailenin bir üyesi olan MmeFz2’ye odaklandı; MmeFz2, belirli DNA dizilerini bulup kesmek için ωRNA adlı kısa bir RNA molekülü kullanır. Kağıt üzerinde MmeFz2 terapi için ideal görünüyordu: kompakt ve programlanabilir. Ancak pratikte, insan hücrelerindeki etkinliği zayıftı; hedef bölgelerin yüzde birinin altında düzenleme yapıyordu. Ekip, bu düşük performanslı enzimi pratik bir araca dönüştürmeyi amaçladı.
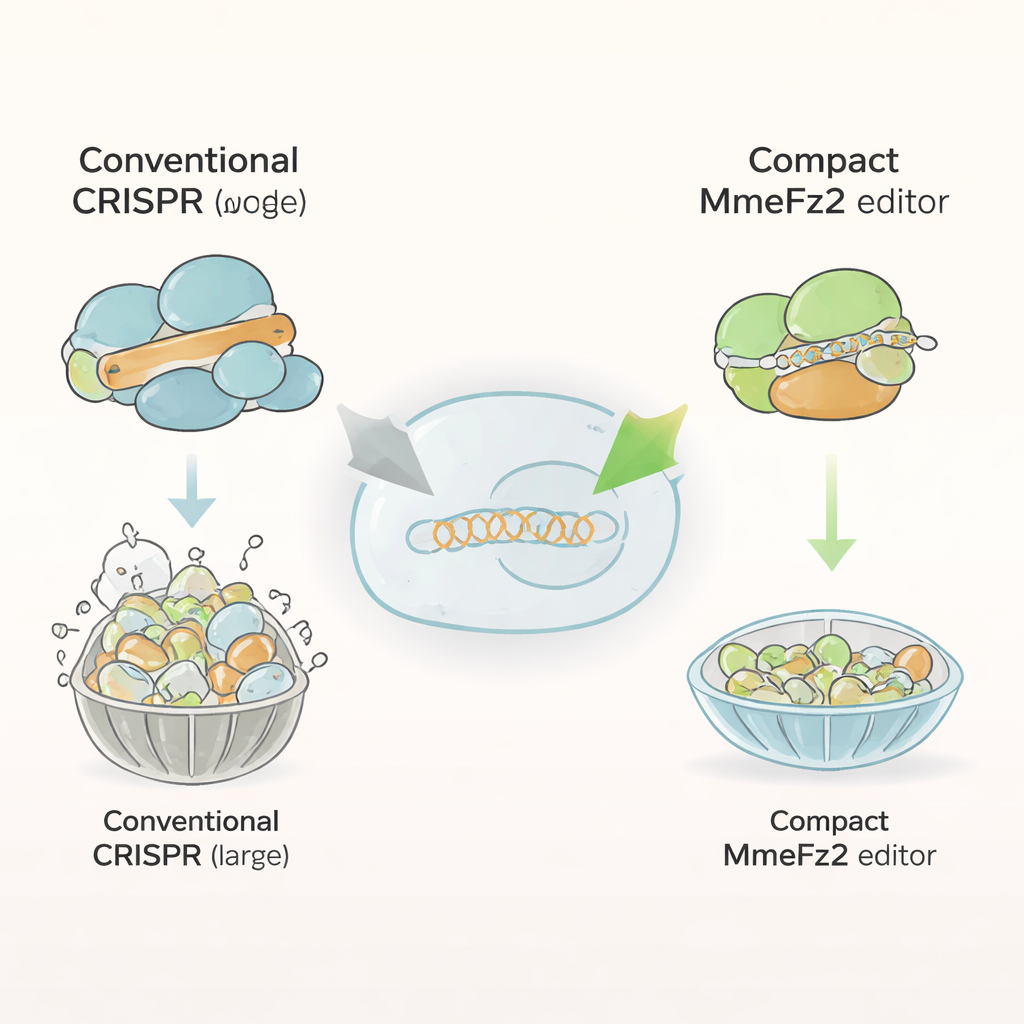
Yönlendirici Molekülü Yeniden Tasarlamak için YZ Kullanımı
İlk hedef, MmeFz2’ye nereye kesme yapacağını söyleyen kılavuz ωRNA’ydı. Araştırmacılar, protein–RNA–DNA komplekslerinin 3B yapısını tahmin eden son teknoloji bir program olan AlphaFold3’ü kullanarak MmeFz2’nin ωRNA ve bir DNA hedefi ile bağlanmış bir modelini oluşturdu. Bu sanal yapı, ωRNA’nın bazı kısımlarının gevşek, zayıf eşleşmiş ve proteine neredeyse değmiyor olduğunu ortaya koydu. Bu bilgi doğrultusunda ekip, RNA’daki kararsız bağları sistematik olarak değiştirdi ve transkripsiyona engel olabilecek uridin dizilerini çıkardı. Daha sonra insan hücrelerinde onlarca varyantı test ettiler. En iyi değişiklikleri üst üste koyup gereksiz bir sap (stem) bölgesini kısaltarak, yüzde 30 daha küçük ancak birçok DNA bölgesinde düzenleme veriminde yaklaşık 20 kat artış sağlayan kısaltılmış bir ωRNA yarattılar.
Proteini Makine Öğrenmesiyle İnce Ayarlama
Sırada proteinin kendisini iyileştirmek vardı. Yine AlphaFold3 kullanılarak MmeFz2’nin RNA ve DNA ile temas ettiği bölgeler haritalandı ve bu temasları güçlendirmeyi veya esnekliği artırmayı hedefleyen yüzün üzerinde tek amino asit değişikliği tasarlandı. Hücrelerde bunları taradıktan sonra performans verilerini, milyonlarca doğal diziden eğitilmiş protein dil modellerine dayanan bir makine öğrenmesi sistemi olan EVOLVEpro’ya verdiler. Bu araç hangi özelliklerin etkinliği artırma eğiliminde olduğunu öğrendi ve daha iyi çalışması öngörülen yeni kombinasyonlar önerdi. Bu hesaplamalı–deneysel döngünün birkaç turu sonucunda, geliştirilmiş ωRNA ile eşleştirildiğinde başlangıç sistemine kıyasla düzenleme etkinliğini 60 katın üzerinde artıran iki optimize enzim varyantına ulaştılar.
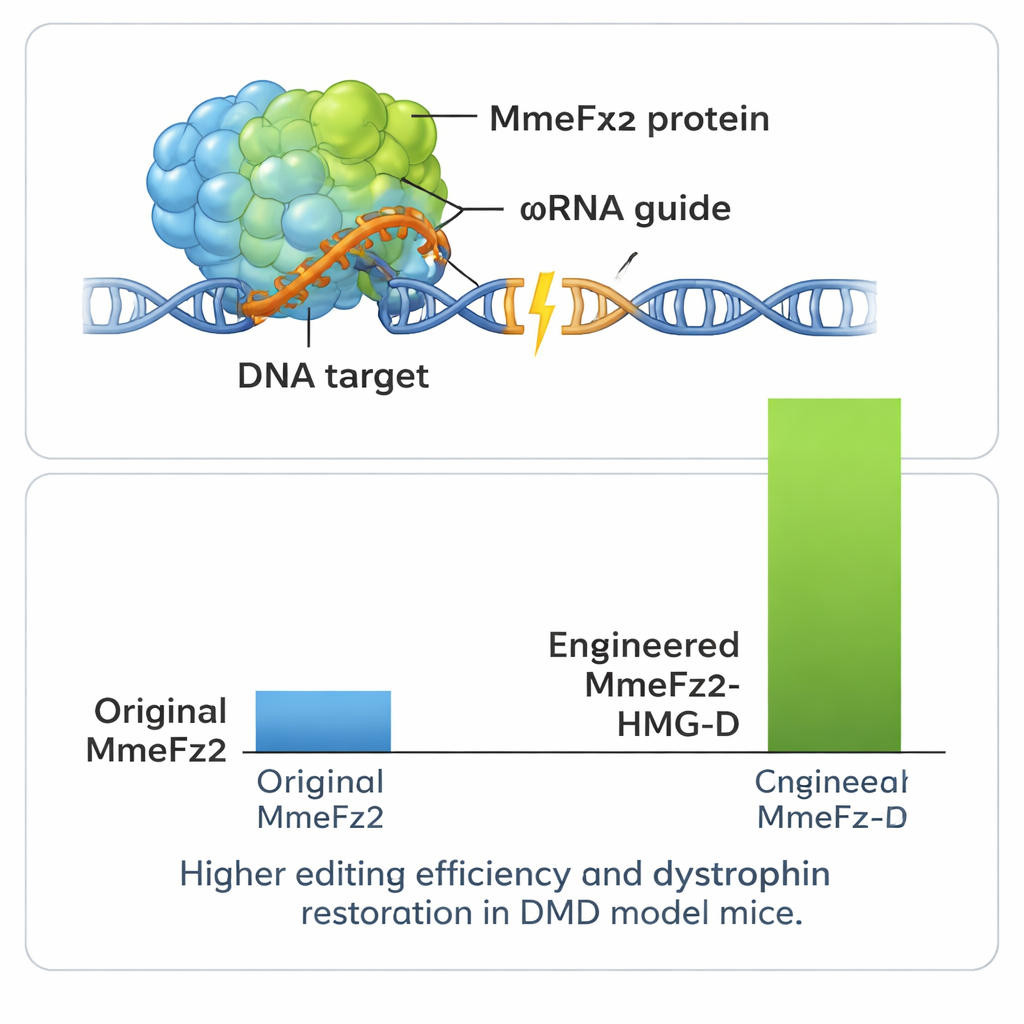
Gücü Artırma ve Hastalık Modelinde Test Etme
Sistemin performansını daha da artırmak için yazarlar MmeFz2’yi genetik materyale tutunmayı kolaylaştıran küçük DNA-bağlayıcı bölgelerle füzelediler. Bunlardan biri olan HMG-D, mühendislenmiş enzimin ucuna eklendiğinde özellikle etkili oldu ve bazı bölgelerde yüzde 80’in üzerinde düzenleme düzeyleri üretti. Önemli olarak, genomdaki öngörülen hedef dışı (off-target) yerlerde yapılan testler, bu ek gücün önemli bir hassasiyet kaybı ile birlikte gelmediğini gösterdi. Tüm gen düzenleyici — protein ve kılavuz RNA dahil — çok kompakt olduğu için tek bir AAV vektörüne rahatça sığabiliyor; bu, çoğu CRISPR sistemi için mümkün değil. Ekip bu avantajı Duchenne kas distrofisi fare modelinde kullandı; bu ölümcül kas erimesi bozukluğu dystrophin genindeki hatalardan kaynaklanır. Bacak kasına tek seferlik AAV ile iletilen düzenleyicinin injeksiyonu, genin RNA’sında tespit edilebilir düzeltmelere yol açtı ve önemli bir oranda kas lifinde dystrophin proteinini geri getirdi.
Gelecek Gen Tedavileri için Anlamı
Uzman olmayanlar için ana mesaj şudur: Yazarlar zayıf, az bilinen bir gen kesme enzimini tek virüs paketinde taşınabilen, yüksek performanslı bir editöre dönüştürdüler ve gerçekçi bir hayvan modelinde ciddi bir genetik hastalığı onarabildiler. Aynı derecede önemli olan, bu sonuca ulaşma biçimleri: yapıya dayalı yapay zekâ tahmini ve makine öğrenmesini odaklanmış laboratuvar testleriyle sıkı şekilde birleştirerek hem proteini hem de kılavuz RNA’yı geleneksel deneme-yanılma yaklaşımlarından çok daha verimli bir şekilde geliştirdiler. Bu entegre strateji, bir sonraki nesil birçok genom editörünün oluşturulmasını hızlandırabilir ve kas distrofisi ile diğer kalıtsal hastalıklardaki hastalara daha hassas ve daha güvenli gen terapilerini daha yakın hale getirebilir.
Atıf: Li, S., Xu, K., Li, G. et al. Engineering the MmeFz2-ωRNA system for efficient genome editing through an integrated computational-experimental framework. Nat Commun 17, 1867 (2026). https://doi.org/10.1038/s41467-026-68644-5
Anahtar kelimeler: gen düzenleme, CRISPR alternatifleri, Duchenne kas distrofisi, viral gen tedavisi, biyolojide yapay zeka