Clear Sky Science · tr
C1q-bağımlı alfa-sinükleinin temizlenmesi, makrofajların erkek farelerde enterik sinüklinopatiyi geçici olarak sınırlamasına izin veriyor
Beyin Hastalığında Bağırsak Neden Önemlidir
Parkinson hastalığı titreme ve hareket problemleriyle bilinir, ama birçok kişi herhangi bir motor semptom ortaya çıkmadan yıllarca şiddetli kabızlık ve diğer bağırsak sorunları yaşar. Bu çalışma, Parkinson ile ilişkili bir proteinin bağırsakta yanlış katlanıp biriktiğinde “vücudun ikinci beyni” sayılan bağırsak sinir ağında neler olduğunu ve yerel bağışıklık hücrelerinin önce nasıl yardım ettiğini, sonra neden başarısız olduğunu araştırıyor. İntramukozal bu erken savaşı anlamak, semptomları hafifletmenin ve belki de beyin ağır hasar görmeden önce hastalık ilerlemesini yavaşlatmanın yeni yollarını açabilir.
Vücudun İkinci Beynindeki Sorunlu Bir Protein
Parkinson hastalığında ve ilişkili bozukluklarda alfa-sinüklein adlı bir protein yanlış katlanabilir ve toksik agregatlar halinde kümelenebilir. Bu kümeler yalnızca beyinde değil, bağırsak hareketini kontrol eden enterik sinir sisteminin tamamında da bulunur. Birçok araştırmacı, en az bazı hastalarda yanlış katlanmış alfa-sinükleinin önce bağırsakta yerleşip sinir yolları boyunca beyne doğru yayılabileceğini düşünüyor. Yazarlar, önceden oluşmuş alfa-sinüklein fibrillerinin mide ve ince bağırsağın üst kısmına enjekte edildiği bir fare modeli kullandı. Önümüzdeki iki ay boyunca, bağırsak nöronlarında kimyasal olarak işaretlenmiş anormal alfa-sinüklein seviyelerinde sürekli bir artış gözlemlediler. Bu birikim, bağırsaklardan materyalin daha yavaş geçmesi ve dışkı miktarının azalması ile eşzamanlıydı; bu, Parkinson’lu birçok kişide görülen kabızlığı yansıtıyor.
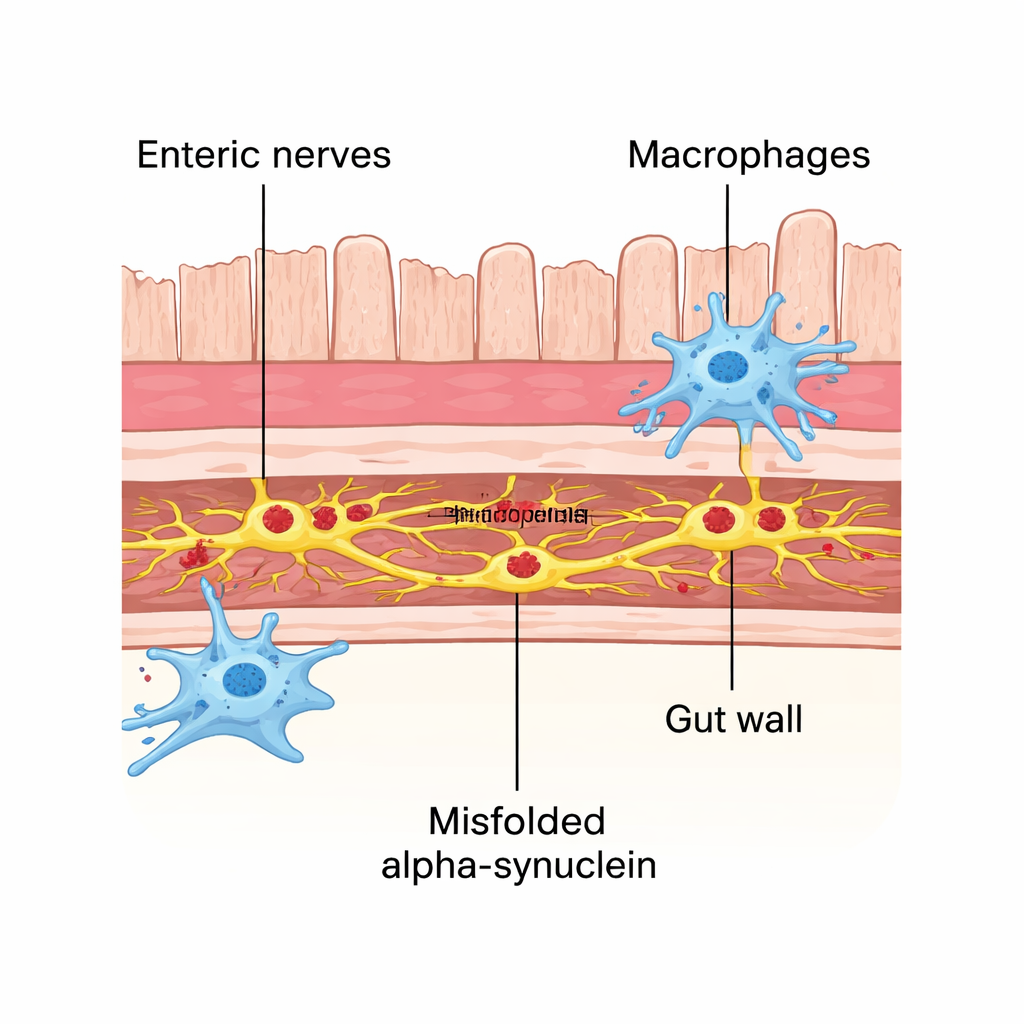
İlk Müdahaleciler Olarak Bağırsak Bağışıklık Hücreleri Devreye Giriyor
Bağırsak duvarı, komşu nöronlarla sürekli iletişim kuran ve dokunun sağlığını koruyan yerleşik bağışıklık hücreleri olan makrofajları içerir. Bu modelde, bu makrofajlar yalnızca hasara tepki göstermekle kalmadı: etkilenen sinir kümeleriyle fiziksel temas kurma sıklıkları arttı ve içinde yanlış katlanmış proteinden küçük noktacıklar barındırdılar. Araştırmacılar bu makrofajları bir antikor tedavisiyle azalttıklarında, enterik nöronlardaki alfa-sinüklein patolojisi anlamlı şekilde arttı. Bu, bağırsak makrofajlarının erken koruyucu bir rol oynadığını; toksik proteini çevre sinir hücrelerinden önce yutarak temizleyen hücresel temizlikçi işlevi gördüğünü öne sürdü.
Yardımcı — ve Zararlı Olabilen Moleküler Bir Etiket
Bu bağışıklık hücrelerinin neyi tanıyıp kaldırdığını anlamak için ekip tek hücreli RNA dizilemesine başvurdu ve binlerce bireysel bağırsak bağışıklık hücresini profilledi. Kas tabakalarındaki belirli makrofaj alt tiplerini, yutma ve protein parçalama ile ilişkili genleri açmış olarak tanımladılar; özellikle kan dolaşımında daha bilinen bir moleküler etiketleme yolu olan kompleman sistemi bileşenleri öne çıktı. Önemli bir oyuncu, C1q, bu bağırsak makrofajlarında yüksek düzeyde aktiftir. Mikroskopta C1q, etkilenen enterik nöronları kaplamış halde görüldü ve makrofajlar hem C1q hem de yanlış katlanmış alfa-sinüklein için pozitif noktacıklar içeriyordu; bu, C1q’nin toksik proteini temizlenmesi için etiketlemeye yardımcı olduğunu gösteriyor. Bilim insanları genetik olarak C1q’den yoksun fareler kullandıklarında, nöronal alfa-sinüklein patolojisi kötüleşti ve makrofajlar daha az protein kümesi içselleştirdi. Buna karşın şaşırtıcı şekilde, bu C1q-eksik farelerin aynı fibrillere maruz kalan normal farelere göre bağırsak motilitesi biraz daha iyiydi; bu da toksik proteini temizleyen sürecin, muhtemelen hareketi kontrol eden sinir bağlantılarını budayarak veya zayıflatarak bağırsak fonksiyonunu bozabileceğini düşündürüyor.
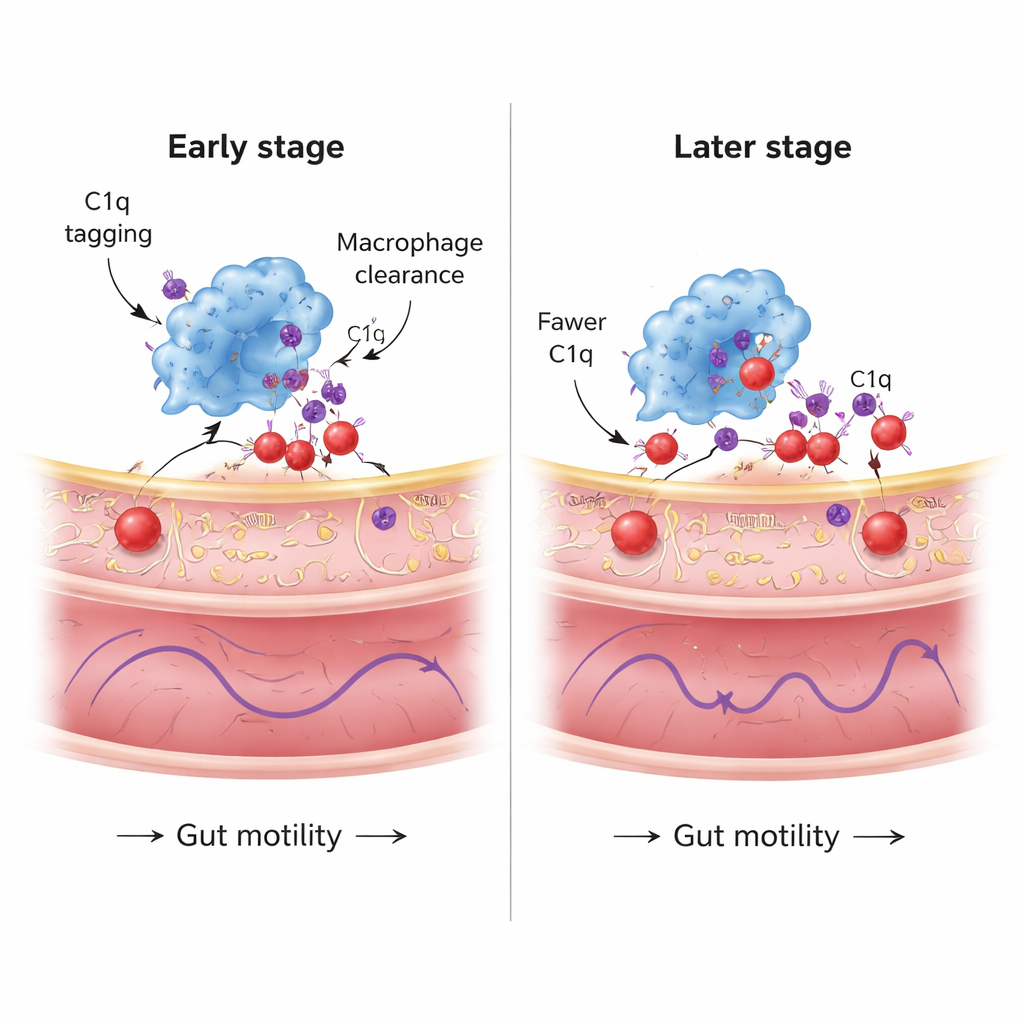
Zamanla Sönen Koruyucu Bir Sistem
Çalışma ayrıca bu temizleme yanıtını daha uzun bir süre izledi. Alfa-sinüklein verildikten yaklaşık bir ay sonra, makrofajlar güçlü C1q ekspresyonu ve hücre gövdelerinde çok sayıda C1q-etiketli protein noktacığı gösterdi; C1q enterik nöronları yoğun şekilde kaplamıştı. Ancak iki ayda, makrofajlardaki genel C1q düzeyleri devam etse de, içselleştirilmiş C1q/alfa-sinüklein noktacıklarının sayısı ve nöronlara biriken C1q miktarı azaldı. Aynı zamanda bağırsaktaki nöronal patoloji artmaya devam etti. Gen analizi, yanlış katlanmış proteinlerin sürekli alımının makrofajların protein işleme makinelerini zorladığını; yanlış katlanmış proteinlere, lizozomlara ve hatta hücre ölümü ile ilişkili stres yolaklarını aktive ettiğini öne sürdü. Başka bir deyişle, makrofajların koruyucu kapasitesi sınırlı görünüyor: başlangıçta patolojiyi dizginliyorlar, ama stres biriktikçe alfa-sinükleini temizleme yetenekleri azalıyor.
Bu, Parkinson ve Bağırsak İçin Ne Anlama Geliyor
Bu çalışma, bağırsak bağışıklık hücrelerinin bağırsaktaki erken Parkinson benzeri değişimleri nasıl şekillendirdiğine dair nüanslı bir tablo çiziyor. İlk etapta yerleşik makrofajlar C1q kullanarak misfolded alfa-sinükleini işaretleyip yutarak yayılmasını sınırlıyor. Ancak aynı kompleman kaynaklı budama, sinir sinyallemesini bozup bağırsak hareketini yavaşlatarak kabızlığa katkıda bulunabilir. Zamanla makrofajların stres yükü altındaki temizleme sistemi zayıflar ve bağırsakta daha fazla patoloji birikmesine izin verir; bu sırada bağırsak fonksiyonu ile beyin tutulumu ayrışabilir. Hastalar için bu, bağırsaktaki makrofaj aktivitesini veya kompleman sinyallemesini hedef almanın — güvenli temizlemeyi artırırken aşırı sinaps kaybını önlemeyi amaçlayarak — bir gün Parkinson ile ilişkili bağırsak semptomlarını tedavi etme veya önleme ve belki de hastalığın genel seyrini etkileme stratejisi olabileceğini öne sürüyor.
Atıf: Mackie, P.M., Koshy, J.M., Bhogade, M.H. et al. C1q-dependent clearance of alpha-synuclein allows macrophages to transiently limit enteric synucleinopathy in male mice. Nat Commun 17, 1877 (2026). https://doi.org/10.1038/s41467-026-68641-8
Anahtar kelimeler: Parkinson hastalığı, enterik sinir sistemi, alfa-sinüklein, bağırsak bağışıklık hücreleri, komplement C1q