Clear Sky Science · tr
Katlanmamış durumlar açıkça hesaba katılarak protein katlanma kararlılığının tahmini
Protein kararlılığının neden önemi var
Vücudunuzdaki her protein, düzgün çalışmak için belirli bir üç boyutlu şekle katlanması gereken küçük bir moleküler makinedir. Bu katlanma çok kırılgansa, protein yanlış çalışabilir, kümelenebilir veya hiç üretilmeyebilir—bunlar hastalıklarla ve protein temelli ilaçlar ile enzimlerin üretimindeki başarısızlıklarla ilişkilidir. Laboratuvarda bir proteinin ne kadar kararlı olduğunu ölçmek yavaş ve güçtür; bu yüzden bilim insanları, yalnızca diziden yola çıkarak bir proteinin ne kadar kolay açılacağını güvenilir şekilde söyleyebilen bilgisayar yöntemleri arıyorlar.
Katlanmış ve katlanmamış proteinlere yeni bir bakış
Çoğu modern algoritma neredeyse tamamen proteinin katlanmış şekline odaklanır. Genellikle AlphaFold gibi yapay zekâ tarafından tahmin edilen bir yapıya dayanır ve o tek yapıyı kararlılığın ana belirleyicisi olarak kabul ederler. Oysa kararlılık gerçekte iki geniş topluluğun enerji farkıdır: kompakt katlanmış durum ile katlanmamış durumu oluşturan çok sayıda gevşek şekil. Yazarlar, katlanmamış tarafın ihmal edilmesinin, mevcut araçların katlanma serbest enerjisinin (ΔG) deneysel ölçümleriyle uyuşmasında başarısız olmasının temel nedenlerinden biri olduğunu savunuyorlar.
Her iki durumu da öğrenen yeni bir model
Araştırmacılar, ΔG’yi tahmin etmek ve her protein için katlanmış ile katlanmamış durumların dengesinin nasıl göründüğünü aynı anda öğrenmek üzere tasarlanmış derin öğrenme sistemi IFUM’u tanıtıyorlar. Katlanmamış durumu belirsiz bir arka plan olarak ele almak yerine IFUM, onu bir “rastgele halka” olarak temsil etmek için polimer fiziğinden fikirler kullanıyor ve hem katlanmış hem de katlanmamış durumları amino asit çiftleri arasındaki mesafelerin haritaları olarak kodluyor. Model, güçlü önceden eğitilmiş dizi ve yapı ağlarından bilgi alıyor, ardından toplam kararlılığı ve proteinin nüfusunun her kalıntı çiftinde ne kadarının katlanmış mı yoksa katlanmamış mı olduğunu tanımlayan bir olasılık haritasını eşzamanlı olarak tahmin ediyor. Çok büyük bir küçük, deneysel olarak karakterize edilmiş proteinler ve bilinen düzensiz proteinler veri kümesi üzerinde eğitim, IFUM’un hem iyi yapılandırılmış hem de gevşek dizileri tanımasına yardımcı oluyor.
Daha iyi sayılar ve daha geniş mutasyon kapsamı
Kontrollü bir küçük protein veri kümesi üzerinde test edildiğinde, IFUM deneysel ΔG değerlerini yalnızca katlanmış yapıya veya diziler üzerinde eğitilmiş dil modellerine dayanan önceki yapay zekâ tabanlı yöntemlere kıyasla daha düşük hata ve daha yüksek korelasyonla tahmin ediyor. Kritik olarak, model aynı zamanda çok çeşitli dizi değişikliklerini de işleyebiliyor. Tek ve çift nokta mutasyonların etkilerini doğru yakalıyor; ayrıca protein uzunluğunu değiştiren eklemeler ve silinmeler gibi birçok mevcut aracın ya tamamen başarısız olduğu ya da çalışacak şekilde tasarlanmadığı durumları doğru değerlendirebiliyor. İçsel bir karşılaştırma, katlanmamış durum hedefinin kaldırılmasının performansı önemli ölçüde kötüleştirdiğini gösteriyor; bu da katlanmamış topluluğun açıkça modellenmesinin sadece kavramsal bir incelik değil, tahminlerin doğruluğu açısından merkezi olduğunu vurguluyor.
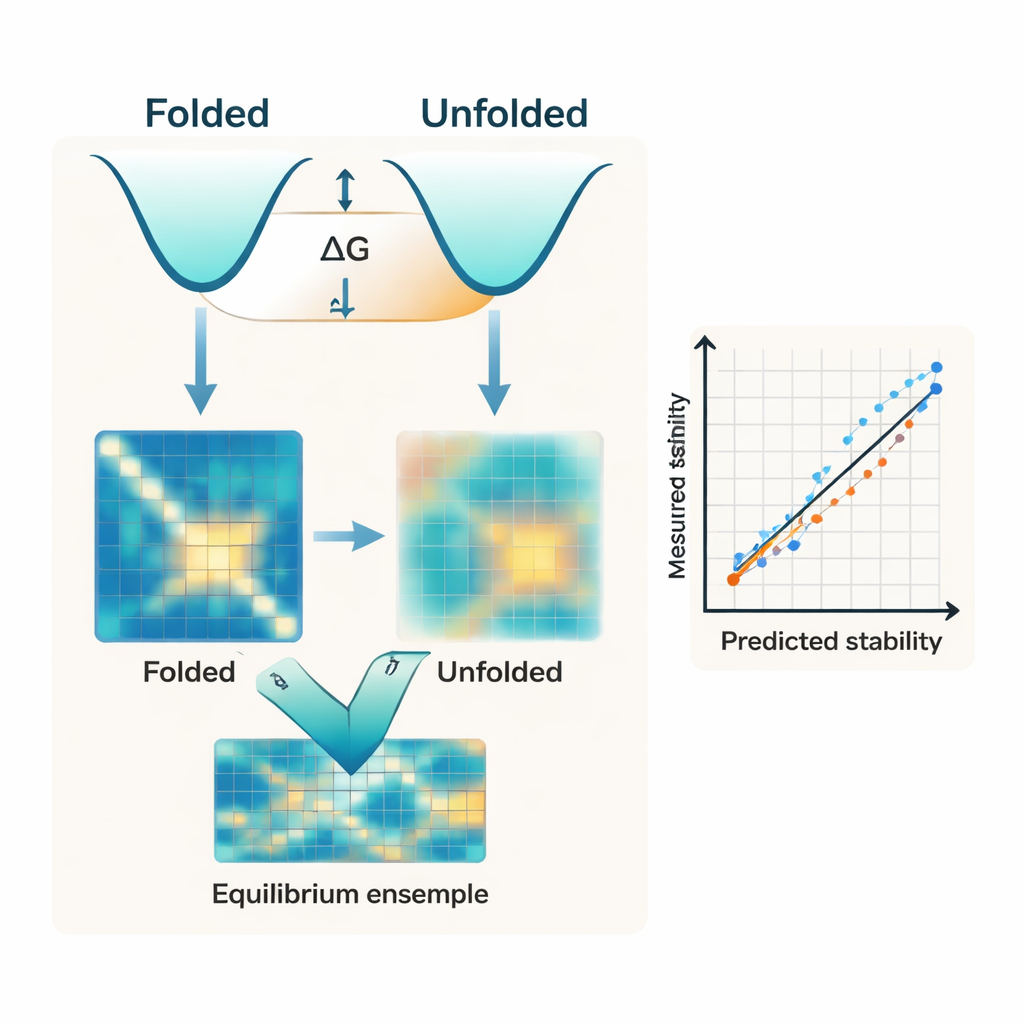
Tasarım tezgâhından gerçek dünya testlerine
IFUM’un gerçek protein mühendisliğine rehberlik edip edemeyeceğini görmek için yazarlar onu üç zor tasarım problemine uyguluyor: interferon‑lambda proteinlerini stabilize etmek, bağışıklık sinyal proteini IL‑10’u yeniden şekillendirmek ve UGT76G1 adlı bir şeker‑modifiye edici enzimi iyileştirmek. Üç durumda da IFUM’un öngördüğü kararlılıklar, proteinin çözülmeden önce ne kadar ısıya dayanabildiğini bildiren erime sıcaklıklarıyla iyi bir eşgüdüm gösteriyor. Model ayrıca hücrelerde katlanma ve çözünürlük ihtimali en yüksek olan yüzlerce tamamen yeni bilgisayar‑tasarımlı proteini tarayıp seçmeye yardımcı olarak, yapı tahmin ağlarının yaygın güven skorlarını geride bırakıyor. Bu sonuçlar, IFUM’un modern protein tasarım iş akışlarında yapı tabanlı kontrollerle birlikte pratik bir “kararlılık filtresi” olarak kullanılabileceğini düşündürüyor.
Sınırlar ve gelecek yönleri
Her model gibi IFUM’un da sınırları var. Model ağırlıklı olarak kısa, tek zincirli, çözünür proteinler üzerinde eğitildiği için, daha büyük proteinlerde veya geniş esnek döngülere ya da zar geçişli bölgelere sahip olanlarda mutlak kararlılık değerleri daha az güvenilir hale geliyor. Katlanmamış durum tanımı hâlâ tüm olası şekillerin tam gerçekçi bir resmi olmaktan çok basitleştirilmiş bir istatistiksel model niteliğinde. Yine de yaklaşım, bir yapay zekâyı hem katlanmış hem de katlanmamış toplulukları göz önünde bulundurmaya öğretmenin daha güvenilir kararlılık tahminleri verdiğini gösteriyor. Uzman olmayanlar için temel çıkarım, IFUM’un bize nicel güvenle “Bu protein tasarımı gerçekten bir arada durur mu?” diye bilgisayara sorma olanağına daha da yaklaştırdığı; bu da daha güvenli biyolojik ilaçların ve daha dayanıklı endüstriyel enzimlerin geliştirilmesini hızlandırabilir.
Atıf: Lee, H., Cho, Y., Yun, J. et al. Protein folding stability estimation with explicit consideration of unfolded states. Nat Commun 17, 1883 (2026). https://doi.org/10.1038/s41467-026-68637-4
Anahtar kelimeler: protein kararlılığı, protein katlanması, derin öğrenme, protein tasarımı, mutasyonlar