Clear Sky Science · tr
Tümör-bağışıklık etkileşimlerinin metabolik karakterizasyonu: Çoklu immünofloresans ile NSCLC’de (küçük hücre dışı akciğer karsinomu) immünoterapi yanıtının mekansal mekanizmalarını açığa çıkarma
Bu araştırma neden önemli
İmmünoterapi, bazı ileri derecedeki akciğer kanseri hastalarının tedavisinde çarpıcı değişiklikler getirdi; yine de çoğu hastada bu güçlü ilaçlara rağmen kanser ilerlemeye devam ediyor. Bu çalışma basit ama hayati bir soruyu gündeme getiriyor: farklı hücrelerin nerede bulunduğu ve ne kadar enerji kullandıkları gibi tümör dokusunun içini daha yakından inceleyerek kimlerin gerçekten immünoterapiden yararlanacağını öngörebilir miyiz? Küçük biyopsi örneklerini ayrıntılı hücresel haritalara dönüştürerek araştırmacılar akciğer kanseri bakımını gerçekten kişiselleştirilmiş bir yaklaşıma yaklaştırmayı amaçlıyor.
Akciğer tümörlerini bir şehir haritası gibi incelemek
Araştırma ekibi, immün kontrol noktası inhibitörleri ile tedavi edilen 55 ileri evre küçük hücre dışı akciğer karsinomu (NSCLC) hastasına ait dokuları inceledi. Tedavi öncesinde, tümör örnekleri çoklu immünofloresans kullanılarak 44 belirteçlik bir panelle boyandı; bu sayede aynı anda birçok protein görülebildi. Ardından derin öğrenme sistemi, tümör hücreleri, T hücreleri, B hücreleri, makrofajlar ve fibroblastlar gibi kilit hücre tiplerini tanımladı; bu hücrelerin işlevsel durumunu (örneğin aktif, bölünen veya tükenmiş) ve bunların metabolik profillerini, yani enerji üretim ve kullanım biçimlerini sınıflandırdı. Sadece hücreleri saymakla kalmayıp, araştırmacılar hücrelerin birbirleriyle nasıl konumlandığını da haritalandırarak her biyopside mahalle benzeri bölgeler oluşturdular.
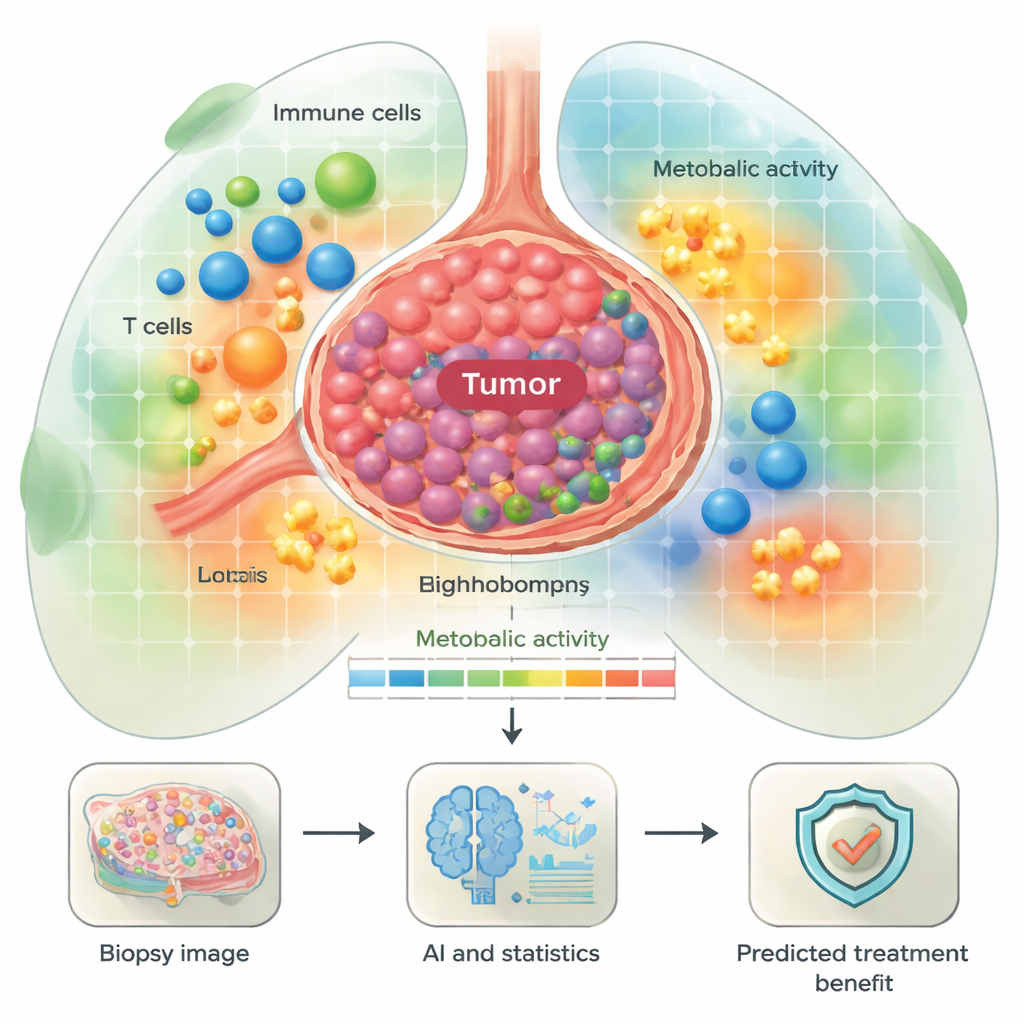
Enerji açısından aç tümörler ve bağışıklık çevreleri
Ana odaklardan biri metabolizmaydı — hücrelerin büyümek veya hastalıkla savaşmak için yakıt ürettikleri yollar. Araştırmacılar düşük aktiviteden oksidatif fosforilasyon ve glikoliz bakımından yüksek aktiviteye dek farklı seviyelerde ve türlerde enerji kullanımı gösteren “metabolik mahalleler” tanımladı. Hem tümör hücreleri hem de makrofajlar gibi bazı immün hücrelerin sık sık güçlü enerji üretim yolları gösterdiğini buldular. Bu desenlerin bir kısmı hasta sonuçlarıyla ilişkilendirildi. Örneğin, amino asitleri kullanmaya ve TCA döngüsünü çalıştırmaya yardımcı olan yollarda yüksek aktivite gösteren tümörler, immünoterapiden sonra erken relaps yaşayan hastalara daha sık aitti. Buna karşın, tümör içinde aktif enerji yollarına sahip bazı plazma hücreleri (antikor üreten B hücreleri), daha iyi sonuç alan hastalarda daha yaygın görüldü; bu da tüm enerjik hücrelerin zararlı olmadığını, bazılarının etkili anti-tümör bağışıklığı destekleyebileceğini düşündürüyor.
Tümör manzarasındaki iyi ve kötü bağışıklık oyuncuları
Basit bolluğun ötesinde, immün hücrelerin türü ve davranışı da önemliydi. Sitotoksik molekül granzyme B taşıyan makrofajlar, özellikle metabolik olarak düşük veya inaktif mahallelerde bulunduğunda daha kötü progresyonsuz sağkalımla güçlü şekilde ilişkilendirildi. Bu bölgeler, bağışıklık saldırısının zayıflatıldığı besin açısından fakir veya uykuda alanları temsil ediyor olabilir. Buna karşılık, tümör ile çevre doku arasındaki sınırda düzenleyici T hücreler (Treg) ve fibroblastların belirli düzenlenişleri daha iyi sonuçlarla ilişkilendirildi; bu durum, baskılayıcı hücrelerin derin tümöre nüfuz etmek yerine kenarlarda tutulduğu bir deseni yansıtıyor olabilir. Granülositler ile CD8 T hücreleri gibi farklı immün hücre oranları da yanıtla korelasyon gösterdi; bu da önemli olanın sadece toplam sayılar değil, bağışıklık dengesinin ve hücrelerin konumlanmasının olduğunun altını çiziyor.
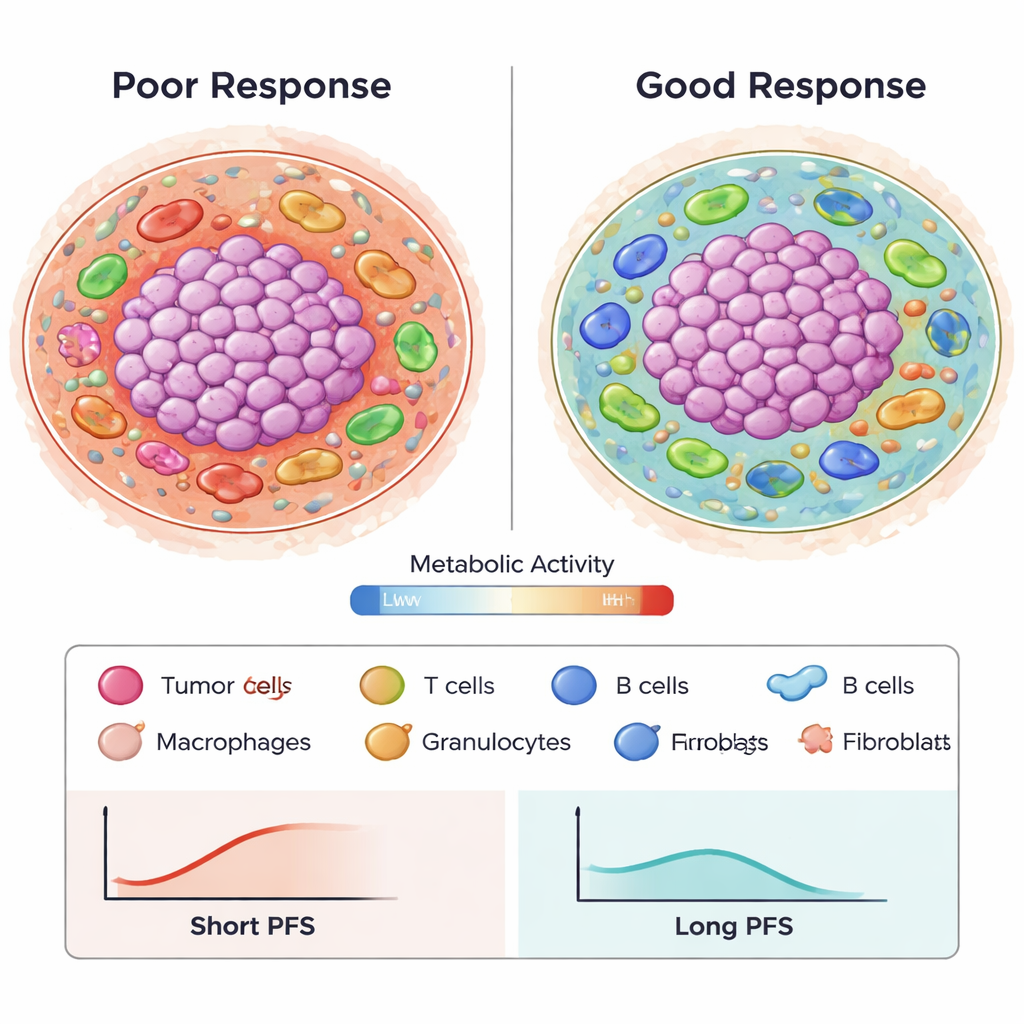
Karmaşık görüntülerden öngörücü desenlere
Hücre tiplerini, mesafelerini ve metabolik durumlarını tanımlayan bir milyonun üzerinde mekansal özellikten anlam çıkarmak için yazarlar gelişmiş bir özellik seçimi yöntemi (Stabl) ve sağkalım modelleme araçları kullandı. Metabolik olarak aktif tümör hücrelerinin makrofajlar ve T hücreleriyle nasıl etkileştiğini veya belirli immün hücre tiplerinin kan damarları ve fibroblastların yakınında nasıl kümelendiğini yansıtan 87 anahtar özellik belirlediler. Bu özellikleri Cox regresyon modellerinde kullanarak 24 ay boyunca progresyonsuz sağkalımı yaklaşık 0,8 AUC doğrulukla tahmin eden bir öngörücü kurdular; bu, daha önce yayınlanmış çalışmalarda PD-L1 boyaması veya tümör mutasyon yükü gibi geleneksel tek belirteçleri geride bırakıyordu. Önemli olarak, birkaç özellik iki bağımsız hasta kohortunda da yeniden üretilebilir bulundu; bu da desenlerin yalnızca rastgele gürültü olmadığını düşündürüyor.
Bu hastalar için ne anlama geliyor
Hastalar için ana mesaj şudur: bir akciğer tümöründe hücrelerin nerede yer aldığı ve nasıl enerji sağladığı, bazı hastaların immünoterapiye iyi yanıt vermesini, bazılarının vermemesini açıklamaya yardımcı olabilir. Bu çalışma, rutin bir biyopsiden elde edilen zengin mekansal ve metabolik bilgilerin yapay zeka ve istatistiksel modellemeyle birleştirilmesiyle, yarar veya direnç olasılığını gösteren imzaların ortaya çıkarılabileceğini gösteriyor. Çalışmanın daha büyük gruplarda ve tüm doku kesitlerinde doğrulanması gerekiyor olsa da, tedavi başlamadan önce hangi hastaların immünoterapiden kalıcı fayda görmeye daha yatkın olduğunu ve hangilerinin alternatif veya kombine stratejilere ihtiyaç duyabileceğini doktorlara söyleyebilecek gelecekteki testlere doğru bir yol haritası çiziyor.
Atıf: Monkman, J., Kilgallon, A., Lawler, C. et al. Metabolic characterization of tumor-immune interactions by multiplexed immunofluorescence reveals spatial mechanisms of immunotherapy response in non-small cell lung carcinoma (NSCLC). Nat Commun 17, 837 (2026). https://doi.org/10.1038/s41467-026-68633-8
Anahtar kelimeler: immünoterapi direnci, küçük hücre dışı akciğer kanseri, tümör mikroçevresi, mekansal biyoloji, kanser metabolizması