Clear Sky Science · tr
G9a aracılı H3K9me2, hücre döngüsüyle ilişkili genlerin epigenetik susturulması yoluyla bağırsak epitelyumunun rejenerasyonunu düzenler
Bağırsakların Kendi Kendini Tamir Etmesi Neden Önemli
Her gün, bağırsak yüzeyi zorlu koşullara maruz kalır: mide asidi, besin parçacıkları ve trilyonlarca mikrop. Buna rağmen bu doku sadece ayakta kalmaz, sürekli kendini onarır. Onarım sistemi bozulduğunda—radyoterapi sonrası, iltihabi bağırsak hastalığında veya şiddetli enfeksiyonlarda—insanlar ağrı, kanama ve hayati komplikasyonlarla karşılaşabilir. Bu çalışma, bağırsak hücrelerinin dinlenmeyi bırakıp yeniden inşa etmeye ne zaman başlayacaklarına karar vermelerine yardımcı olan gizli bir “anahtarı” ortaya koyuyor ve bağırsakların doğal onarım kapasitesini güçlendirebilecek yeni tedavilere işaretler sunuyor.
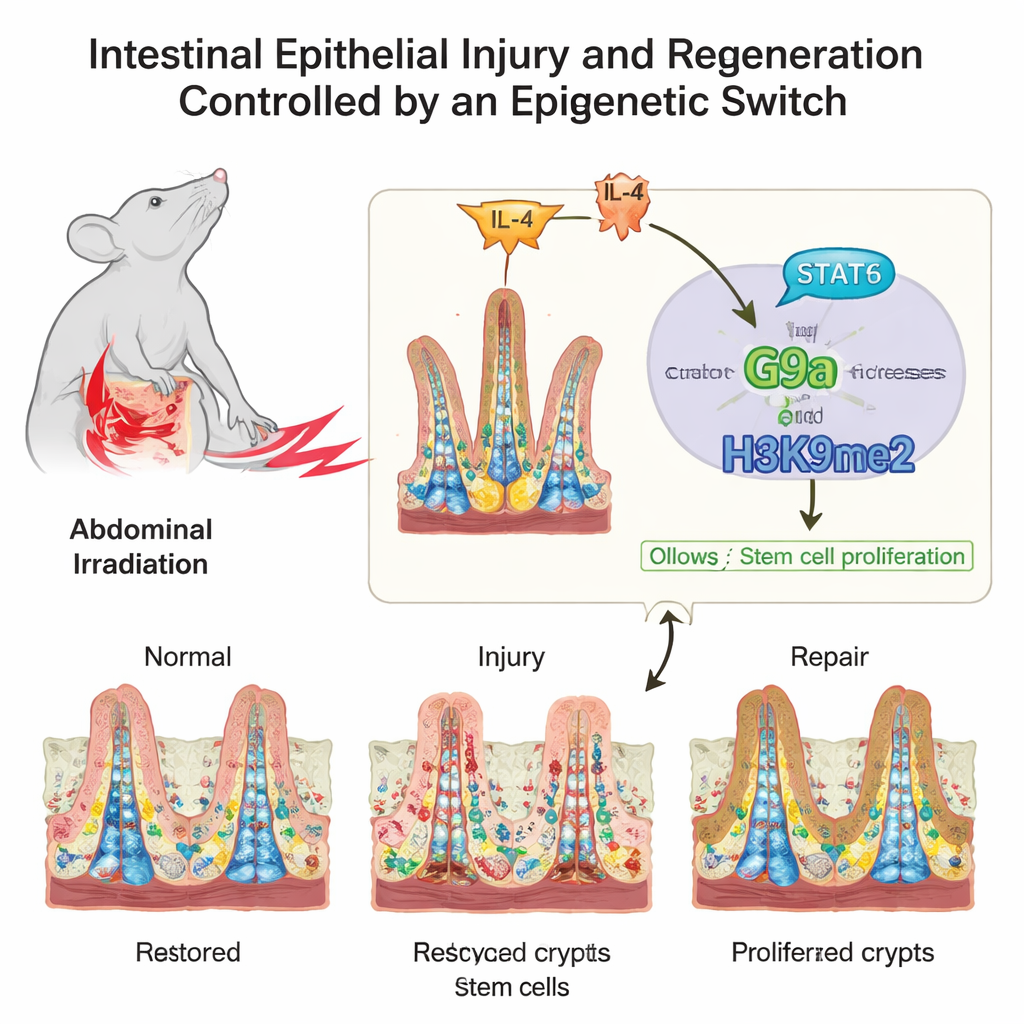
Sürekli Stres Altında İnce Bir Mimari
Bağırsak iç yüzeyi mikroskop altında bir peluş halı gibi görünür; parmak şeklindeki villuslar besinleri emer ve kök hücrelerin yaşadığı kript adı verilen cepler bulunur. Bu kök hücreler ve hızlı bölünen yavruları, düzenli yenilenme ile acil onarım arasında bir denge kurmak zorundadır. Yazarlar, DNA paketleyen proteinler olan histonlardaki kimyasal etiketlerin bu dengeyi nasıl etkilediğine odaklandı. Bu etiketler genlerin kendisini değiştirmez; daha çok birer dimmer anahtarı gibi davranır, bağırsak normal durumdan yaralanmaya ve yeniden sağlığa dönerken gen kümelerini açıp kapatır.
Hasarı ve İyileşmeyi İzleyen Bir Epigenetik İşaret
Araştırmacılar, kanser tedavisi sırasında bağırsak yaralanmasının yaygın bir nedeni olan ışınlanmaya maruz bırakılan farelerde, kök hücre açısından zengin kriptlerde birçok farklı histon işaretini taradılar. H3K9me2 olarak bilinen bir işaret, bağırsak yaralanmadan onarıma geçerken belirgin şekilde arttı. Bu işareti oluşturan enzim olan G9a proteini de aynı deseni izledi. Ekip daha sonra pelvik radyoterapi görmüş hastalardan ve Crohn hastalarından alınan insan örneklerini inceledi. Her iki durumda da bağırsak hücrelerinde daha yüksek H3K9me2 ve G9a seviyeleri doku onarımının daha iyi göstergeleriyle birlikteydi; bu da bu sistemin fareler ve insanlar arasında korunduğunu düşündürüyor.
Anahtar Bozulduğunda Onarım Nasıl Etkilenir
Bu işaretin sadece bir seyirci mi yoksa gerçekten iyileşmeyi tetikleyen unsur mu olduğunu test etmek için bilim insanları farelerde G9a’yı özel olarak bağırsak epitelinden çıkardılar veya etkinliğini bir ilaçla bloke ettiler. Her iki durumda da H3K9me2 seviyeleri düştü. Radyasyon veya kimyasal yaralanma sonrası bu fareler daha fazla kilo kaybetti, daha kısa ve daha fazla hasarlı bağırsaklara sahip oldu ve normal hayvanlara göre daha az rejeneratif kript ve kök hücre gösterdi. Kasıtlı bir yaralanma olmasa bile G9a eksikliğinin olduğu farelerin bağırsak örtüsü cılız görünüyordu: kriptler daha sığ, villuslar daha kısa ve kök hücrelerin ile onların özelleşmiş türevlerinin sayısı azalmıştı. Bu hücrelerden kültürde büyütülen küçük “mini‑bağırsaklar” da zayıf büyüdü; bu da bu moleküler sistemin bağırsak günlük yenilenmesinde merkezi olduğunu vurguluyor.
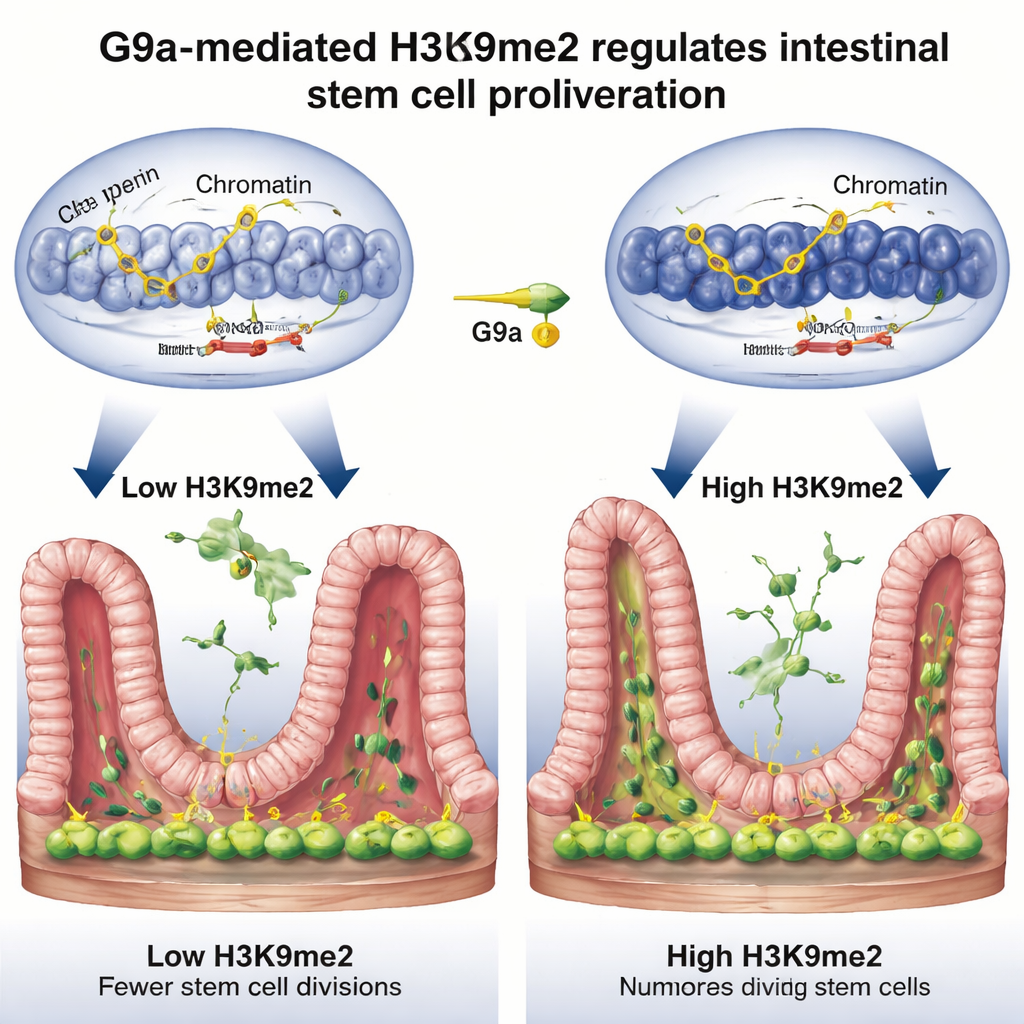
Hücre Bölünmesindeki Frenleri Serbest Bırakmak
Daha derine indiklerinde, ekip bu onarım anahtarının hangi genleri kontrol ettiğini sordu. Üç güçlü tüm‑genom yöntemi birleştirdiklerinde, G9a tarafından yerleştirilen H3K9me2’nin genellikle hücre döngüsünde fren görevi gören DNA bölgelerinde bulunduğunu tespit ettiler—Rb1cc1, Rb1, Cdkn1a ve Pten gibi genler hücre bölünmesini yavaşlatır veya durdurur. G9a eksik olduğunda, bu kimyasal işaret bu bölgelerden kayboldu, çevreleyen DNA açıldı ve bu fren genleri daha güçlü şekilde aktifleşti; bu da kök hücre proliferasyonunda yavaşlamaya yol açtı. Yaralanma sonrası normal onarım sırasında bu genlerde H3K9me2 seviyeleri yükseldi, aktiviteleri düştü ve kök hücreler daha serbestçe bölünerek örtüyü yeniden inşa edebildi. Özetle, G9a ve H3K9me2 doku yeniden büyüyene kadar geçici olarak “dur” sinyallerini susturur.
Bağışıklık Sinyallerinden Onarıma Uzanan Bir İşaret Zinciri
Bağırsak tek başına hareket etmez; sürekli olarak bağışıklık sisteminden gelen sinyalleri dinler. Araştırmacılar bu işte G9a’nın yukarısında çalışan bir sinyali izlediler. Yaralanma sonrası bağışıklık haberci molekülü IL‑4 seviyeleri arttı ve bu, bağırsak hücreleri içinde STAT6 adlı bir proteinin etkinleşmesini tetikledi. Etkinleşmiş STAT6 doğrudan G9a geninin kontrol bölgesine bağlandı ve üretimini artırdı. Bu, bir komuta zinciri yarattı: IL‑4 STAT6’yı aktifleştirir, STAT6 G9a’yı yükseltir ve G9a hücre döngüsü fren genlerini susturmak için H3K9me2 ekler; böylece kök hücreler genişleyip hasarlı örtüyü onarabilir.
Gelecekteki Tedaviler İçin Anlamı
Bir uzman olmayan için bu bulgular, bağırsak onarımının yalnızca genlerle değil, o genlerin ne zaman kullanılacağını hassas ayarlayan geri döndürülebilir kimyasal işaretlerle yönlendirildiğini gösteriyor. IL‑4–STAT6–G9a–H3K9me2 yolakları, kök hücre bölünmesindeki frenleri iyileşme için yeterince gevşeten sonra tekrar sıfırlanabilen dahili bir kontrol paneli gibi davranır. Gelecekte, bu yolu nazikçe güçlendiren terapiler—örneğin doğru zaman ve yerde G9a düzeylerini artıran ilaçlar veya gen temelli araçlar—radyasyon hasarından, iltihabi bağırsak hastalığı alevlenmelerinden veya bağırsak örtüsünü zedeleyen diğer durumlardan daha hızlı iyileşmeye yardımcı olabilirken, kontrolsüz hücre çoğalması risklerini en aza indirebilir.
Atıf: Chen, J., Shi, X., Zhou, X. et al. G9a-mediated H3K9me2 orchestrates intestinal epithelial regeneration through epigenetic silencing of cell cycle-related genes. Nat Commun 17, 1874 (2026). https://doi.org/10.1038/s41467-026-68626-7
Anahtar kelimeler: bağırsak rejenerasyonu, epigenetik, kök hücreler, histon metilasyonu, iltihabi bağırsak hastalığı