Clear Sky Science · tr
Pseudomonas aeruginosa’da çift işlevli quorum sensing sinyal sentezleyicileri DspII ve DspI virülans anahtarını koordine ediyor
Hastane Süper Bakterisinin Saldırı Stratejisini Nasıl Değiştirdiği
Pseudomonas aeruginosa, özellikle savunmasız hastalarda inatçı akciğer ve yara enfeksiyonlarına yol açabilen tanınmış bir hastane mikrobudur. Korunmuş, yavaş büyüyen bir topluluk olan biyofilm ile dokuya hızla saldıran, hareketli agresif biçim arasında geçiş yaparak hayatta kalır. Bu çalışma, bakterinin uzun süreli bir biyofilmden ne zaman çıkıp ani bir akut saldırı başlatmaya karar verdiğini ortaya koyarak gelecekteki tedaviler için potansiyel yeni zayıf noktalar gösteriyor.
Gizlenme ile Saldırma Arasındaki Mikrobiyal Yaşam
Birçok bakteriyel enfeksiyon aşamalı olarak ilerler. Erken dönemde serbest yüzen hücreler vücuda yayılır ve konak dokulara zarar veren güçlü silahlar kullanır. Daha sonra genellikle kateterler, akciğer dokusu veya yaralar gibi yüzeylere yapışarak kalın, sümüksü biyofilmlere yerleşirler. Bu topluluklarda hücreler, antibiyotikler ve bağışıklık savunmaları tarafından öldürülmeyi zorlaştıran koruyucu bir matriksle sarılır. Ancak biyofilm bir çıkmaz değildir. Hücreler ayrılabilir, hareketliliğini yeniden kazanabilir ve başka yerlerde yeni akut enfeksiyon turları başlatabilir. Bugüne dek Pseudomonas aeruginosa’nın kronik kalıcılıktan tekrar agresif hastalığa geçişi nasıl aktif şekilde koordine ettiği belirsizdi.
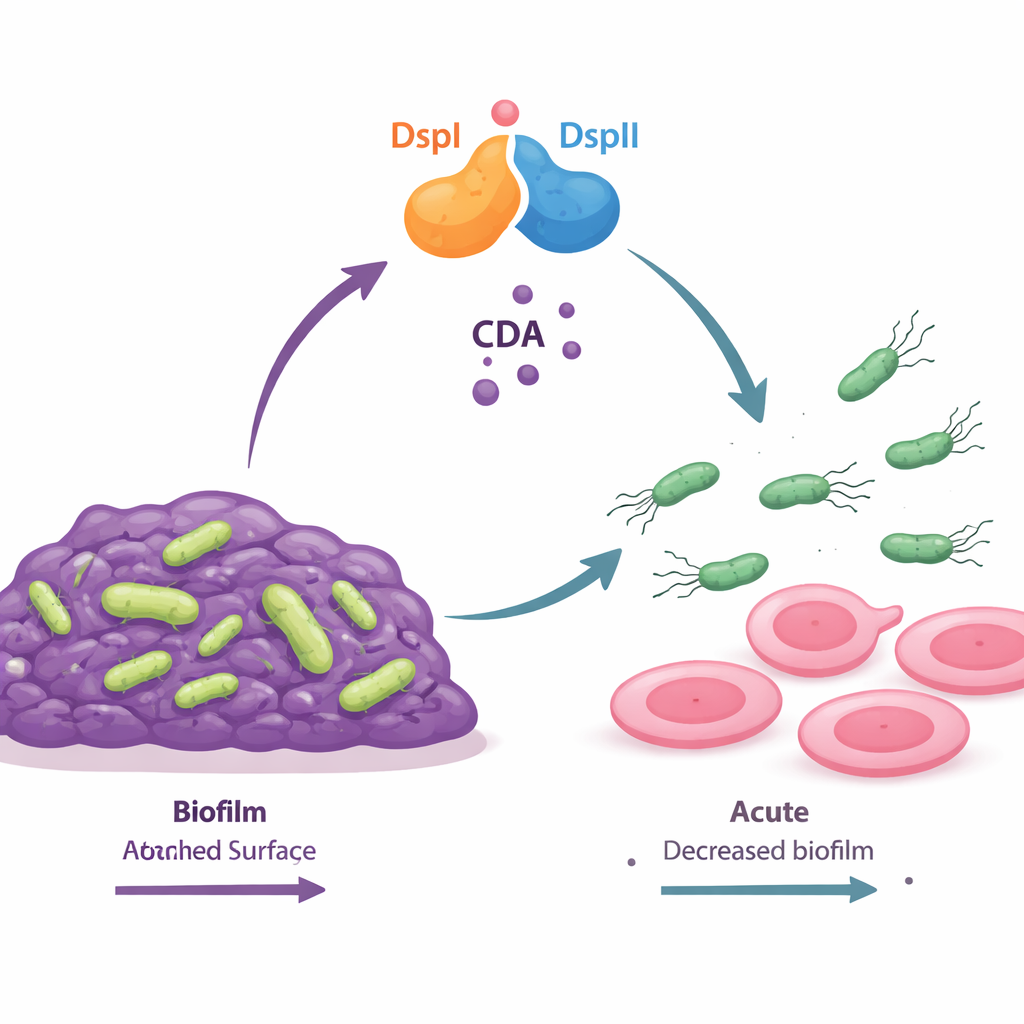
Kimyasal "Git" Sinyali Üreten İki Proteinlik Bir Anahtar
Yazarlar, DspI ve DspII adında iki bakteriyel proteinin moleküler bir anahtar gibi birlikte çalıştığını keşfettiler. Her ikisi de aynı genel enzim türüne ait olup bakteri genomunda yan yana yerleşmiş ve nüfus yoğunlaştıkça birlikte açığa çıkar. İkisi birleştiğinde cis-2-dekenoik asit (CDA) adlı küçük bir yağ asidi sinyali üretirler; bu, DSF sinyalleri olarak bilinen daha geniş bir iletişim molekülleri grubunun parçasıdır. DspI veya DspII eksik mutant bakteriler CDA üretemedi, olağandışı kalın biyofilm oluşturdu ve yüzeylerde sürünme yeteneklerini kaybetti. Sadece her iki protein birlikte geri getirildiğinde hücreler normal sinyal üretimini, biyofilm çözülmesini ve hareketliliği geri kazandı; bu da iki enzimin birbirine bağımlı bir takım olarak işlediğini gösteriyor.
Kimyasal Sinyalden Hareket ve Kaçışa
CDA tek başına hareket etmez; bakterinin iç devrelerine bağlanır. Araştırma ekibi, CDA’nın başka bir haberci molekül olan siklik di-GMP düzeylerini düşürdüğünü ve bunu bu haberciyi parçalayan RbdA adlı özel bir enzimin aktivitesini artırarak yaptığını gösterdi. Yüksek siklik di-GMP normalde yapışkan matriks üretimini uyararak biyofilm kurulumunu teşvik eder ve yüzgeç benzeri flagellaları baskılar. CDA varlığında siklik di-GMP düzeyleri düşer, FleQ adlı bir düzenleyici vites değiştirir, yapışkan şeker üretimi azalır ve flagellalar uzayıp güçlenir. Sonuç olarak biyofiller gevşer ve hücreler uzaklaşma yeteneğini yeniden kazanarak yeni bölgeleri kolonize eder.
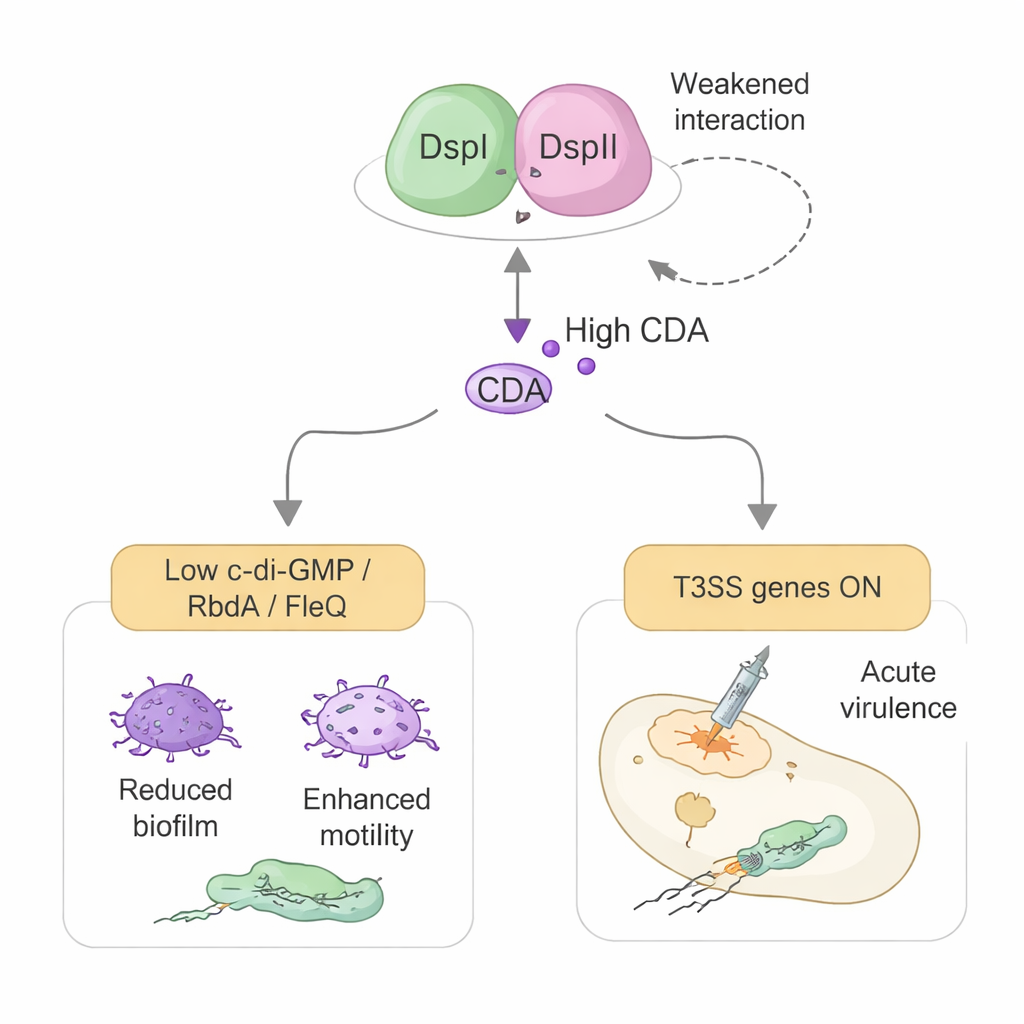
Bakteriyel Silah Sisteminin Yeniden Kablosu
Çalışma ayrıca DspI ve DspII için kimyanın ötesinde beklenmedik ikinci bir rol ortaya koyuyor. Aynı protein çifti, toksinleri doğrudan konak hücrelere enjekte etmek için kullanılan enjektör benzeri tip III salgılama sistemi (T3SS) adlı bakterinin silahını da açmaya yardımcı oluyor. Bu etki CDA aracılığıyla değil, genetik anahtarların doğrudan kontrolü yoluyla çalışır. DspI ve DspII, normalde T3SS protein üretimini kapatan iki küçük düzenleyici RNA olan RsmY ve RsmZ'nin üretimini azaltır. Bunu, bir RNA’nın DNA kontrol bölgesine bağlanarak ve GacA adlı ana düzenleyici bir proteinle fiziksel etkileşime girerek yaparlar. RsmY ve RsmZ baskılandığında, aşağı doğru aktivatör RsmA serbest kalır ve T3SS ile onun ana denetleyicisi ExsA genleri açılarak hücre kültüründe sitotoksisiteyi artırır ve bir böcek enfeksiyon modelinde öldürücülüğü yükseltir.
Kendini Ayarlayan Bir Sistem ve İlaç Hedefleri
Zekice bir biçimde, DspI–DspII ortaklığının gücü ve virülans üzerindeki kontrolü kendisi CDA düzeyleriyle ayarlanır. Düşük konsantrasyonlarda—biyofilmden yeni ayrılan hücrelerde beklenen seviyeler gibi—CDA iki proteinin etkileşimini sıkılaştırır ve daha fazla sinyal üretimi ile T3SS aktivasyonunu teşvik eder. Yoğun biyofiller içinde yüksek konsantrasyonlarda ise CDA etkileşimi zayıflatır ve DNA üzerindeki tutuşlarını azaltır; bu da kalan hücrelerde daha fazla sinyal sentezini ve maliyetli silah üretimini sınırlar. Bu çift rol, DspI–DspII kompleksini nüfus büyüklüğünü, biyofilm kaçışını ve akut virülansı birbirine bağlayan merkezi bir düğüm haline getirir. Kompleksi bozmanın hem sinyal üretimini hem de toksin sisteminin aktivasyonunu engelleyebileceği göz önüne alındığında, Pseudomonas’ı daha az zararlı, kronik bir durumda kilitleyip tehlikeli alevlenmeleri önleyebilecek gelecekteki ilaçlar için çekici bir hedef sunar.
Atıf: Huang, J., Zhou, T., Zhou, X. et al. Dual-functional quorum sensing signal synthases DspII and DspI coordinate virulence switch in Pseudomonas aeruginosa. Nat Commun 17, 1926 (2026). https://doi.org/10.1038/s41467-026-68622-x
Anahtar kelimeler: Pseudomonas aeruginosa, biyofilm disperzasyonu, quorum sensing, virülans anahtarı, cis-2-dekenoik asit