Clear Sky Science · tr
Laktamaz evriminde etkinlik‑stabilite ödünleşiminin dinamik imzası
Antibiyotik direnci açısından neden önemli
Antibiyotik direnci sıklıkla bir kara kutu gibi görünür: bakteriler “bir şekilde” değişir ve ilaçlar işe yaramaz hale gelir. Bu çalışma, dünyanın en tanınmış direnç enzimlerinden biri olan TEM‑1 β‑laktamaz için o kara kutuyu açıyor; bu enzim bakterilerin penisilin benzeri antibiyotikleri parçalamasına yardım eder. Enzimin evrilip daha yeni ilaçları hedeflediğinde şeklinin ve hareketlerinin nasıl değiştiğini izleyerek, aktiviteyi artıran mutasyonların neden genellikle stabiliteyi zayıflattığını ve evrimin her ikisi arasında dengeyi nasıl akıllıca kurduğunu ortaya koyuyor.
Penisilini yenenden daha geniş spektrumlu bozana
TEM‑1 başlangıçta daha eski penisilin antibiyotikleri parçalamada olağanüstü olsa da, sefotaksim gibi daha yeni, hacimli ilaçlarla başa çıkmada zayıftır. Birçok klinik izolde, G238S adı verilen tek bir önemli mutasyon enzimin aktif bölgesinin, yani antibiyotiklerin kesildiği cebin yakınında ortaya çıkar. Bu mutasyon, enzimin sefotaksimi yok etme yeteneğini dramatik şekilde artırırken, özgün penisilin‑yıkım işini yalnızca ılımlı şekilde azaltır. Yazarlar, G238S’in cebin yalnızca genişlettiğini göstermiyor; çevresindeki birkaç loop ve heliksin hareket etme biçimini yeniden düzenleyerek hacimli ilaçları daha iyi ağırlayan yeni bir işlevsel konformasyon yaratıyor.
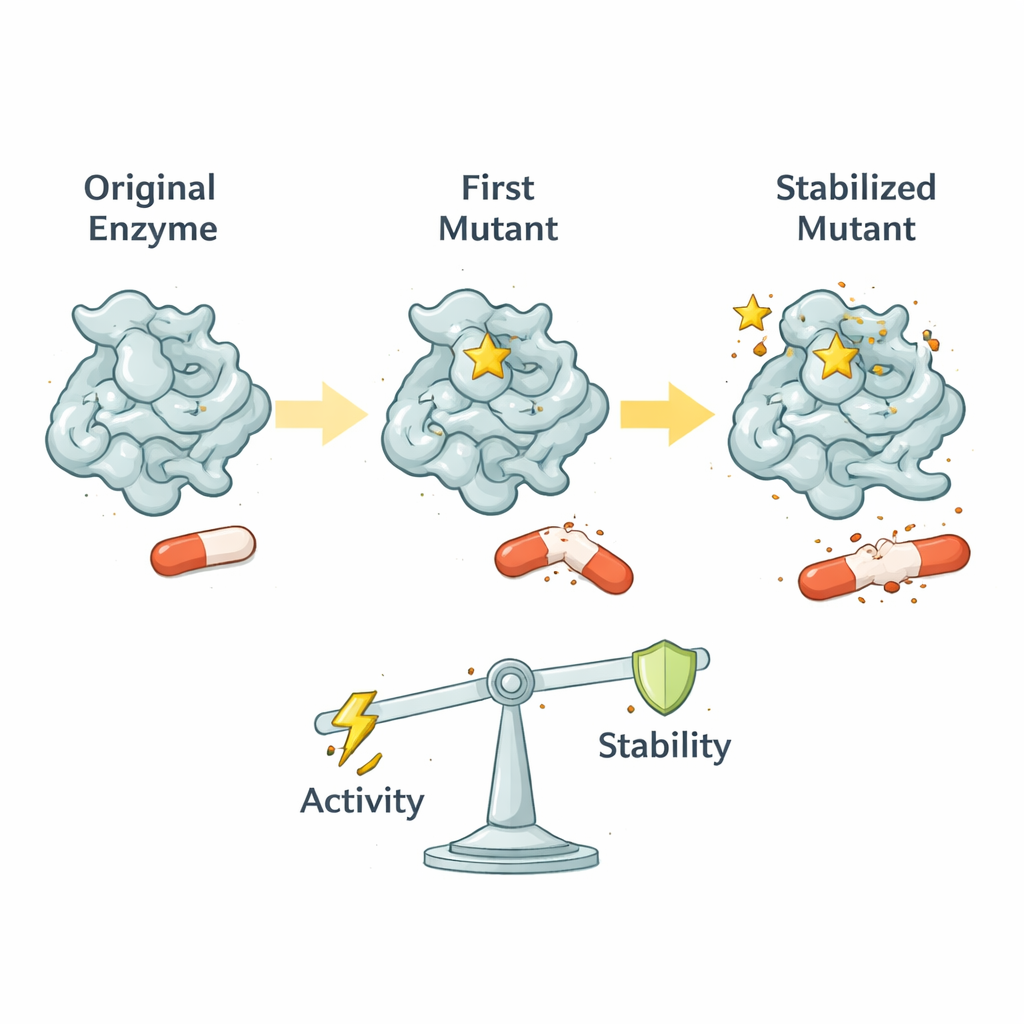
Evrimsel bir ayar düğmesi olarak protein hareketi
Gelişmiş nükleer manyetik rezonans (NMR) tekniklerini kullanarak araştırmacılar, TEM‑1’in farklı bölümlerinin trilyonda bir ila binde bir saniye arasındaki zaman ölçeklerinde nasıl hareket ettiğini ölçtüler. Vahşi tip TEM‑1 oldukça rijittir; bu da özgün substratlarını verimli şekilde işlemesine yardımcı olur. G238S bu hızlı rijitliğin çoğunu korur ama aktif bölgenin birçok duvarında daha yavaş, dikkatlice ayarlanmış hareketler getirir. Bu hareketler, enzimin kimyasıyla eşzamanlı kalacak kadar hızlı ama kritik katalitik kalıntıları bozacak kadar vahşi değildir. Sonuç, bir “optimize edilmiş esneklik penceresi”dir: sefotaksimi için cebi açmaya yetecek kadar hareket, aynı zamanda çekirdek kimya makinelerini doğru hizada tutacak kadar sabitlik.
Tek bir şekli seçmek yerine iki şekil arasında denge kurmak
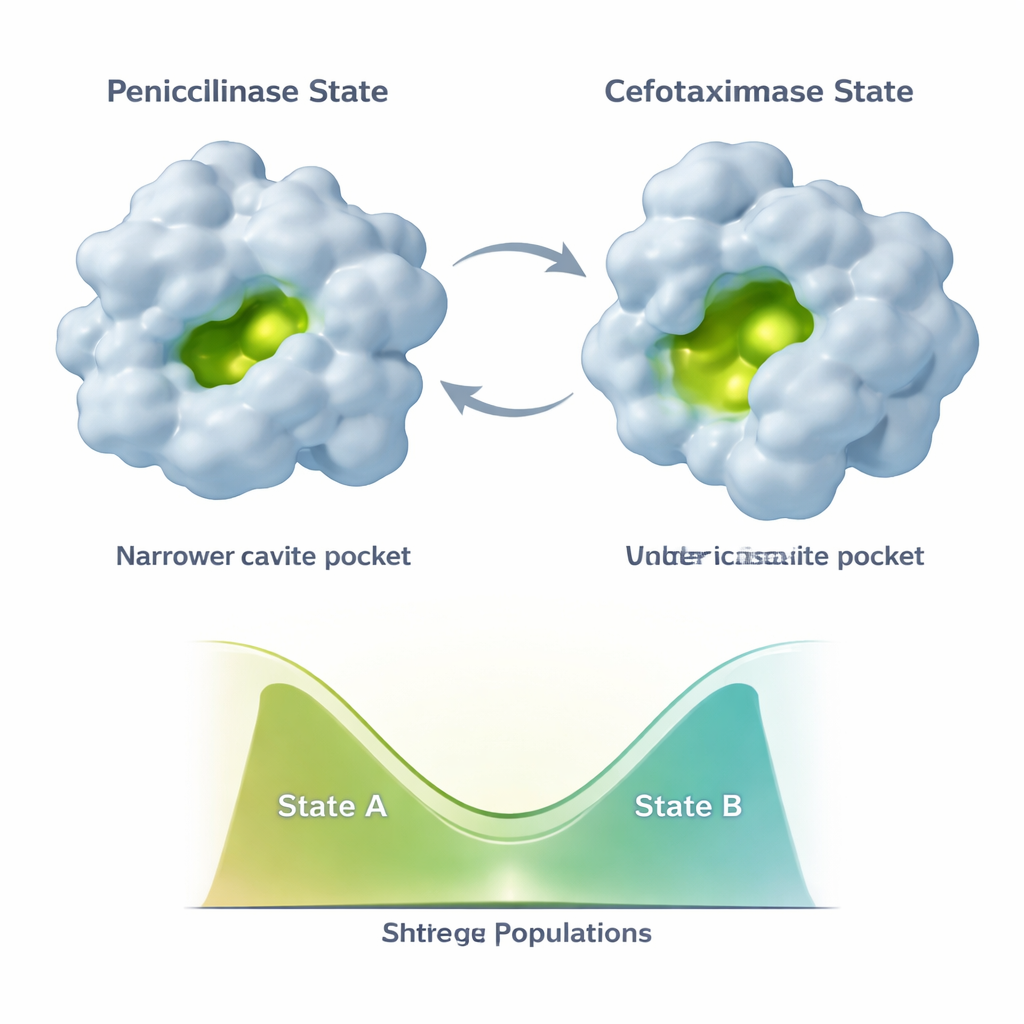
Evrim TEM‑1’i tek bir yeni şekle dondurmaz. Bunun yerine enzim en az iki ana konformasyonu örnekler: orijinal yapıya benzeyen bir “penisilinas” durumu ve yeni ilaçlara daha uygun daha açık bir “sefotaksimase” durumu. Daha sonra ortaya çıkan E104K ve A42G gibi ek mutasyonlar ince bir etki yapar. Yeni, sefotaksimase‑dostu şekli basitçe daha stabil hale getirmek yerine, iki durumun karışımını yeniden dengelerler. NMR verileri, aktif bölgenin farklı parçalarının ve destekleyen iskelenin bu iki durumlu süreklikte popülasyonlarını bağımsız olarak kaydırabileceğini gösterir. Bu, her biri penisilina benzer ve sefotaksime benzer konformasyonların farklı karışımlarına ve dolayısıyla farklı katalitik profillere sahip kombinatoryal bir enzim varyantları setine yol açar.
Gizli zayıf noktalar ve uzak mesafe onarımları
Aktiviteyi artıran mutasyonlar genellikle gizli bir maliyet taşır: proteini daha az stabil hale getirirler. Ekip, yalnızca tam açılmaya bakmak yerine, hidrojen–döteryum değişimlerini kütle spektrometrisiyle kullanarak kısa segmentler düzeyinde yerel stabiliteyi haritaladı. G238S yalnızca yakın çevredeki loop’ları değil, aynı zamanda yapısal bir omurga oluşturan uzak heliksleri ve yaprak bölgelerini de destabilize etti. Bu bölgelerin bazıları, proteinin çekirdeğinde nadiren ziyaret edilen ve küçük molekülleri bağlayıp aktiviteyi azaltabilen ‘‘kriptik’’ bir allosterik cebiyle örtüşür. G238S bu cebi açmayı kolaylaştırır; fiilen enzime hafif bir kendi kendini baskılama özelliği inşa eder. Daha sonraki mutasyonlar, özellikle A42G, bu zayıflamış omurga ağını güçlendirir; üç etkileşen heliksin etrafında yerel stabiliteyi iyileştirirken faydalı aktif‑bölge dinamiklerini kaldırmaz. Başka bir deyişle, evrim orijinal yeniliği geri almak yerine uzak yapısal zayıf noktaları yamalar.
Çalışmanın evrimin stratejisi hakkında açığa çıkardıkları
Sıradan bir okura göre temel mesaj şudur: TEM‑1 gibi proteinler direnci basit bir açık‑kapalı anahtarla kazanmaz. Her mutasyon, enzimin nasıl nefes alıp verdiğini, esnediğini ve farklı çalışma pozları arasında zamanını nasıl paylaştırdığını hafifçe yeniden şekillendirir. G238S yeni bir işe—daha yeni antibiyotikleri parçalamaya—kapıyı açar ama aynı zamanda yerel kırılganlıklar ve kısmen kendi kendini baskılayan bir durum yaratır. İkincil mutasyonlar dikkatli takviyeler gibi davranarak iskelenin stabilitesini artırır ve eski ile yeni konformasyonlar arasındaki dengeyi ince ayarlar, böylece enzim hem aktif hem de dayanıklı kalabilir. Hareketlerin ve yerel zayıflıkların statik yapı kadar önemli olduğu bu dinamik evrim görüşü, gelecekteki antibiyotiklerin ve enzimleri hedef alan ilaçların tasarımına rehberlik edebilir—bakterilerin ustaca atlatmasını daha zorlaştıracak yaklaşımlar geliştirilebilir.
Atıf: Arcia, E., Keramisanou, D., Jacobs, L.M.C. et al. Dynamic signature of activity-stability tradeoff in lactamase evolution. Nat Commun 17, 1884 (2026). https://doi.org/10.1038/s41467-026-68620-z
Anahtar kelimeler: antibiyotik direnci, beta‑laktamaz, protein evrimi, enzim dinamikleri, protein stabilitesi