Clear Sky Science · tr
İki adımlı isonitril biyosentezi için yüksek dinamik mononükleer non‑heme demir enzimi
Bakteriler Egzotik Kimyasal Araçları Nasıl İnşa Ediyor
Isonitriller küçük ama güçlü kimyasal gruplardır; çok yönlü bir araç kutusu gibidirler: metallere tutunabilir, çeşitli tepkimelere girebilir ve sıklıkla güçlü doğal antibiyotiklerin ve toksinlerin “savaş başı” rolünü üstlenirler. Tüberküloz patojeni Mycobacterium tuberculosis dahil bazı hastalık yapıcı bakteriler, konakçılarından metal çalmak için yağlı moleküllere isonitril eklerler. Bu makale, Rv0097 adındaki bir enzimin bu olağandışı zorlu kimyayı iki dikkatle kurgulanmış adımda nasıl gerçekleştirdiğini inceliyor.
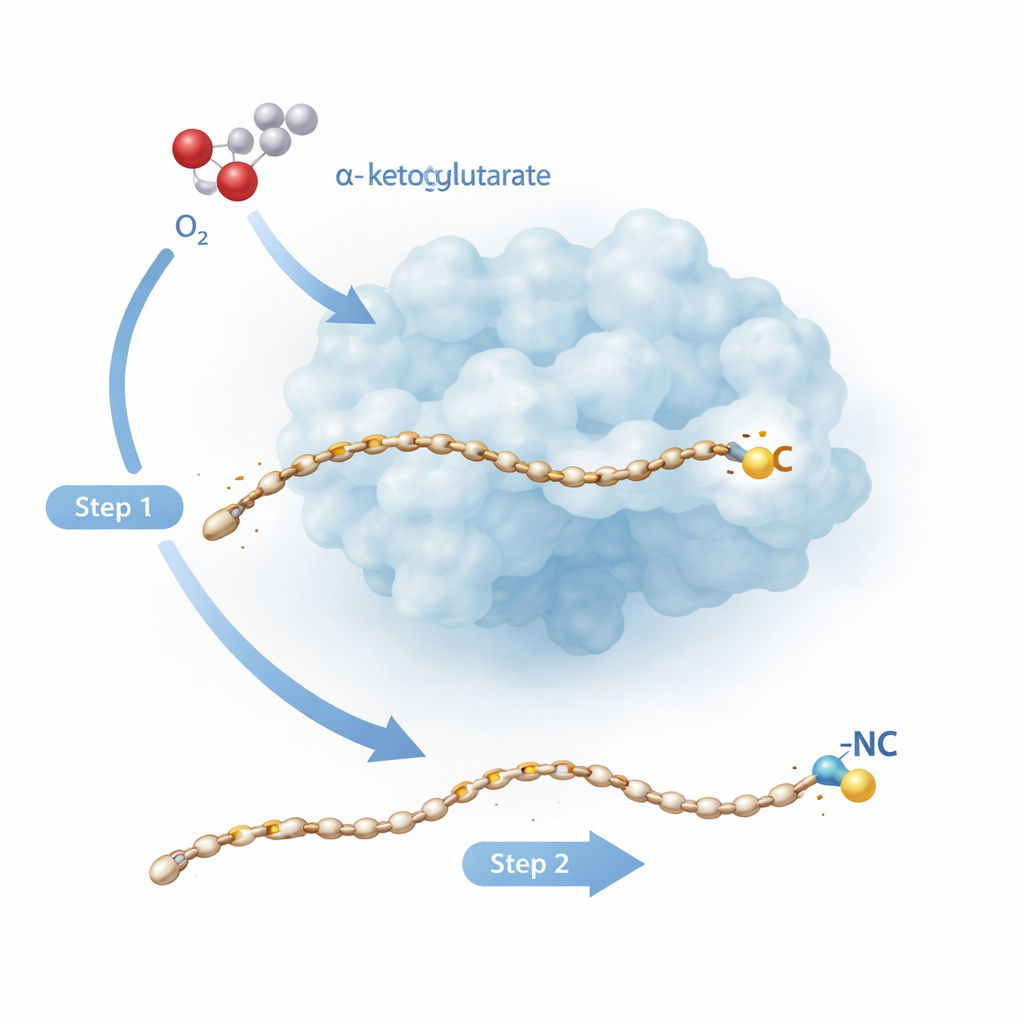
İki Aşamalı Moleküler Dönüşüm
Rv0097, genellikle bir molekülde tek bir noktaya oksijen eklemek gibi daha basit görevleri gerçekleştiren geniş bir demir‑bağımlı enzim ailesine aittir. Buradaki görev daha zordur: “glisil–yağ asidi” yapı taşından başlarken enzim, her iki ana atomu—karbon ve nitrojeni—aynı küçük glisin parçasından sağlayarak tamamen yeni bir isonitril grubunu oluşturmalıdır. İlgili bir enzim olan ScoE üzerinde yapılan önceki çalışmalar bunun tek adımda yapılamayacağını öne sürdü. Bunun yerine, α‑ketoglutarat adlı yardımcı molekülün parçalanıp havadan oksijenle birleşmesiyle oluşan bir demir–oksijen türü tarafından her biri beslenen iki ayrı reaksiyon “yarı çevrimi” gerekir. Yeni çalışma, tüberküloz enzimi Rv0097’ye yönelerek, aynı substrat üzerinde bu iki radikal adımın nasıl kontrol kaybı yaşanmadan peş peşe yürütülebildiğini atomik çözünürlükte izliyor.
Enzimi İşbaşındayken Dondurmak
X‑ışını kristalografisi kullanılarak araştırmacılar Rv0097’nin farklı durumlarını gösteren on altı yüksek çözünürlüklü anlık görüntü yakaladı: boş halde, yağlı substratına (on karbonlu CADA adlı molekül) bağlı halde, α‑ketoglutarat yardımcıya bağlı halde ve geçici reaksiyon ara ürünlerini taklit eden kombinasyonlarda. Bu yapılar Rv0097’nin bölünmüş bir kişiliğe sahip olduğunu gösteriyor. Dinlenme halinde aktif bölgesi büyük ölçüde kapalıdır; uzun yağlı kuyruk cebini kuru ve hidrofobik bağlanmaya hazır tutan anahtar bir amino asit (fenilalanin 102) iki konum arasında dönmektedir. CADA bağlandığında bu kalıp tek bir konuma sabitlenir ve substratın polar “başı” yüklü yan zincirlerle sabitlenirken yağlı kuyruğu dar bir tünele yerleşir. Bu kapı işlevi gören kalıp rezidülerinin (F102 ve yakınındaki glisin G204) mutasyonu ya cebi bloke eder ya da çok fazla suyun girmesine izin verir; bu da aktivitenin keskin biçimde azalmasına ve enzimin tercih ettiği zincir uzunluklarının değişmesine yol açar.
Hareketli Kapaklar ve Dinamik Döngüler
Substrat cebinin ötesinde Rv0097, hareket eden kapıları olan küçük bir makine gibi davranır. Ekip, iki kapak benzeri bölgenin aktif bölge üzerinde açılıp kapanarak ayrıldığı veya bir araya geldiği “açık” ve “kapalı” konformasyonlar gözlemledi. Açılma demir merkezini açığa çıkarır ve α‑ketoglutarat ile substratın girmesi için bir yol oluşturur; kapanma ise reaksiyon ilerlerken kimyayı çevredeki sudan korur. Histidin ve arginin taşıyan His döngüsü ve Arg döngüsü adı verilen iki esnek yüzey döngüsü ek bir kapı görevi görür. Bazı yapılarda bu döngüler içe doğru sallanarak arginin rezidüsünün α‑ketoglutaratı yakalamasına izin verir; diğerlerinde dışa doğru sallanarak harcanmış yardımcı parçacıkların (succinat ve karbondioksit) çıkabileceği ve ikinci adım için taze α‑ketoglutaratın girebileceği yan bir kanalı oluşturuyor gibi görünür—tüm bunlar substrat kaynaklı ara ürün yerinde sıkıca tutulurken gerçekleşir.
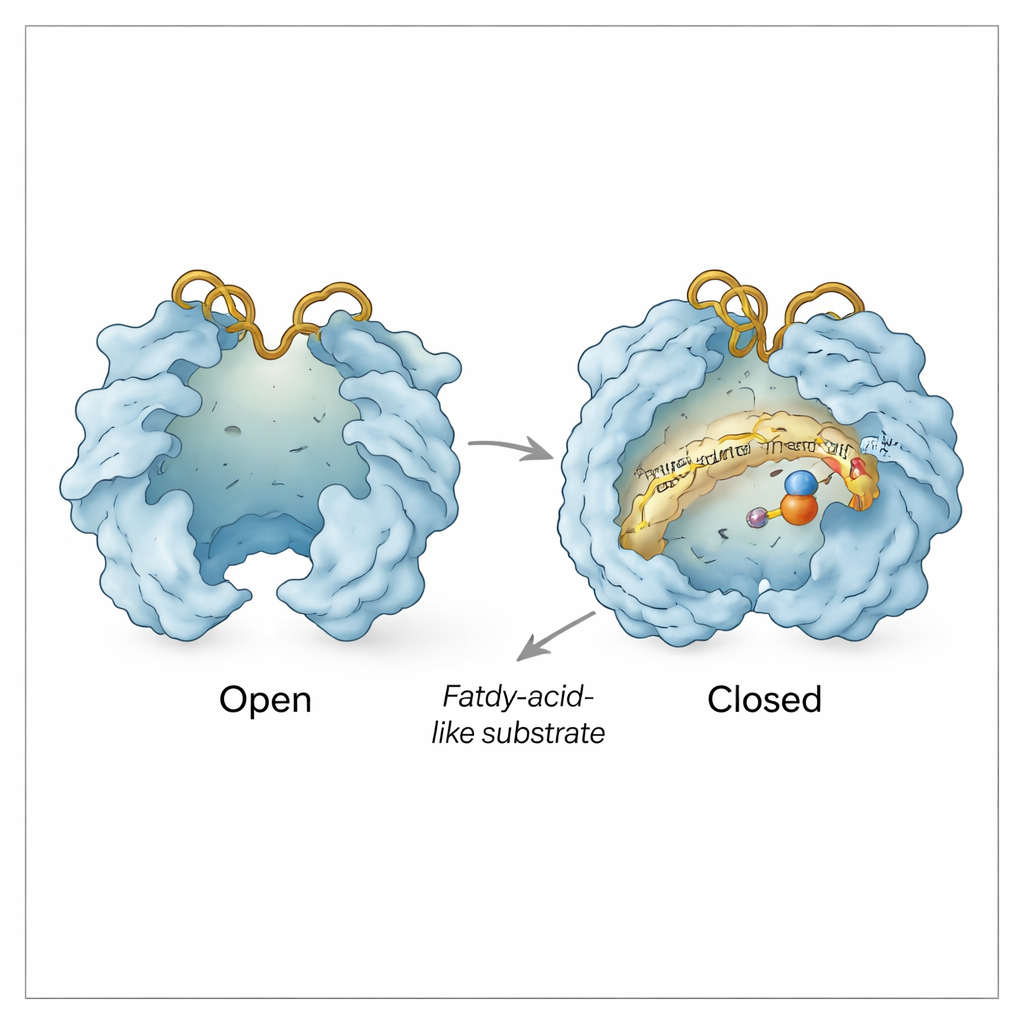
Kırılgan Bir Ara Ürünü Korumak
Biyokimyasal deneyler bu yapısal resmi destekliyor. Reaksiyonun ilk yarısı CADA’yı hızla parçalanabilecek yüksek derecede reaktif bir imine ara ürününe dönüştürür. Yazarlar, parçalanma ürününü kimyasal olarak kapanıstırarak, söz konusu ara ürünün çoğunun yalnızca enzim hâlâ mevcutken tespit edildiğini gösteriyor; bu da iki yarı reaksiyon arasında ara ürünün enzimin içinde bağlı ve korunmuş kaldığını ima ediyor. Yapılar bunun nasıl olduğunu açıklıyor: His ve Arg döngülerinin hafif yeniden konumlanmaları ve yakın rezidülerin küçük kaymaları, ara ürünü korunaklı bir boşluğa mühürlerken α‑ketoglutarat, succinat ve karbondioksit gibi küçük moleküllerin kontrollü kanallar aracılığıyla değiş tokuşuna izin veriyor gibi görünüyor.
Bu Neden TB ve Ötesi İçin Önemli
Bu bulgular birlikte Rv0097’yi aynı substrat üzerinde art arda demir‑temelli kimya kullanan, son derece dinamik tek proteinlik bir üretim hattı olarak ortaya koyuyor; tehlikeli bir ara ürünü asla serbest bırakmıyor. Tüberküloz bakterileri için bu hassasiyet, vücut içinde gerekli metalleri elde etmelerine yardımcı olan isonitril‑süslü moleküllerin üretilmesini destekler ve genetik çalışmalar bu yolun enfeksiyon sırasında hayatta kalmaları için önemli olduğunu gösteriyor. Kimyagerler ve ilâç tasarımcılar için çalışma, benzer enzimleri yeni isonitril içeren bileşikler yapmak üzere mühendislik etme yolunda bir plan sunuyor ve Rv0097’nin hareket eden kapakları ile kapılarını hedef almanın yeni antibiyotikler geliştirmek için bir yol olabileceğini düşündürüyor.
Atıf: Ye, N., Del Rio Flores, A., Zhang, W. et al. A highly dynamic mononuclear non-heme iron enzyme for the two-step isonitrile biosynthesis. Nat Commun 17, 2034 (2026). https://doi.org/10.1038/s41467-026-68588-w
Anahtar kelimeler: isonitril biyosentezi, non‑heme demir enzimi, Mycobacterium tuberculosis, enzim dinamikleri, metal şelatlayıcı doğal ürünler