Clear Sky Science · tr
Demir homeostazının bozulması pankreas kanserini geri döndürülemez elektroperforasyona duyarlı hale getiriyor
Ölümcül Bir Kana Karşı Elektrik ve Demiri Kullanmak
Pankreas kanseri tedavisi en zor kanserlerden biridir ve agresif lokal tedaviler bile sıklıkla tekrarını durduramaz. Bu çalışma, mevcut bir prosedürü — tümörleri kısa, güçlü elektrik darbeleriyle öldüren geri döndürülemez elektroperforasyonu — daha iyi ve daha güvenli hale getirmenin yeni bir yolunu araştırıyor. Kanser hücrelerinin demiri nasıl kullandıklarını kurnazca bozarak, araştırmacılar hayatta kalan hücreleri yıkıcı bir hücre ölümü biçimine itebileceklerini gösteriyorlar; bu da tümörün yeniden ortaya çıkma olasılığını azaltabilir.
Neden Elektrik Darbeleri Tek Başına Yeterli Değil
Geri döndürülemez elektroperforasyon (GEP), kanserin içine veya etrafına ince elektrotlar yerleştirip hızlı, yüksek voltajlı darbeler vererek tümörleri tedavi eder. Bu darbeler hücre zarlarında kalıcı delikler açar, birçok kanser hücresini öldürür ve bağışıklık yanıtını harekete geçirir. Ancak elektrik alanı tamamen homojen değildir. Biraz daha zayıf darbeler alan alanlar bazı kanser hücrelerini canlı bırakabilir ve bu hayatta kalanlar yeni bir tümörü başlatabilir. Ekip, subletal (ölümcül olmayan) bir elektrik alanına maruz kalan pankreas kanseri hücrelerini ve fare tümörlerini yakından incelediğinde, bunların demir kaynaklı bir süreç olan ferroptozla ölmek yerine geniş bir antioksidan savunma programını açtıklarını buldu. Demirle ilgili hasarı nötralize etmeye yardımcı olanlar dahil kritik koruyucu genler yükseltilmişti; bu da hücrelerin stresi atlatıp toparlanmasına izin verdi.
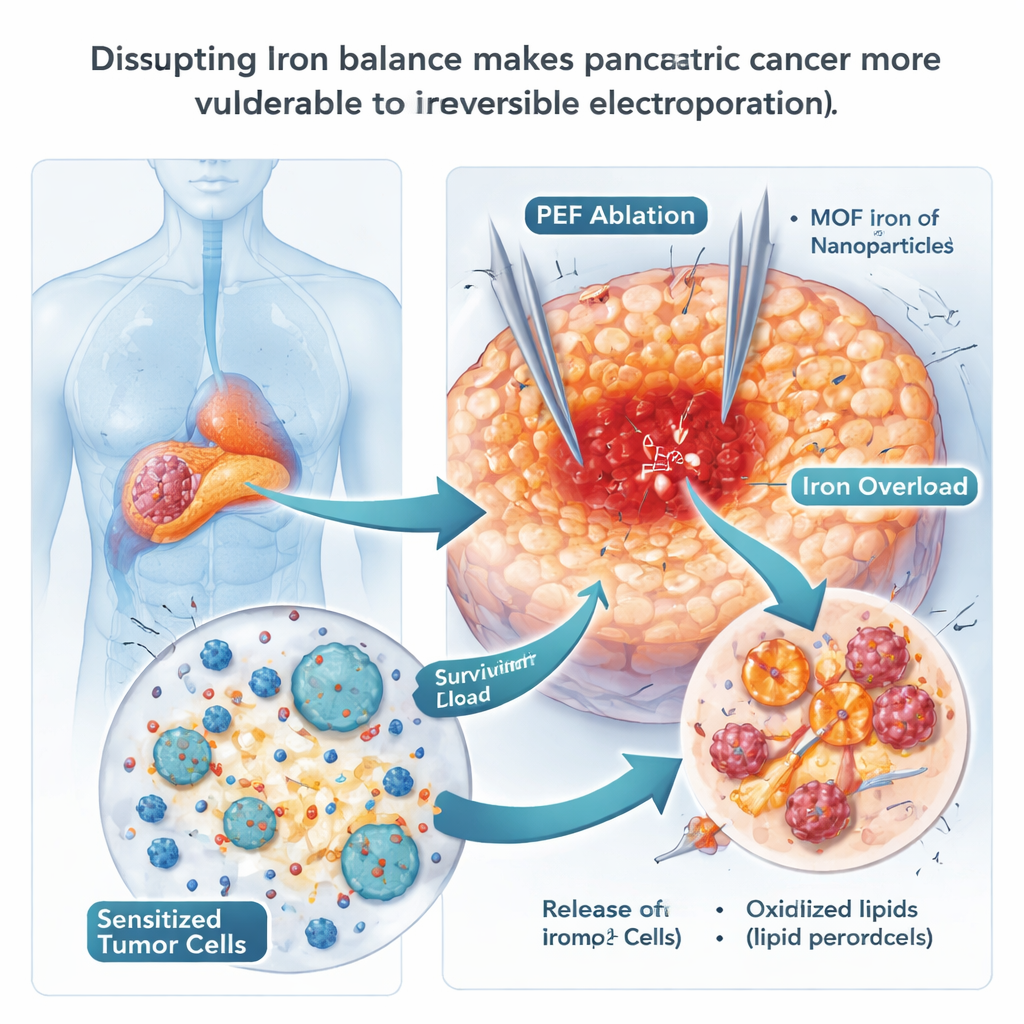
Hücreleri Yok Oluşa İtmek İçin Demir Nanopartikülleri Kullanmak
Ferroptozun demire bağlı olması nedeniyle, bilim insanları demir bakımından zengin nanopartiküllerin kanser hücrelerini eşiğin ötesine zorlayıp zorlayamayacağını test ettiler. Hücrelerin asidik kompartmanlarında hızla demir salan özel tasarlanmış metal-organik kafes parçacıkları (MOF-Fe) kullandılar. Plaklarda, bu parçacıkları alan pankreas kanseri hücreleri serbest demir ve zar lipitlerinin oksidasyonunu biriktirdi — ferroptozun klasik işaretleri — ve çok daha az koloni oluşturdu. Farelerde, MOF-Fe ile GEP kombinasyonu tek başına uygulanan her iki tedaviden daha uzun süre tümör yeniden büyümesini geciktirdi ve tümörler daha fazla oksidatif hasar belirtisi gösterdi. Ancak bu fayda geçiciydi: yaklaşık üç hafta sonra tümörler yeniden büyümeye başladı; bu da kanserin demir yüklemesine adapte olmanın bir yolunu bulduğunu gösteriyordu.
Hücresel Demir 'Kasa'sına Hedef Taşıma
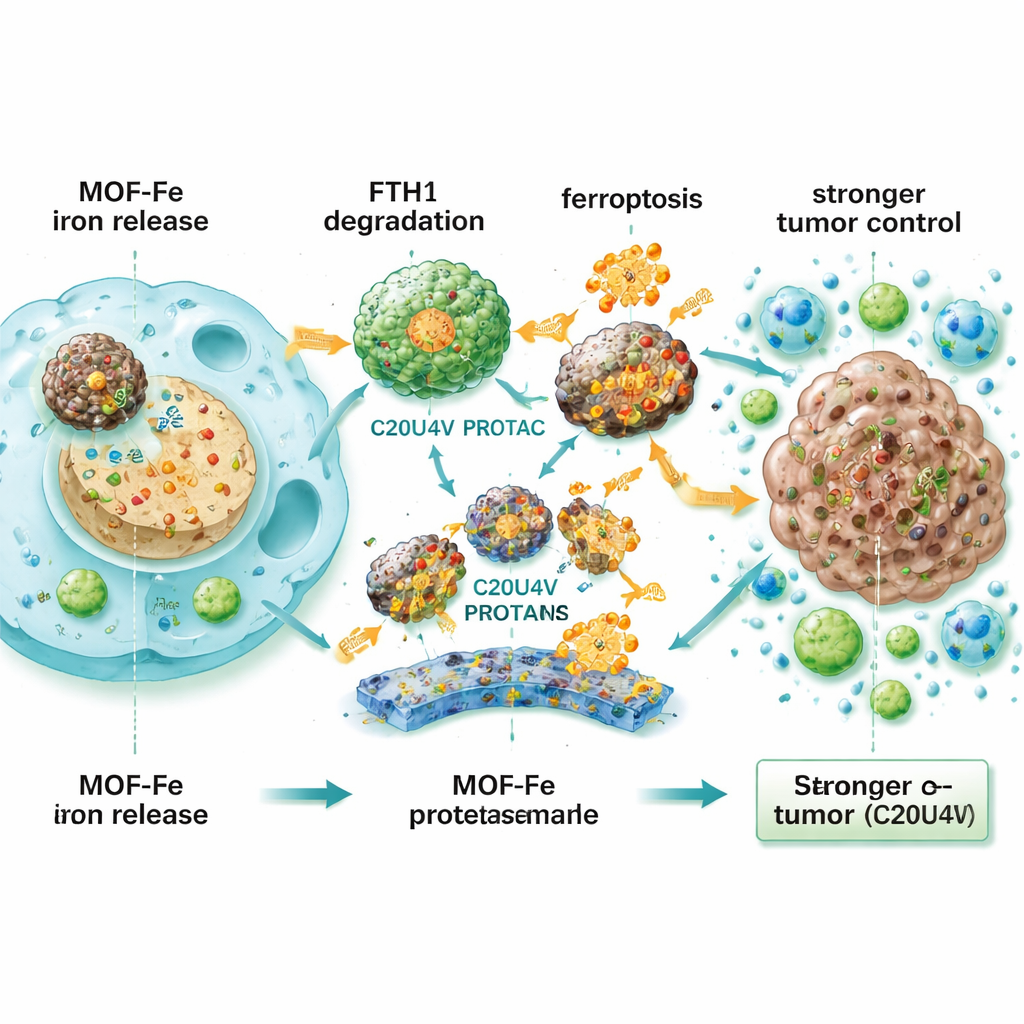
Bu direnci anlamak için ekip, MOF-Fe tedavisinden sonra hangi proteinlerin değiştiğini analiz etti. Öne çıkanlardan biri, hücrenin demir depolama kompleksinin bir parçası olan ferritin ağır zincir 1 (FTH1) oldu — fazlalık demir için moleküler anlamda yangına dayanıklı bir kasa. FTH1 seviyeleri deneysel olarak artırıldığında kanser hücreleri ferroptoza karşı daha dirençli hale geldi; FTH1 azaltıldığında ise daha duyarlı oldu. Bu, FTH1'i demir kaynaklı ölüme karşı merkezi bir kalkan olarak işaretledi. Araştırmacılar daha sonra tasarım bir molekül oluşturdu: araşidonik asitten (yüksek derecede oksitlenebilir bir yağ) yapılan ve belirli proteinleri hücrenin atık-sindirim mekanizmasına yönlendiren bir PROTAC iskeletiyle bağlı C20U4V. MOF-Fe varlığında, C20U4V ferritini bağlayıp etiketlenip yok edilmek üzere çekti; bu da FTH1 seviyelerini keskin biçimde azalttı ve hücrenin demiri güvenli şekilde kilitlemesini engelledi.
Hücre Plakalarından Mini-Tümörlere ve Farelere
MOF-Fe ile C20U4V birlikte uygulandığında, pankreas kanseri hücrelerinde daha yüksek oksidatif stres, daha fazla hasarlı zar lipidi, daha hasta mitokondriler ve yeniden çoğalma kabiliyetinde büyük düşüş görüldü. Bu sinerji, gerçek hastalardan türetilmiş üç boyutlu organoidlerde — küçük tümör benzeri yapılar — de ortaya çıktı; ilaç çifti organoidlerin boyutunu ve sayısını çöktürdü. C20U4V yağlı ve suda çözünmeyen bir bileşik olduğundan, ekip bunu reaktif oksijene duyarlı küçük miseller (M-C20U4V) içine paketledi; bunlar kan dolaşımında taşınıp stresli, hasarlı tümör dokusunda ilacı salabilir. Deri altına ve pankreasa yerleştirilmiş pankreas tümörlü fare modellerinde, GEP, MOF-Fe ve M-C20U4V'nin üçlü kombinasyonu tümörleri tekli veya ikili tedavilere göre çok daha etkili küçülttü ve hayatta kalmayı uzattı. Tedavi edilen tümörlerde daha az bölünen hücre, daha fazla ferroptoz belirteci ve T hücreleri ile diğer bağışıklık hücrelerinin daha yoğun infiltrasyonu görüldü; bu da stratejinin kanser hücrelerini doğrudan öldürmesinin yanı sıra bağışıklık sisteminin tümörü tanımasına ve saldırmasına da yardımcı olduğunu gösteriyor.
Bu Hastalar İçin Ne Anlama Gelebilir
Uzman olmayan birine ana fikir basit: pankreas tümörleri elektrik darbesi ablasyonundan sonra sıklıkla kaçıyor çünkü bazı kanser hücreleri hayatta kalıyor ve hızla uyum sağlıyor. Bu çalışma, bu hücreleri demirle doldurmanın ve aynı anda onların demir 'kasa'sını devre dışı bırakmanın, hücreleri kolayca direnemeyecekleri kendini yok etme hâline zorlayabileceğini gösteriyor. Bu yaklaşım hâlâ deneysel aşamada olup insanlarda güvenlik ve uygulanabilirlik açısından geniş testler gerektirse de, tümörlerin demiri işlemesini hassas şekilde ayarlamanın kusurlu bir lokal tedaviyi en ölümcül kanserlerden birine karşı daha kararlı bir darbeye dönüştürebileceğini düşündürüyor.
Atıf: Li, L., Su, S., Wang, Z. et al. Disruption of iron homeostasis sensitizes pancreatic cancer to irreversible electroporation. Nat Commun 17, 1866 (2026). https://doi.org/10.1038/s41467-026-68585-z
Anahtar kelimeler: pankreas kanseri, geri döndürülemez elektroperforasyon, ferroptoz, demir nanopartiküller, PROTAC terapisi