Clear Sky Science · tr
HIF böbrek temiz hücre karsinomunda EPAS1 ifadesinin bir transkripsiyonel düzenleyici devresini sürdürür
Neden böbrek kanseri daha yakından incelenmeli?
Temiz hücreli böbrek hücreli karsinom, böbrek kanserinin en yaygın biçimidir ve birçok hasta artık HIF‑2α adlı bir proteini engelleyen ilaçlar alıyor. Bu ilaçlar tümörleri küçültebilir, ancak herkes için aynı derecede etkili değiller. Bu çalışma basit ama önemli bir soruyu soruyor: bazı böbrek tümörleri neden bu kadar fazla HIF‑2α üretir ve bu “açma düğmesini” anlamak, kimin tedaviden en çok yararlanacağını tahmin etmemize ve yeni tedaviler tasarlamamıza yardımcı olabilir mi?
Kontrolden çıkan oksijen sensörü
Sağlıklı böbrek hücreleri, HIF olarak bilinen oksijen algılayıcı faktörleri sıkı kontrol altında tutmak için VHL adlı bir güvenlik proteinine güvenir. Oksijen bol olduğunda VHL, HIF proteinlerini yıkım için işaretleyerek kan damarlarının büyümesini ve hücre bölünmesini teşvik eden genlerin açılmasını önler. Temiz hücreli böbrek kanserinde VHL genellikle kaybolur ya da hasar görür. Sonuç olarak, HIF ailesinin bir üyesi olan HIF‑2α (EPAS1 geni tarafından kodlanır) yıkımdan kaçıp birikir. Önceki çalışmalar yüksek HIF‑2α aktivitesinin daha hızlı tümör büyümesi ve daha kötü sonuçlarla ilişkili olduğunu ve HIF‑2α bloke edildiğinde bazı hastalarda tümörlerin yavaşlayıp durabildiğini göstermişti. Ancak böbrek tümörlerinde EPAS1 gen aktivitesini artıran moleküler adımlar iyi anlaşılmamıştı.
Bir kanser geni için gizli bir DNA anahtarı
Yazarlar hasta tümör örnekleri, tek hücre verileri ve kanser hücre modellerini kullanarak HIF‑2α haberci RNA’sının temiz hücreli böbrek tümörlerinde normal böbrek dokusuna veya diğer böbrek tümörü türlerine göre belirgin şekilde daha yüksek olduğunu gösteriyorlar. Ardından EPAS1 genom bölgesini aktif düzenleyici DNA’yı işaretleyen kimyasal ve yapısal işaretler açısından tarıyorlar. Bu, EPAS1’in yaklaşık 70.000 DNA bazı yukarısında yer alan ve temiz hücreli tümörlerde özgün şekilde aktif olan güçlü bir güçlendiriciyi—uzun mesafeli bir gen anahtarını—ortaya çıkarıyor. Tümör hücrelerinde bu güçlendiricideki kromatin açık, etkinleşme işaretleriyle süslü ve fiziksel olarak EPAS1 promotörüne döngü oluşturacak şekilde temas halindeyken, normal böbrek tübül hücrelerinde bu bölge büyük ölçüde sessizdir. Bu güçlendiricideki aktivite, büyük kanser veri setlerinde daha yüksek EPAS1 seviyeleriyle korele oluyor. 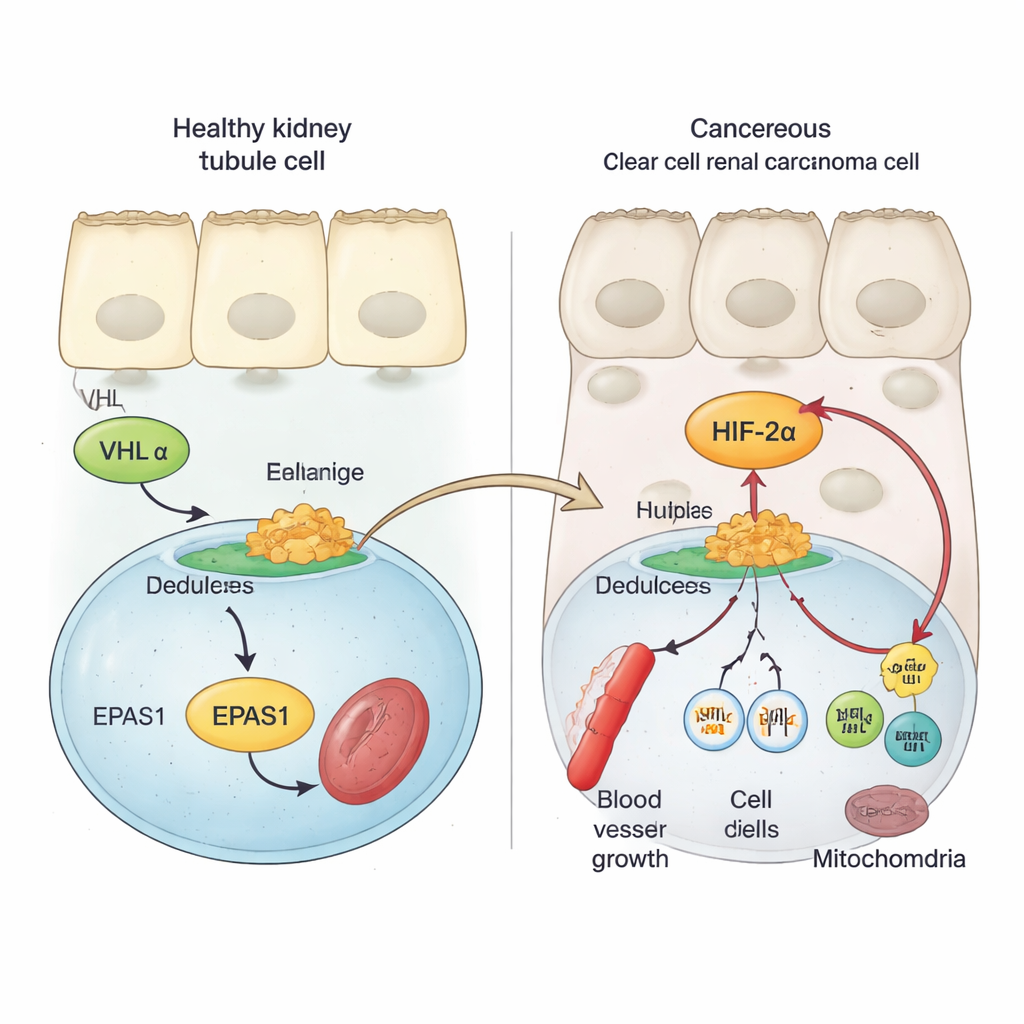
Böbrek kimlik faktörleri tarafından desteklenen kendini güçlendiren bir döngü
Çalışma HIF proteinlerinin sadece düşük oksijene yanıt vermekle kalmayıp aslında kendi üretimlerini de desteklediğini gösteriyor. Araştırmacılar VHL’i geri getirdiklerinde veya önemli bir HIF ortak proteini (HIF‑1β) çıkardıklarında EPAS1 seviyeleri düşüyor ve güçlendirici daha az erişilebilir hale geliyor. Protein–DNA temaslarının doğrudan haritalanması, HIF’in EPAS1’in yukarısındaki iki güçlendirici bölgeye, temiz hücreye özgü güçlendirici dahil, bağlandığını gösteriyor. Böbrek tümörü hücrelerinde bu güçlendirici ayrıca böbrek hücre kimliğini tanımlayan ve tümör büyümesini desteklediği bilinen transkripsiyon faktörleri PAX8 ve HNF‑1β tarafından da işgal ediliyor. PAX8 veya HNF‑1β’yi bozmak ya da güçlendiricideki bağlanma bölgelerini mutasyona uğratmak HIF‑2α RNA ve proteinini azaltıyor ve güçlendirici aktivitesini zayıflatıyor. Birlikte, bu bulgular oto‑düzenleyici bir devreyi ortaya koyuyor: HIF‑2α, böbrek soy faktörleriyle birlikte EPAS1 güçlendiricisinin aktivitesini artırıyor ve bu da daha fazla HIF‑2α üretimini tetikliyor.
Genetik risk ve tümör davranışı aynı devrede birleşiyor
EPAS1 bölgesi uzun süredir genom genelindeki çalışmalarda böbrek kanseri riski için bir sıcak nokta olarak işaretlenmiş; belirli kalıtsal varyantlar daha yüksek kanser oranları ve tümörlerde VHL mutasyonlarıyla ilişkilendirilmiş. Genetik verileri gen ifadeleriyle birleştirerek yazarlar, önemli bir EPAS1 varyantının yüksek riskli formunu taşıyan bireylerin tümörlerinde genellikle daha yüksek HIF‑2α seviyelerine sahip olduğunu gösteriyorlar—ve deneysel olarak HIF stabilize edildiğinde normal böbrek tübül hücrelerinde bile. Bu, kalıtsal DNA farklılıklarının güçlendiricinin ne kadar güçlü yanıt vereceğini ayarlayabileceğini, VHL kaybı sonrası bazı böbreklerin HIF‑2α’yı daha güçlü şekilde artırmaya hazır hale gelmesine neden olabileceğini düşündürüyor. Glioblastoma hücrelerindeki deneyler, aynı güçlendiricinin bazı beyin tümörlerinde de etkinleşebileceğini göstererek, bu düzenleyici modülün HIF‑2α’nın önemli olduğu diğer kanserlerde de yeniden kullanılabileceğine işaret ediyor. 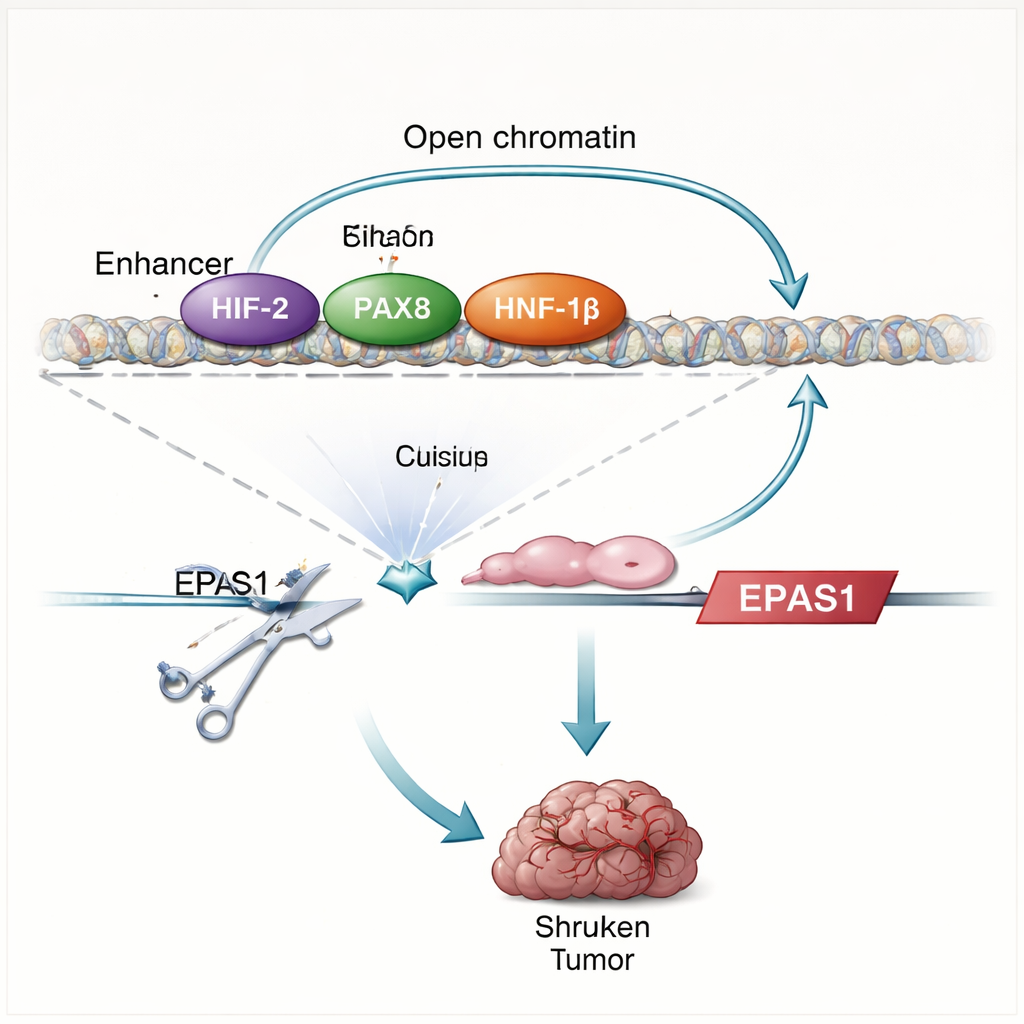
Döngüyü kırarak tümör büyümesini durdurmak
Bu güçlendiricinin ne kadar gerekli olduğunu test etmek için ekip, böbrek kanseri hücre hatlarında ve taze hasta tümör hücrelerinde CRISPR genom düzenlemesi kullanarak içindeki HIF bağlanma motiflerini hasara uğratıyor. Bu kesim HIF‑2α RNA’sını yaklaşık üçte bir ile yarı arası oranında azaltıyor, CCND1 ve VEGFA gibi iyi bilinen HIF‑2α hedef genlerin seviyelerini düşürüyor ve daha geniş hipoksi gen programını zayıflatıyor. Düzenlenmiş hücreler farelere implante edildiğinde büyük ölçüde tümör oluşturamıyorlar; kontrol hücrelerinin aksine. Güçlendirici bozulduktan sonra görülen gen değişiklikleri paterni doğrudan klinik bir ilaçla HIF‑2α’yı bloke etmenin etkilerini yakından yansıtıyor; bu da tek bir DNA unsurunun bu kanserlerde HIF‑2α yolunun başlıca sürücüsü olduğunu vurguluyor.
Hastalar ve tedaviler için anlamı
Uzman olmayanlar için ana mesaj şudur: Yazarlar temiz hücreli böbrek tümörlerinde HIF‑2α adlı önemli bir kanser teşvik edici proteini açık tutan kendini güçlendiren bir DNA düğmesi keşfetmişler. Bu düğme hem VHL güvenlik freninin kaybına hem de böbreğe özgü yardımcı proteinlere bağlı ve kalıtsal genetik varyantlardan etkileniyor. Güçlendirici birçok temiz hücre tümöründe yüksek derecede aktif olduğundan ve HIF‑2α yolunun ne kadar güçlü çalıştığıyla yakından bağlantılı olduğundan, onun aktivitesini ölçmek—veya doğrudan hedeflemek—mevcut HIF‑2α inhibitörlerinden en çok kimlerin yararlanacağını belirlemeye yardımcı olabilir ve tümörler ilaç direnci kazandığında bu yolu kapatmanın yeni yollarını sunabilir.
Atıf: Naas, S., Krüger, R., Grampp, S. et al. HIF sustain a transcriptional regulatory circuit of EPAS1 expression in renal clear cell carcinoma. Nat Commun 17, 1764 (2026). https://doi.org/10.1038/s41467-026-68576-0
Anahtar kelimeler: temiz hücreli böbrek hücreli karsinom, HIF-2α, EPAS1 güçlendirici, VHL mutasyonu, böbrek kanseri genetiği