Clear Sky Science · tr
Nükleotit bağlı insan telomerazının telomerik DNA tekrar ekleme döngüsünün birkaç adımındaki yapıları
Kromozomlarımızın uçları neden önemli
Her hücre bölünmesinde, kromozomlarımızın uçlarındaki koruyucu kapaklar — telomerler — biraz kısalır. Çok kısa hale gelirlerse hücreler bölünmeyi durdurur veya işlevleri bozulur; bu da yaşlanma ve hastalığa katkıda bulunur. Telomerleri yeniden inşa edebilen telomeraz adlı bir moleküler makine vardır ve bu enzim çoğu kanserde olağanüstü derecede aktiftir. Bu çalışma, insan telomerazının telomerleri adım adım nasıl tuttuğunu ve uzattığını benzeri görülmemiş ayrıntıda ortaya koyuyor; bu, bir gün yaşa bağlı bozukluklarda ve kanserde bu enzimi nasıl ince ayar yapabileceğimize dair ipuçları veriyor.
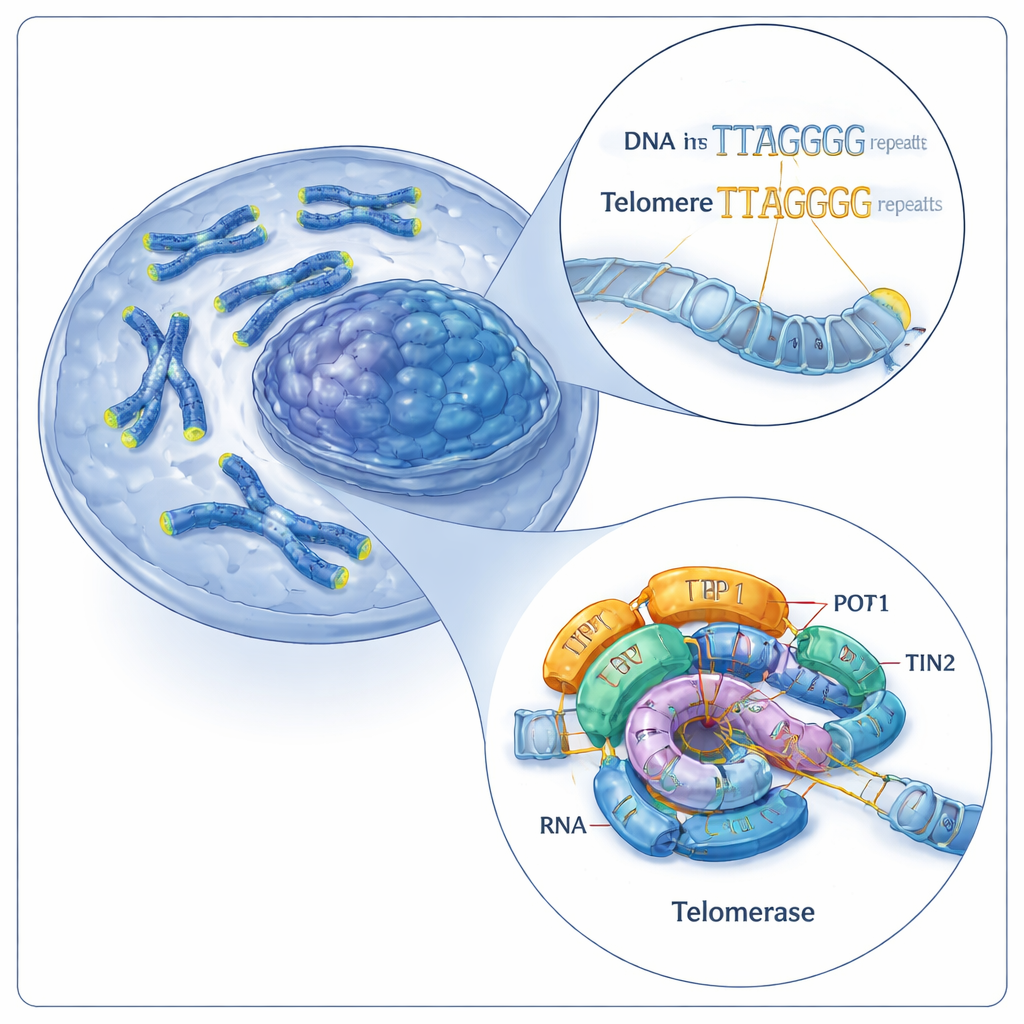
Hücrenin kromozom ucu onarım ekibi
Telomerler kısa, tekrarlayan DNA dizilerinden oluşur (insanlarda altı harfli bir desen: TTAGGG). Telomeraz bu tekrarları kromozom uçlarına ekleyerek telomerleri uzatır. Bunu iki ana bileşenle yapar: telomeraz ters transkriptaz (TERT) adlı bir protein ve şablon görevi gören yerleşik bir RNA molekülü (hTR). Birlikte bu bileşenler katalitik çekirdeği oluşturur; çekirdek, TPP1–POT1–TIN2 üçlüsü de dahil olmak üzere shelterin olarak bilinen yardımcı proteinlerle desteklenir. Önceki çalışmalar insan telomerazını yalnızca tek bir çalışma durumunda görselleştirmişti; geriye büyük bir soru kalmıştı: bu makine DNA’dan kopmadan nasıl tekrar tekrar yeni tekrarlar ekleyebiliyor?
Telomerazı hareket halinde dondurmak
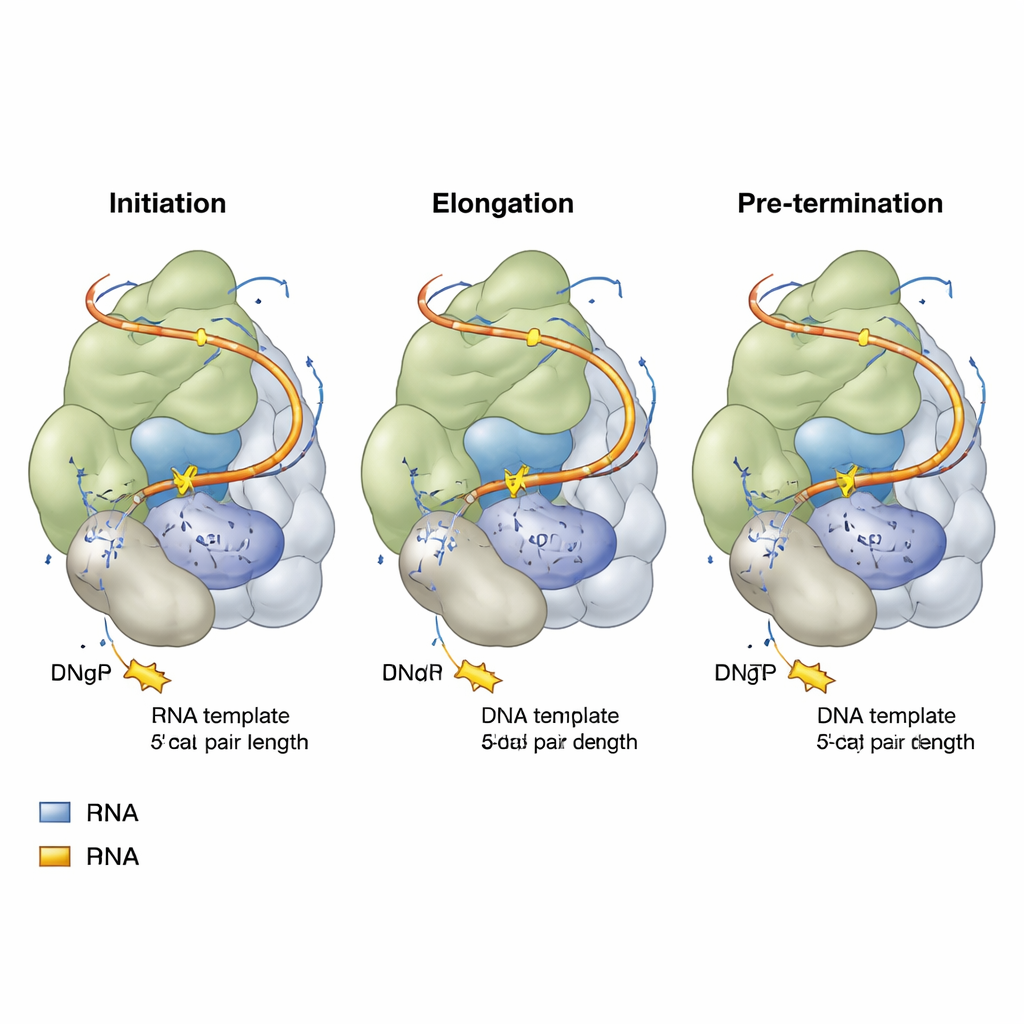
Araştırmacılar insan hücrelerinde insan telomerazını yeniden oluşturdu ve ardından dikkatle tasarlanmış telomerik DNA parçaları ve reaksiyona girmeyen nükleotit analogları — DNA harflerine benzeyen ama tamamen katılamayan moleküller — ile bir araya getirdiler. Yüksek çözünürlüklü kriyo-elektron mikroskobu kullanarak, telomerazın tekrar-ekleme döngüsünün üç kilit aşamasında: başlangıç (başlatma), kopyalamanın ortası (uzatma) ve bir tekrar bitmeden hemen önce (ön-sona erme) anlık görüntüler yakaladılar. Her anlık görüntü, katalitik çekirdeğin kısa bir DNA–RNA hibritini kavradığını ve aktif bölgede, büyüyen DNA zincirine eklenecek yeni bir nükleotidin hazır beklediğini gösterdi.
Büyük bir süreci kontrol eden küçük bir fermuar
Üç aşamanın tümünde şaşırtıcı bir tema ortaya çıktı: telomeraz içindeki DNA–RNA hibriti temelde aynı uzunlukta kalıyor — sadece dört baz çifti uzunluğunda ve yeni bir nükleotid girdiğinde geçici olarak beşe uzuyor. TERT içindeki belirli bir amino asit, “fermuar başı” lakabıyla, tutarlı biçimde bu kısa hibritin sonunu işaretliyor ve uzamasını engelliyor. Yeni DNA harfleri eklendikçe, uzak uçtaki bir baz çifti eriyip ayrılıyor; böylece hibrit bu sıkı dört ila beş çiftlik pencereden daha uzun olmuyor. Bu kompakt tasarım, zincirlerin ayrılmasını ve konum değiştirmesini kolaylaştırıyor; böylece enzim ilerleyip bir sonraki tekrara başlayabiliyor ancak DNA’yı tamamen bırakmıyor. Kısa hibritte hangi DNA ve RNA harflerinin bulunduğundaki ince farklılıklar, bazı telomerik uç dizilerinin telomeraza diğerlerinden daha sıkı bağlanmasını açıklıyor.
Esnek RNA bağlantıları ve hareketli parçalar
Telomeraz içindeki RNA şablonu serbestçe yüzmez; her iki tarafta da 5′ ve 3′ şablon bağlayıcıları adı verilen esnek bölümlerle bağlanmıştır. Telomeraz başlatmadan ön-sona ermeye ilerledikçe, yukarı yönlü (5′) bağlayıcı bir bungee ipi gibi gerilir ve sonunda bir tekrarın sonunu işaretlemeye yardımcı olacak tam gerilmiş bir duruma ulaşır. Bu arada aşağı yönlü (3′) bağlayıcı dışa doğru kabarır ve başka bir RNA yapısına (P6.1 sap-döngüsü) ve yakınlardaki protein bölgelerine yaklaşır. Bu bağlayıcılar çok kısa ya da çok uzun olursa veya P6.1 değiştirilirse, telomerazın ardışık tekrarlar ekleme yeteneği keskin biçimde düşer. Önemli olarak, TEN domaini ve TRAP kama adı verilen telomeraz-spesifik bir ek gibi bazı protein bölgeleri ayarlanabilir kılavuzlar olarak hareket eder; hem DNA hem de bu RNA bağlayıcılarla temas kurarlar. TRAP kamasının hacmini azaltan mutasyonlar, aslında enzimi daha procesif hale getirebilir; bu da bu kamanın şablon hareketini zamanlayan kontrollü bir bariyer olarak normalde görev yaptığını düşündürüyor.
Terapi hedefi hakkında yeni içgörüler
Yapısal anlık görüntüleri hedeflenmiş mutasyonların fonksiyonel testleriyle birleştirerek, çalışma insan telomerazının telomerleri tekrar tekrar nasıl uzattığına dair ayrıntılı bir mekanik model öneriyor. Enzim çok kısa bir DNA–RNA hibriti tutuyor, bu uzunluğu zorunlu kılmak için fermuar benzeri bir kalıntı kullanıyor ve şablonu ilerletmek ve DNA’yı birden çok kopyalama turunda sabit tutmak için esnek RNA bağlayıcılarına ve hareketli protein elemanlarına dayanıyor. Uzman olmayanlar için ana mesaj şudur: telomeraz statik bir kopyalama makinesi değil; geometrisi ve hareketli parçaları telomerleri ne kadar ve ne kadar verimli koruyabileceğini belirleyen hassas ayarlı, yay yüklü bir cihaz gibi çalışır. Bu koreografiyi anlamak, kanserlerde telomerazı azaltabilecek veya erken yaşlanma hastalıklarında işlevini stabilize edebilecek ilaçların geliştirilmesinin önünü açıyor.
Atıf: Balch, S., Franco-Echevarría, E., Ghanim, G.E. et al. Structures of nucleotide-bound human telomerase at several steps of its telomeric DNA repeat addition cycle. Nat Commun 17, 1847 (2026). https://doi.org/10.1038/s41467-026-68560-8
Anahtar kelimeler: telomeraz, telomerler, cryo-EM, genom kararlılığı, kanser biyolojisi