Clear Sky Science · tr
A. fumigatus’ta tüm genom çapında kodlamayan transkriptlerin keşfi ve fenotiplemesi, antifungal ilaç duyarlılığında rolü olan lncRNA’ları ortaya koyuyor
Evimizdeki küf neden önemli?
Çoğumuz küfü ekmekteki bir sorun veya nemli köşelerde görürüz; ancak yaygın bir küf türü olan Aspergillus fumigatus, yılda iki milyondan fazla ölüme neden oluyor—malarya ve HIV’den daha fazla. Hekimler bu patojeni kontrol altında tutmak için sınırlı bir antifungal ilaç silahına dayanıyor ve bu ilaçlara karşı direnç hızla artıyor. Bu çalışma, proteini kodlamayan ancak yine de mantarın tedaviye yanıtını etkileyebilen uzun kodlamayan RNA’lar (lncRNA’lar) gibi mantarın genomundaki gizli bir katmanı araştırıyor. Bu “sessiz” genetik unsurları anlamak, antifungal direnci tahmin etme, izleme ve nihayetinde karşı koyma yollarını açabilir.
Mantar DNA’sındaki gizli mesajlar
Klasik bakışla genler, hücrenin işlerini yapan proteinleri kodlayan DNA dizileri olarak düşünülmüştür. Son on yılda bilim insanları, genoma ait geniş bölgelerin protein haline gelmeyen RNA moleküllerine transkribe edildiğini keşfettiler. Bu uzun kodlamayan RNA’lar hâlâ hücre davranışını, örneğin ilaçlara nasıl yanıt verdiklerini etkileyebilir. lncRNA’lar insanlarda ve mayada haritalanmış olsa da, hastalık yapıcı küfler—örneğin A. fumigatus—gibi organizmalarda büyük ölçüde keşfedilmemişti. Yazarlar, bu gizemli transkriptlerin tüm genom çapında bir kataloğunu oluşturarak herhangi birinin ilaç duyarlılığı ile direncin dengesini değiştirip değiştirmediğini sorgulamaya karar verdiler.
İlaç saldırısı altındaki küfü dinlemek
lncRNA’ları ortaya çıkarmak için ekip, A. fumigatus’u mantar hücre zarını hedef alan yaygın azoller de dahil altı farklı antifungal bileşiğe maruz bıraktı ve ardından üretilen tüm RNA’ları diziledi. Özel bir biyoinformatik boru hattı kullanarak onlarca bin transkript derlediler ve bilinen protein kodlayan genlere veya kısa ev içi RNA’lara karşılık gelenleri sistematik olarak elemeye yöneldiler. Birden çok filtreleme ve el ile kürasyon turundan sonra, genom boyunca yayılan yüksek güvenilirlikte 1.089 yeni uzun kodlamayan RNA’ya ulaştılar. Bunların çoğu ya bilinen genlerin arasında yer alıyordu ya da ters yönde örtüşüyordu ve birlikte mantarın aktif olarak transkribe edilen genom fraksiyonunu yaklaşık üçte ikiden dörtte birinden fazla olacak şekilde genişlettiler.
Koordine yanıtlar ve korunmuş sıcak noktalar
Araştırmacılar bu lncRNA’ların farklı ilaç dozları altında nasıl değiştiğini karşılaştırdıklarında mantarın bunları rastgele kullanmadığını buldular. Bunun yerine lncRNA’lar yaklaşık 15 farklı yanıt desenine ayrılıyordu; bazıları birden fazla ilaçta paylaşılıyordu, diğerleri ise belirli tedavilere özgüydü. Örneğin benzer biyokimyasal yolları hedefleyen ilaçlar örtüşen lncRNA imzaları tetiklerken, bir protein sentezi inhibitörü birçok benzersiz yanıt oluşturdu. Birçok lncRNA, demir yakalama veya mantar hücre zarlarının ana bileşenlerinden biri olan ergosterolün biyosentezi gibi azol duyarlılığını etkilediği bilinen genlere çok yakındı. Birkaç durumda, yakınlardaki bir lncRNA ile ilaç yanıt geninin birlikte yukarı veya aşağı değişmesi, bu kodlamayan elemanların hayatta kalma programlarını koordine etmeye yardımcı olabileceğini işaret etti.
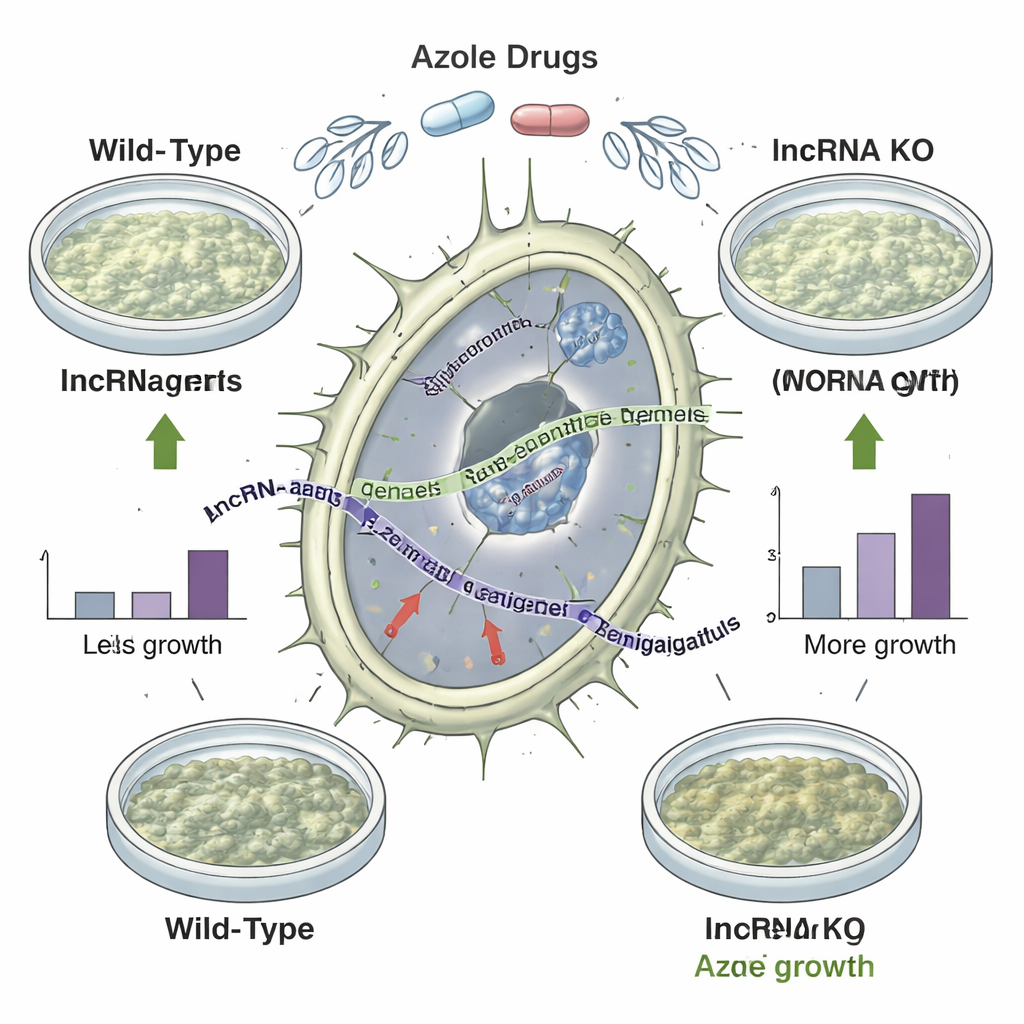
“Sessiz” genlerin yok edilmesi ilaç duyarlılığını değiştiriyor
lncRNA’ların kataloglanması bir şey; önemli olduklarını kanıtlamak başka bir şey. Ekip, mantarın genomundan seçilmiş 92 lncRNA bölgesini sildi ve mutantların yüksek sıcaklık, düşük demir ve üç farklı azol ilaca maruz kalma dahil çeşitli stresler altında nasıl büyüdüğünü karşılaştırdı. Altmış mutant koşula özgü uygunluk değişiklikleri gösterdi ve 35’i azollerle karşılaştıklarında aslında orijinal türden daha iyi büyüdü. Öne çıkan bir silme suşu, yakınlardaki protein kodlayan genleri basitçe artırmak yerine tüm test edilen azollerde gelişmiş büyüme gösterdi; bu da eksik lncRNA’nın kendisinin ilaç toleransını sınırladığına güçlü olarak işaret ediyor. Bilinen ilaç duyarlılık profillerine sahip birçok klinik ve çevresel izolat incelendiğinde, belirli lncRNA genlerinin varlığının veya yokluğunun her suşun azollerle ne kadar kolay engellendiğiyle örtüştüğü görüldü.
Bu, ölümcül mantar enfeksiyonlarıyla mücadele için ne anlama geliyor?
Uzman olmayanlar için temel mesaj, bir zamanlar “çöp” sayılan mantar genomu parçalarının A. fumigatus’ın ne kadar tehlikeli olduğunu ve ilaçlarımızın ona karşı ne kadar etkili olduğunu aktif olarak şekillendirdiğidir. Bu büyük patojende uzun kodlamayan RNA’ların ilk kapsamlı haritasını oluşturarak ve onlarcasını ölçülebilir ilaç yanıtı değişiklikleri ile ilişkilendirerek, bu çalışma yeni bir genetik belirteç ve potansiyel hedef sınıfının kapısını aralıyor. Uzun vadede, lncRNA’lar bazı suşların neden doğal olarak tedaviye daha dirençli olduğunu açıklamaya yardımcı olabilir, daha etkili tanıların tasarımına rehberlik edebilir ve direnci mantarı doğrudan öldürmek yerine ona dayanmasına yardımcı olan sessiz düzenleyicileri susturarak etkisiz hale getiren tedavilere ilham verebilir.
Atıf: Weaver, D., Qi, T., Chown, H. et al. Genome-wide discovery and phenotyping of non-coding transcripts in A. fumigatus reveals lncRNAs with a role in antifungal drug sensitivity. Nat Commun 17, 1832 (2026). https://doi.org/10.1038/s41467-026-68543-9
Anahtar kelimeler: Aspergillus fumigatus, antifungal direnç, uzun kodlamayan RNA, azole ilaçlar, fungal genomik