Clear Sky Science · tr
Palmitik asit kaynaklı B7H3 palmitoilasyonu, bağışıklıktan kaçışı teşvik ediyor
Bu araştırma kanser hastaları için neden önemli
Yeni immünoterapi ilaçlarının bağışıklık sisteminin kanseri hedeflemesine yardımcı olabildiğini çoğu kişi duymuştur; ancak yaygın görülen kolorektal (bağırsak) kanseri hastalarının birçoğu bu tedavilerden az yarar görür. Bu çalışma, kolorektal tümörlerin bağışıklıktan korunmak için kullandığı gizli bir biyokimyasal numarayı ortaya koyuyor ve bu hastalarda immünoterapinin daha etkili olmasını sağlayabilecek yeni bir ilaç türüne —küçük bir peptide— işaret ediyor.
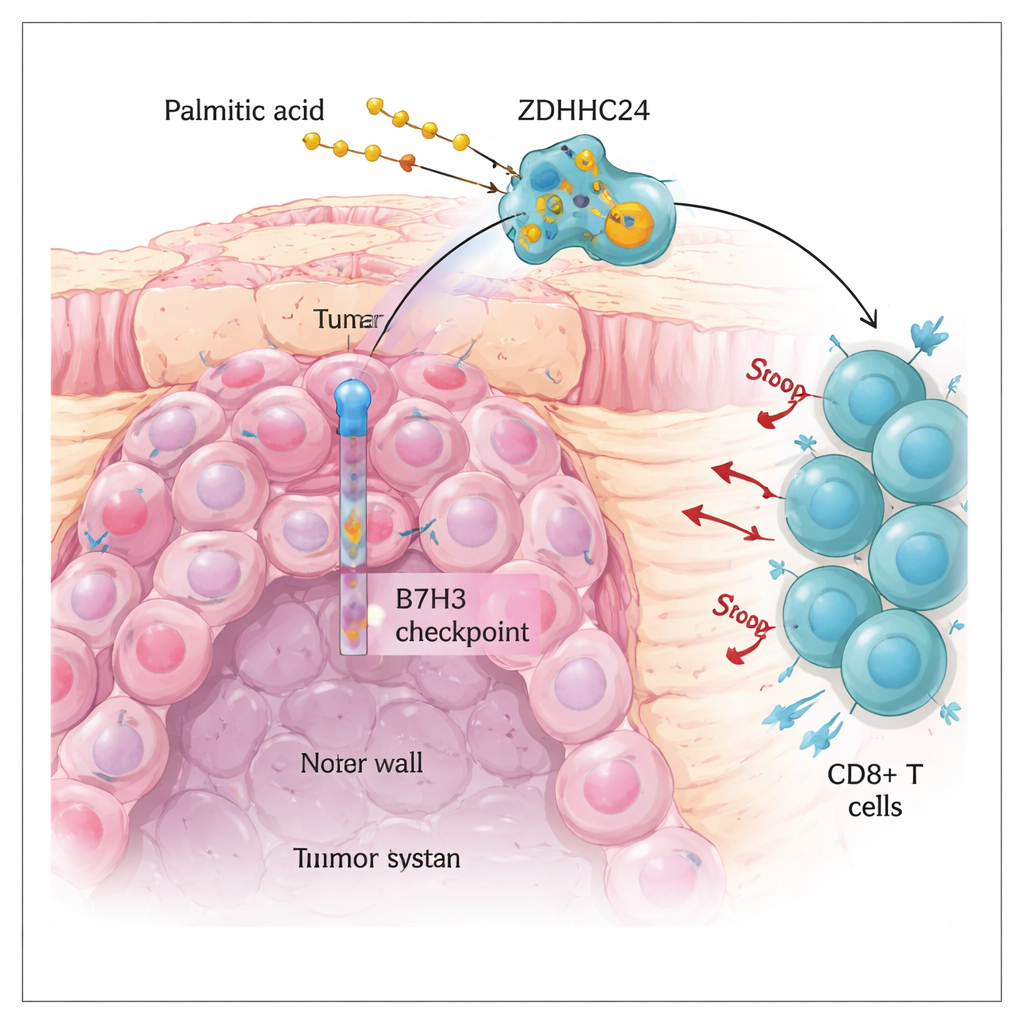
Mevcut bağırsak kanseri immünoterapisinde bir engel
Kolorektal kanser dünya çapında en yaygın kanserlerden biridir. PD-1 ve PD-L1 inhibitörleri gibi bağışık “frenlerini” serbest bırakan immünoterapi ilaçları, çok sayıda DNA hatası taşıyan (so‑called MSI-H) tümörlere sahip azınlıktaki hastalar için tedaviyi dönüştürdü. Ne yazık ki, çoğu kolorektal kanser mikrosatellit stabil (MSS) olup bu tedavilere zayıf yanıt verir. Yazarlar, tümör hücrelerinin yüzeyinde yer alıp özellikle CD8+ T hücrelerinin etkinliğini azaltan B7H3 adlı başka bir fren molekülüne odaklandı. B7H3 proteininin MSS tümörlerde güçlü şekilde yükseldiğini ve daha kötü sağkalımla ilişkili olduğunu buldular; oysa altta yatan B7H3 geni daha aktif değildi. Bu uyumsuzluk önemli bir soruyu işaret etti: tümör hücrelerinde B7H3 proteinini bu kadar bol tutan şey neydi?
Yaygın bir yağın tümörlerin saklanmasına nasıl yardımcı olduğu
Ekip, tümör metabolizmasının B7H3’ü stabilize ediyor olabileceğini düşündü. MSS ve MSI-H kolorektal tümörlerin gen aktivitesi ve küçük molekül profillerini karşılaştırarak, birçok yağla ilgili yolakta farklılıklar olduğunu ve palmitik asit adlı tek bir yağ asidinin öne çıktığını keşfettiler. Laboratuvarda kolon kanseri hücrelerini çeşitli yağ parçalanma ürünlerine maruz bıraktıklarında, yalnızca palmitik asit B7H3 protein seviyelerinde belirgin bir artışa neden oldu. Daha ileri deneyler bunun nedenini gösterdi: palmitik asit, palmitoilasyon adı verilen bir kimyasal değişiklik sürecine giriyor; bu süreçte yağ zinciri proteinlerin belirli bölgelerine ekleniyor. ZDHHC24 adlı bir enzim tarafından B7H3 içindeki tek bir sistein konumunda gerçekleştirilen bu modifikasyon, B7H3’ü daha stabil ve tümör hücresi yüzeyinde daha bol hale getirdi.
Bir bağışıklık freninin çöp yolunun bloke edilmesi
Hücreler normalde istenmeyen veya hasarlı proteinleri geri dönüşüm ve çöp imha gibi çalışan sistemlerle ortadan kaldırır. Araştırmacılar, B7H3’ün ağırlıklı olarak otofaji adı verilen bir hücresel “kendini yeme” yoluyla parçalandığını ve bu yolda taşıyıcıları yok edilmek üzere etiketlemek için SQSTM1/p62 adlı bir reseptör proteinin kullanıldığını gösterdiler. B7H3 palmitoilasyonlu olduğunda bu reseptöre zayıf bağlandı ve otofajik degradasyondan kaçtı; bu da bağışıklık freninin kalıcı ve yüksek seviyelerde kalmasına yol açtı. Palmitoilasyon bölgesi mutasyona uğratıldığında ya da ZDHHC24 enzimi silindiğinde, B7H3 daha etkin bir şekilde hücresel “çöp torbalarına” yönlendirildi ve parçalandı. Farelerde palmitoilasyonlu B7H3 eksik tümörler daha yavaş büyüdü, bağışık yetmez hayvanlarda kendi iç büyüme hızlarını değiştirmedi ve çok daha fazla CD8+ T hücresi ile güçlü tümör öldürücü aktivite gösterdi. Bu, modifikasyonun esasen bağışıklığı devre dışı bırakarak etkisini gösterdiğini, kanser hücrelerinin bölünme hızını değiştirmediğini kanıtladı.
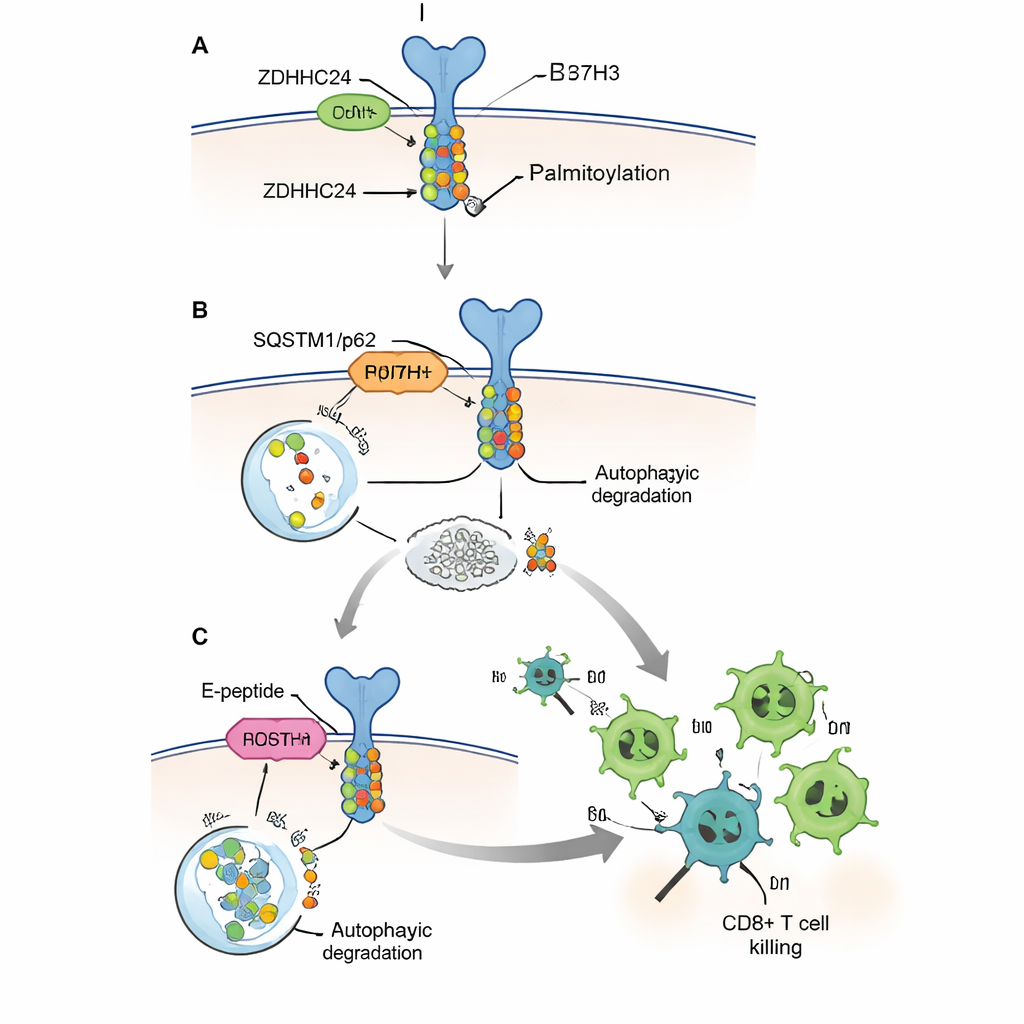
Kalkanı azaltmak ve T hücrelerini güçlendirmek
ZDHHC24 ya da B7H3’ü genetik olarak tamamen ortadan kaldırmanın hastalarda pratik bir tedavi olmadığı için, yazarlar E-peptid adını verdikleri kısa, hücreye nüfuz edebilen bir peptid tasarladılar. Bu peptid, normalde ZDHHC24’e bağlanan B7H3 proteininin küçük bir bölümünü taklit ederek enzimin gerçek B7H3 moleküllerini modifiye etmesini önleyen bir yem görevi görür. Kültürdeki hücrelerde E-peptid, B7H3 palmitoilasyonunu ve protein seviyelerini azalttı, otofaji makinesinin tanımasını geri getirdi ve insan CD8+ T hücrelerinin tümör hücrelerini daha etkin öldürmesine izin verdi. İnsan bağışıklık hücrelerini ve insan kolorektal tümörlerini taşıyan insanlaştırılmış fare de dahil olmak üzere birkaç fare modelinde E-peptid enjeksiyonları tümörleri küçülttü, içlerindeki CD8+ T hücre sayısını artırdı ve granzyme B ile interferon‑gamma gibi önemli öldürücü moleküllerin üretimini artırdı.
Mevcut immünoterapi için yeni bir ortak
Son olarak araştırmacılar, bu stratejinin standart PD‑1 blokajı ile birlikte işe yarayıp yaramayacağını sordular. Kolorektal kanser fare modellerinde hem tek başına E‑peptid hem de tek başına anti‑PD‑1 antikoru bir miktar tümör kontrolü sağladı. Ancak iki tedavi birlikte uygulandığında, çok daha güçlü ve daha uzun süreli tümör baskılama görüldü; bazı durumlarda tümörlerin kaybolmasına yol açtı ve ortalama sağkalımı kontrol gruplarına kıyasla iki kattan fazla uzattı. Bu, B7H3 kalkanını yağ "çapa"sını keserek devre dışı bırakmanın PD‑1 yolunu hedefleyen mevcut kontrol noktası ilaçlarını tamamlayabileceğini düşündürüyor.
Gelecekteki kanser tedavileri için ne anlama geliyor
Basitçe ifade etmek gerekirse, bu çalışma yaygın bir diyet yağı olan palmitik asidin kolorektal tümörler tarafından bağışıklığı engelleyen bir proteini (B7H3) kimyasal olarak zırhlamak ve kanserin saklanmasına yardımcı olmak için nasıl kötüye kullanılabileceğini gösteriyor. Bu tek kimyasal bağlanmayı engelleyerek yazarlar zırhı soyabildiler, hücrenin kendi imha sistemlerinin B7H3’ü kaldırmasına izin verdiler ve CD8+ T hücrelerinin saldırısına yeniden erişim açtılar. E‑peptid’in kendisi erken aşamada deneysel bir araç olsa da çalışma, B7H3 palmitoilasyonunu ve bunu yapan enzim ZDHHC24’ü umut vaat eden ilaç hedefleri olarak tanımlıyor. Benzer ajanlar insanlarda güvenli ve etkili bulunursa, bir gün daha fazla kolorektal kanseri immünoterapiyi görmezden gelen “soğuk” tümörlerden bağışıklık sistemi tarafından tanınan ve yok edilen “sıcak” tümörlere çevirebilirler.
Atıf: Rao, Z., Huang, C., Wu, Q. et al. Palmitic acid-triggered B7H3 palmitoylation promotes immune escape. Nat Commun 17, 1810 (2026). https://doi.org/10.1038/s41467-026-68525-x
Anahtar kelimeler: kolorektal kanser immünoterapisi, B7H3 kontrol noktası, palmitik asit metabolizması, protein palmitoilasyonu, CD8 T hücresi tümör bağışıklığı