Clear Sky Science · tr
Zebrabalığı makrofajları fiziksel yara sinyallerini hızlı damar geçirgenliğine çeviriyor
Ufacık Bir Balık Bize Yaralanma Ödemi Hakkında Ne Öğretiyor
Dizini sıyırdığınızda, bölge hızla kızarır, şişer ve sıvıyla sızar. Yakınlardaki kan damarlarındaki bu hızlı değişim enfeksiyonla savaşmak ve onarımı başlatmak için kritik önemdedir; ancak vücudun hasarı nasıl saniyeler içinde algıladığı ve tepki verdiği gerçek zamanlı olarak gözlemek zor olmuştur. Şeffaf zebrabalığı larvaları ve gelişmiş canlı görüntüleme kullanılarak yapılan bu çalışma, kan damarlarının etrafına sarılmış özelleşmiş bağışıklık hücrelerinin yaranın fiziksel şokunu neredeyse anında damar sızıntısına nasıl çevirdiğini ortaya koyuyor; bu da iltihap, iyileşme ve hatta insan akciğer yaralanması hakkında yeni bakış açıları sunuyor.
Hasarın Vücuda Nasıl Yayıldığını İzlemek
Araştırmacılar, şeffaf vücutları sayesinde mikroskop altında hücreleri ve kan damarlarını hareket halinde izlemeye olanak veren genç zebrabalıkları kullandılar. Kuyruk yüzgecinin ucunu kestiler ve dolaşımı sağlıklı damarların içinde kalan parlak bir boya ile doldurdular. Yaralanmış balıklar normal tatlı suya geri konulduğunda, dokulara ani su girişi yaranın çevresinde bir “ozmotik şok” oluşturdu. Dakikalar içinde yakındaki damarlar genişledi ve floresan boya çevre dokuya sızmaya başladı; bu, insan yaralarında görülen şişme ve sızıntıyı taklit ediyordu. Balıkları normal ve özel dengelenmiş tuz ya da şeker çözeltileri arasında geçirerek, ekip bu hızlı damar geçirgenleşmesinin yalnızca doku yırtılmasına değil, büyük ölçüde ozmotik değişimlere bağlı olduğunu gösterdi.
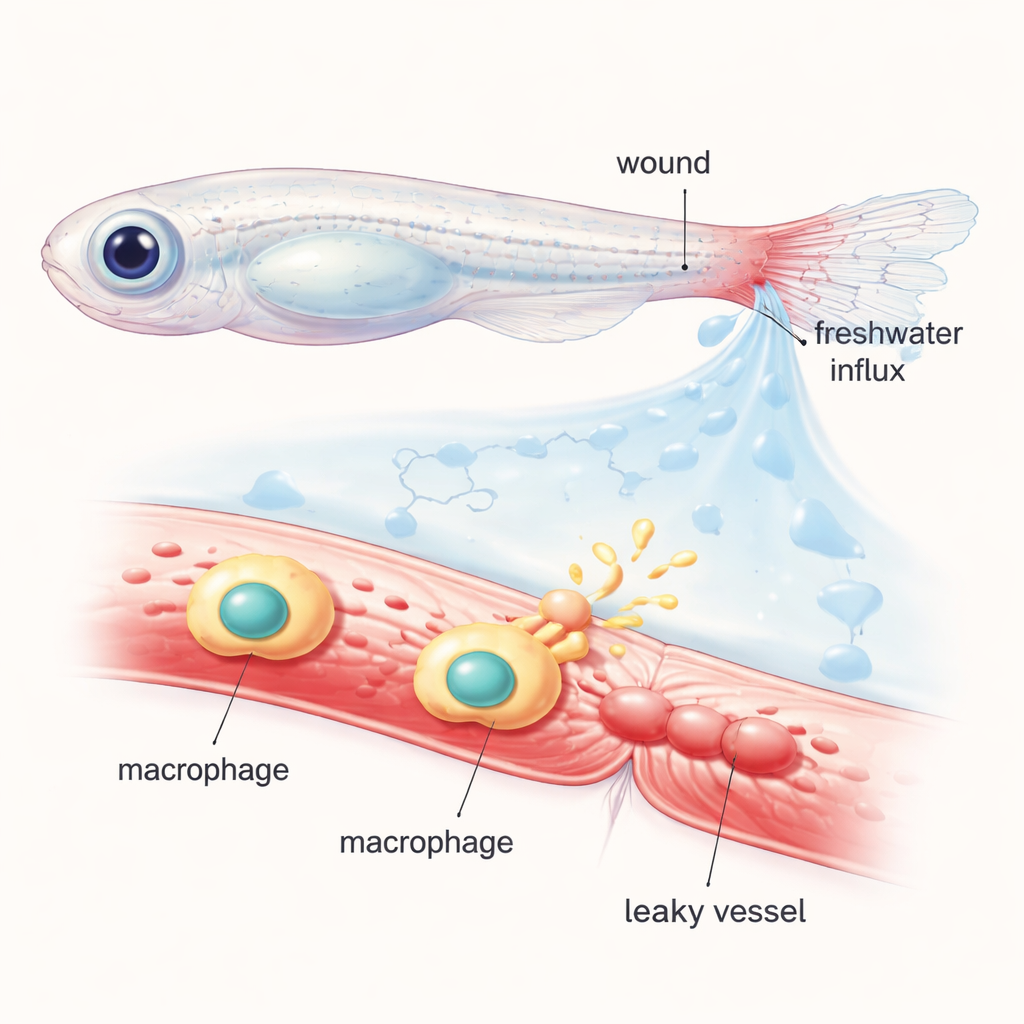
Sızdıran Kimyasal Haberciyi İzlemek
Fiziksel şoku sızıntı sinyaline çeviren hangi moleküller olduğunu belirlemek için bilim insanları, arakidonik asitten türeyen eikosanoid adlı yağlı bileşik ailesini incelediler. Bu lipidler iltihap ve kan akışı rolleriyle iyi bilinir. Genetik mutanlar ve ilaçlar kullanarak eikosanoid yolundaki belirli enzimleri seçici olarak devre dışı bıraktılar. Alox5a (5-lipoksijenaz) adı verilen kilit bir enzimi veya onun partneri Lta4h’yi engellemek, ozmotik şok sonrasında damarlardan ne kadar boyanın kaçtığını keskin biçimde azalttı; bununla birlikte yara kapanmasını durdurmadı. Buna karşılık, ilişkili diğer enzimlerin engellenmesi çok az etki gösterdi. Bu, hızlı sızıntı tepkisinin ana itici gücü olarak lipid yolunun belirli bir dalını işaret etti; neredeyse isteğe bağlı açılıp kapatılabilen kimyasal bir vana gibi davranıyor gibiydi.
Damarları Saran Bağışıklık Hücrelerinin Sürpriz Rolü
Kanda farklı tip bağışıklık hücreleri bulunur ve zebrabalığı larvalarında nötrofiller ile makrofajlar başlıca oyunculardır. Ekip, yaralanmadan önce ya nötrofilleri ya da makrofajları seçici olarak yok etmek için zeki bir genetik hile kullandı. Nötrofilleri kaldırmak damar sızıntısı üzerinde çok az fark yarattı. Ancak makrofajlar yok edildiğinde, sızıntı tepkisi yaklaşık yarı yarıya düştü; bu, Alox5a–Lta4h lipid yolunu engellemenin etkisini yansıtıyordu. Önemli olarak, bu müdahaleler yaranın hızla kapanmasını engellemedi; bu da lökosit çekilmesi ile damar sızıntısının bir dereceye kadar bağımsız olarak kontrol edilebileceğini gösteriyor. Bu, damar dışına sıkıca oturmuş perivasküler makrofajları—fiziksel hasar ile vasküler davranış arasında ana tercümanlar olarak—önemli aktörler olarak ortaya koydu.
Çekirdek Gerilmesinden Kimyasal Sinyale
Bu perivasküler makrofajlar uzaktaki bir yarayı nasıl algılıyor? Yanıt, çekirdeklerinin mekanik strese nasıl tepki verdiğinde yatıyor. Yaradan yayılan ozmotik şok yakındaki doku boyunca ilerlediğinde, su girişi hücrede hafif şişme ve çekirdek deformasyonuna neden olur. Araştırmacılar, mekanosensitif bir enzim olan cPla2’yi floresan bir işaretle etiketleyip bunu özel olarak makrofajlarda ifade ettiler. Normal tatlı suda yaralanma sonrası, cPla2 makrofajlarda nükleer zarın iç yüzeyine hızla taşındı; bu hareket doku boyunca yaklaşık saniyede 50 mikrometre hızla yayılan bir dalga şeklindeydi ve çözünmüş tuzların yayılımıyla uyumluydu. Bu translokasyon hipotonik koşullara bağlıydı ve izotonik çözeltilerde çok daha zayıftı. Kan damarlarına yakın makrofajlar özellikle keskin, geri döndürülebilir nükleer cPla2 bağlanma darbeleri gösterdi; bu da arakidonik asidin salgılanmasına ve sızıntı oluşturan lipidlerin dönüştürülmesine yol açtı.
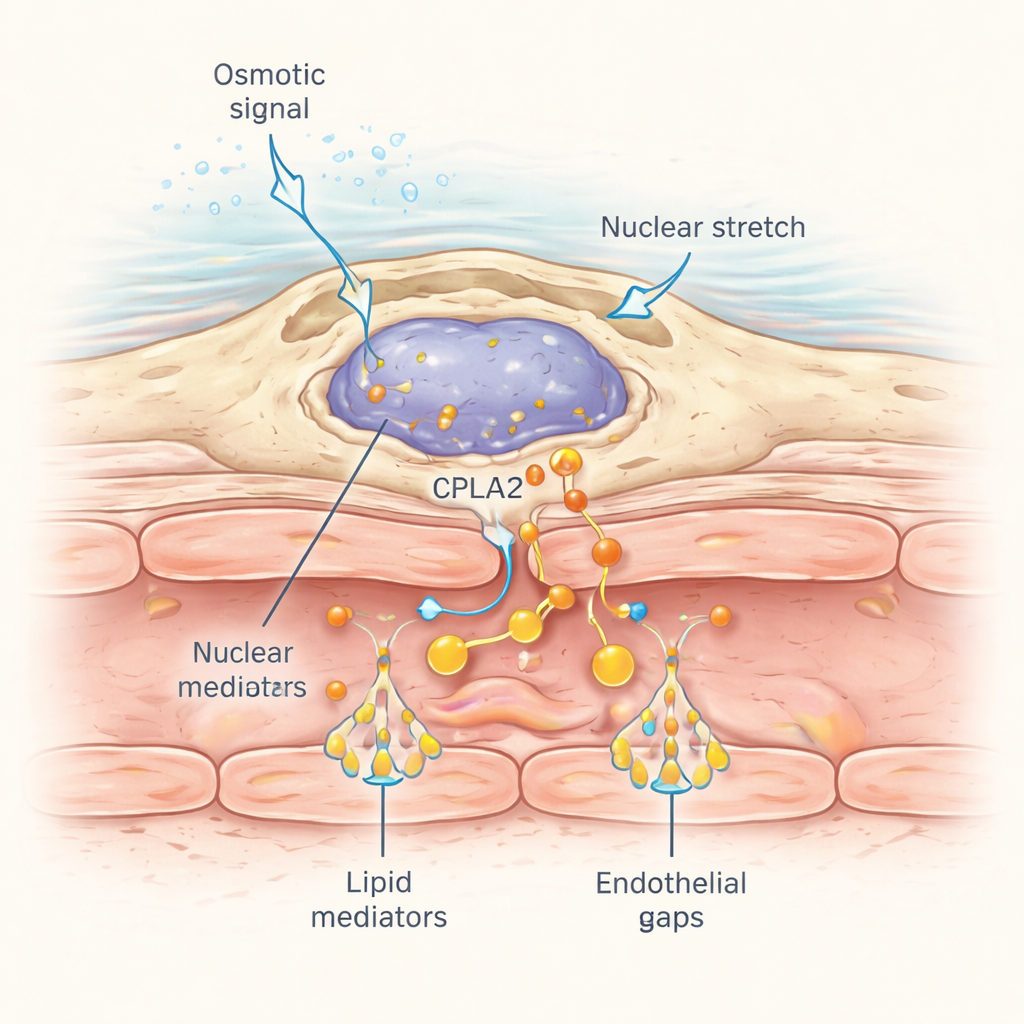
Balıkların Ötesinde Neden Önemli
Özetle bu çalışma, belirli makrofajların fiziksel nöbetçiler gibi davrandığını gösteriyor: yara çevresindeki ozmotik değişimlerin neden olduğu doku ve nükleer zar gerilimini hissediyor, nükleer yüzeylerinde cPla2’yi açıyor ve çevredeki kan damarlarına “kapıları açın” sinyali veren lipid habercileri hızla üretiyorlar; böylece sıvı ve bağışıklık faktörleri içeri akıyor. Zebrabalıkları tatlı suda yaşar ve benzersiz ozmotik zorluklarla karşılaşırlar, ancak benzer mekanosensitif yolların, mekanik ventilasyon sırasında akciğerler gibi değişen basınç ve akımlara maruz kalan insan dokularında da işlediği muhtemeldir. Nükleer gerilme ve lipid sinyallerinin damar geçirgenliğini gerçek zamanlı olarak nasıl kontrol ettiğini anlamak, zamanla akut akciğer yaralanması gibi durumlarda zararlı sızıntıyı hafifletmeyi ya da doku onarımını hızlandırmak için faydalı tepkileri güçlendirmeyi amaçlayan tedavilere ışık tutabilir.
Atıf: Gelashvili, Z., Shen, Z., Ma, Y. et al. Zebrafish macrophages convert physical wound signals into rapid vascular permeabilization. Nat Commun 17, 1807 (2026). https://doi.org/10.1038/s41467-026-68520-2
Anahtar kelimeler: yaralanma iyileşmesi, kan damarları, makrofajlar, iltihap, zebrabalığı