Clear Sky Science · tr
Mikrosaniye zaman çözünürlüklü kriyo-EM için ultraince sıvı hücreler
Proteinleri Gerçek Zamanlı Çalışırken İzlemek
Hücrelerimizi canlı tutan makinelerin çoğu proteinlerden oluşur ve bu proteinlerin donmuş hâllerinin nasıl göründüğünü sıklıkla biliriz. Ancak asıl görmek istediğimiz, görevlerini yaparken nasıl hareket ettikleridir. Bu çalışma, bu hareketleri inanılmaz kısa zaman ölçeklerinde—mikrosaniyeler düzeyinde—ve moderne kriyo-elektron mikroskobunun (kriyo-EM) sağladığı keskin ayrıntıdan ödün vermeden izlemenin yeni bir yolunu tanıtıyor.
Mikroskobik Dünyaya Yeni Bir Pencere
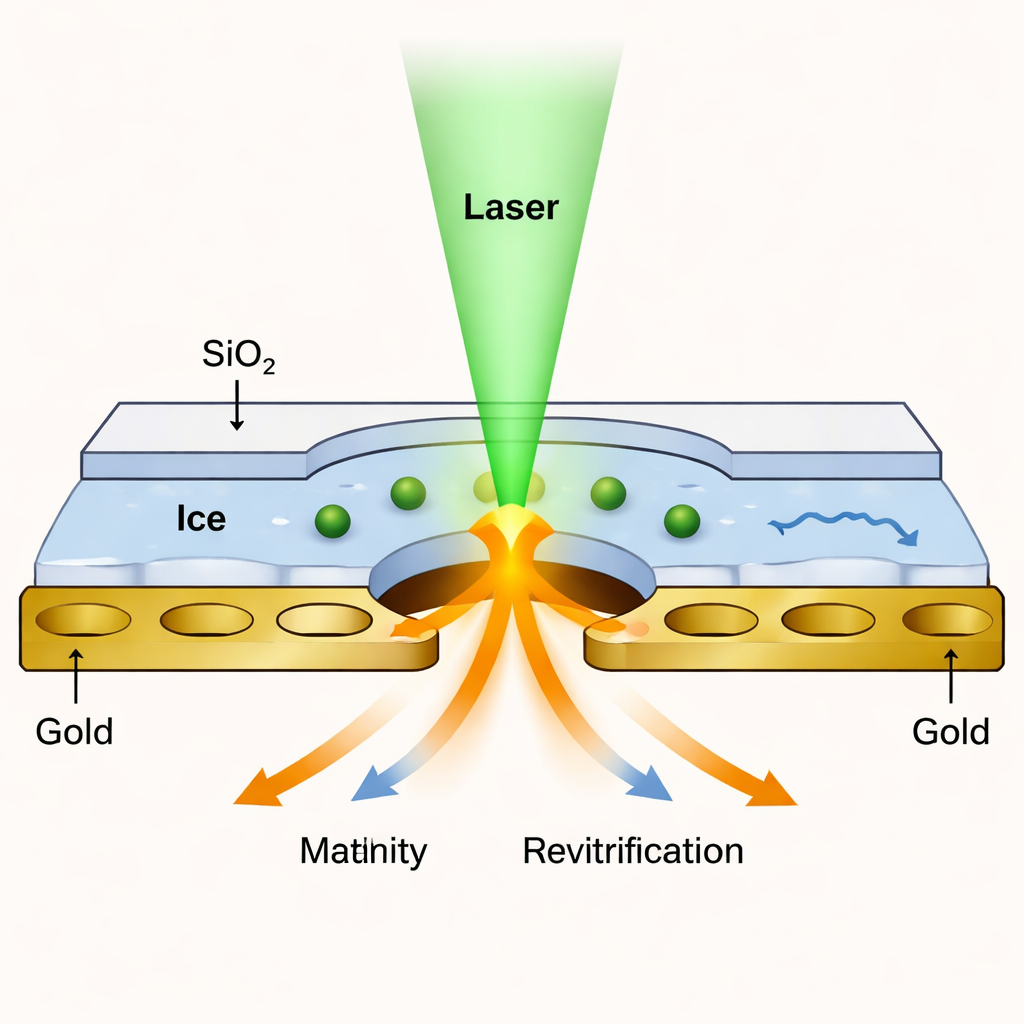
Kriyo-EM, yapısal biyolojide donmuş proteinleri neredeyse atomik çözünürlükte görüntüleyerek devrim yarattı. Ancak geleneksel yöntemler yalnızca hareketsiz görüntüler sunuyor. Hareketi yakalamak için araştırmacılar, donmuş bir örneği kısa süreliğine eritmek için bir lazer kullanan ve ardından proteinleri yeni konumlarda yakalamak üzere örneği hızla yeniden donduran “mikrosaniye zaman çözünürlüklü kriyo-EM” geliştirdiler. Sorun şuydu: lazerle oluşturulan çok ince sıvı film birkaç on mikrosaniye sonra parçalanma eğilimindeydi ve bu da proteinlerin ne kadar süre gözlemlenebileceğini sınırlıyordu. Yeni çalışma, örneği ultraince bir sıvı hücreyle kaplayarak bu darboğazı çözüyor ve daha yavaş, daha karmaşık hareketleri izleyecek kadar istikrar sağlıyor.
Ultraince Bir Sıvı Hücre İnşa Etmek
Ekip, nanoskopedik bir sandviç türü yarattı: protein çözeltisi standart delikli bir altın ızgaranın üzerine donduruluyor, ardından her iki taraf yaklaşık 1,4 nanometre kalınlığında—sadece birkaç atom—silikon dioksit tabakalarıyla kaplanıyor. Bu cam benzeri katmanlar, lazer buzları erittiğinde sıvının buharlaşmasını önleyen şeffaf kapaklar görevi görüyor. Kısa lazer darbeleri kapalı örneği kontrollü bir sıcaklığa ısıtıyor ve ardından mikrosaniyeler içinde yeniden donmasına izin veriyor. Membranlar bu kadar ince olduğundan, mikroskopun görüntü üretmesi için hâlâ yeterli elektron geçişine izin veriyor; böylece geleneksel kriyo-EM ile neredeyse aynı çözünürlüğü koruyarak test proteini apoferritin için yaklaşık 1,7–1,8 angström düzeyine kadar inilebiliyor.
Daha Keskin Görünümler ve Daha Adil Açılar
Kriyo-EM’de gizli bir sorun, proteinlerin ince buz tabakasındaki hava–su arayüzüne yapışma eğiliminde olmasıdır; bu da moleküllerin benzer yönelimlerde sıralanmasına ve tam 3B görünümün yeniden yapılandırılmasını zorlaştırır. Bu sıvı hücrelerdeki silikon dioksit kaplamalar yüzeyi su–hava yerine su–katı hâline çevirir ve suya karşı daha dostu yapar. Sonuç olarak, proteinlerin tek bir pozda yapışma olasılığı azalır. Yazarlar büyük bir hücresel makine olan 50S ribozomal alt ünitesini test ettiklerinde, parçacıkların açısal dağılımının neredeyse mükemmel şekilde eşit hale geldiğini; böylece uzun zamandır sorun olan “tercih edilen yönelim” neredeyse tamamen ortadan kalkarken nihai yeniden yapılandırmalarda yüksek çözünürlüğün korunduğunu buldular.
Moleküler Bir Kolu Zamanlamak
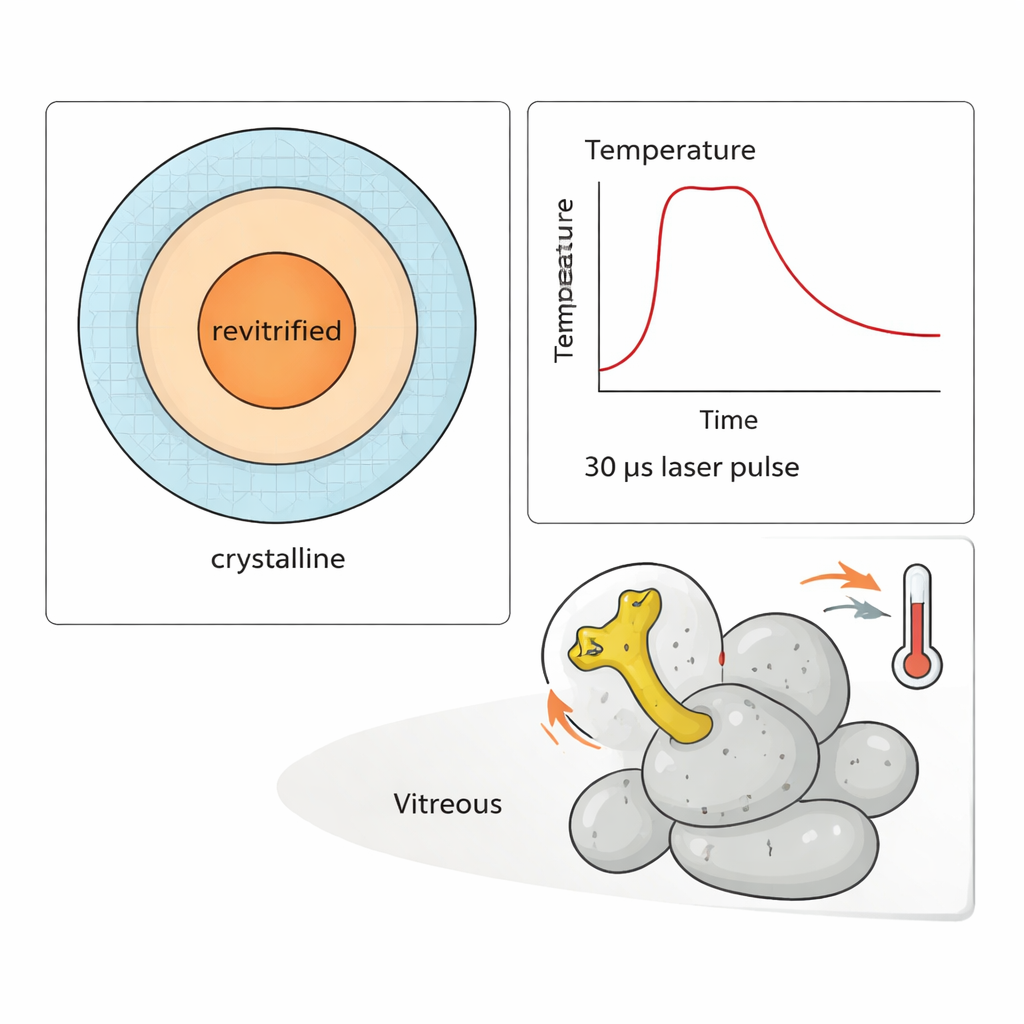
Yöntemlerinin gücünü sergilemek için araştırmacılar 50S alt ünitesi üzerinde bir “sıcaklık sıçraması” deneyi gerçekleştirdiler. Bu parçacıkta L1 sapı olarak bilinen esnek bir kol, protein sentezi sırasında bir kaldıraç gibi sallanır. 30 mikrosaniyelik lazer darbeleri dizileri vererek örneği yaklaşık 300 mikrosaniyeye kadar farklı sıcaklıklara ısıtıp sonra yeniden dondurabildiler. Hangi bölgelerin cam gibi yeniden donduğu üzerine yapılan simülasyonlar ve ölçümler, her gözlenen parçacık için sıcaklığı tahmin etmelerine olanak verdi. Binlerce görüntünün analizinde, L1 sapı hareketinin genliğinin açıkça sıcaklıkla arttığını gösterdiler—ancak bunun gerçekleşmesi yüzlerce mikrosaniye geçmesini gerektiriyordu. Erken zamanlarda konformasyon dağılımı hâlâ dondurmadan önceki oda sıcaklığı durumunu yansıtıyordu.
Gelecek Biyolojisi İçin Neden Önemli
Uzman olmayanlar için ana mesaj şudur: bu ultraince sıvı hücre tasarımı, proteinlerin hareket halinde ne kadar süre gözlemlenebileceğini yapısal ayrıntıları bulanıklaştırmadan dramatik biçimde uzatıyor. Bu, mikrosaniye zaman çözünürlüklü kriyo-EM’yi yalnızca en hızlı olayları yakalamaktan daha yavaş, biyolojik açıdan önemli yeniden düzenlemeleri incelemeye kaydırıyor; örneğin L1 sapının bir ısı darbesine geç yanıt vermesi gibi. Daha fazla iyileştirmeyle bu yaklaşım milisaniye aralığına ve ötesine köprü kurabilir; ayrıca örnek hazırlama, görüntüleme artefaktlarını azaltma ve reaksiyonları doğrudan ızgarada başlatma için yeni yollar sunar. Pratik olarak bu, bilim insanlarının protein şekillerini hücre içindeki gerçek işlevleriyle bağlayan “moleküler filmler” yapmaya daha da yaklaşması demektir.
Atıf: Curtis, W.A., Wenz, J., Krüger, C.R. et al. Ultrathin liquid cells for microsecond time-resolved cryo-EM. Nat Commun 17, 1799 (2026). https://doi.org/10.1038/s41467-026-68515-z
Anahtar kelimeler: zaman çözünürlüklü kriyo-EM, protein dinamikleri, sıvı hücre elektron mikroskobu, ribozom L1 sapı, ultraince silikon dioksit membranlar