Clear Sky Science · tr
Hücreler arası peptit kendi kendine örgülenmesinin mekanik kuvvetleri küre oluşumunu tetikliyor
Laboratuvarda Küçük Dokular İnşa Etmek
Bilim insanları, gerçek insan dokularına benzer davranış gösteren minyatür doku modelleri yaratmak için yarışıyor. Bu canlı modeller, kanser ilaçlarının daha güvenli test edilmesini sağlayabilir ve diyabet ile diğer hastalıklar için yeni tedavilerin gerçeğe dönüşmesini hızlandırabilir. Bu çalışma, hücreleri kendi içinde ilkel “damar benzeri” ağlara sahip gerçekçi üç boyutlu kümeler halinde toplanmaya yönlendiren zekice bir yöntem sunuyor; bu ağlar besin taşınmasını ve işlevi iyileştiriyor.
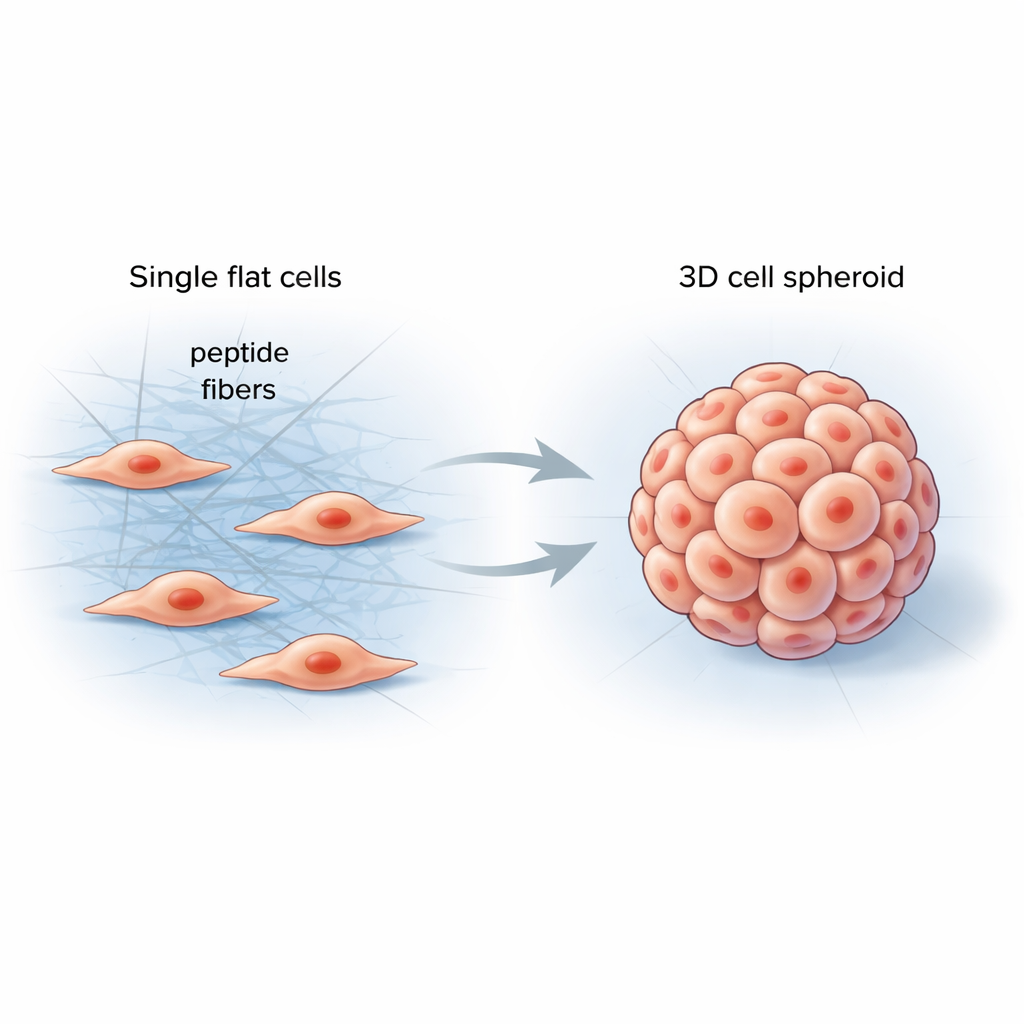
Hücrelerin Çevrelerini Hissetmelerine Yardım Etmek
Vücudumuz içinde hücreler, dokuları destekleyen ve hücrelere sürekli mekanik sinyaller gönderen proteinlerden oluşan yumuşak ama yapılı bir ortam olan ekstrasellüler matriks içinde yaşar. Geleneksel laboratuvar malzemeleri bu karmaşıklığı taklit etmekte zorlanır ve sıklıkla gerçek organlar ya da tümörlerden çok farklı davranan düz hücre katmanları üretir. Araştırmacılar, hücrelerin arasına doğrudan oluşacak, çevrelerini kontrollü şekilde sertleştirecek ve onları daha doğal üç boyutlu biçimlere yönlendirecek basit, programlanabilir bir malzeme tasarlamayı hedeflediler.
Hücreler Arasında Örgülenen Akıllı Peptitler
Ekip, hücre yüzeylerindeki belirli enzimlerle karşılaştıklarında birbirine bağlanıp uzun, ince lifler oluşturabilen kısa protein parçacıkları yani peptitler yarattı. Bu peptitler kanser hücrelerine eklendiğinde, başta şeffaf bir çözelti gibi etkisiz kaldılar. Hücrelerin kendi enzimleri molekülün bir kısmını budadığında, peptitler hızla komşu hücrelerin etrafını ve arasını saran fibroz bir ağ halinde kendi kendine örgülendi. Bu yeni lif ağı yerel mekanik kuvvetleri değiştirerek hücrelerin birbirlerini çekmesini, iç iskeletlerini yeniden düzenlemesini ve yayılıp bir tabaka oluşturmaktansa yuvarlak 3B küreler hâlinde toplanmasını teşvik etti.
Hücre Kümelerinden Damar Benzeri Ağlara
Gerçek dokuya daha yakınlaşmak için bilim insanları, normalde kan damarlarını döşeyen tip olan insan endotelyal hücreleri ve bu hücreleri çeken küçük bir “adres etiketi” taşıyan ikinci bir peptidi tanıttı. Orijinal ve değiştirilmiş peptitler birlikte ortak bir nanolif iskelesi oluşturdu. Endotelyal hücreler bu iskelesi kullanarak kürelerin etrafına ve içine sarmalanan tüp benzeri uzantılar oluşturdu ve kılcal damar benzeri yapılar meydana geldi. Araştırmacılar bu yapıların etrafından floresan şeker benzeri moleküller akıttıklarında, iç tüplerin olmadığı kürelere kıyasla küre çekirdeğine çok daha derin bir nüfuz gözlemlediler; bu da besin ve sinyal taşınımının belirgin şekilde iyileştiğini gösterdi.
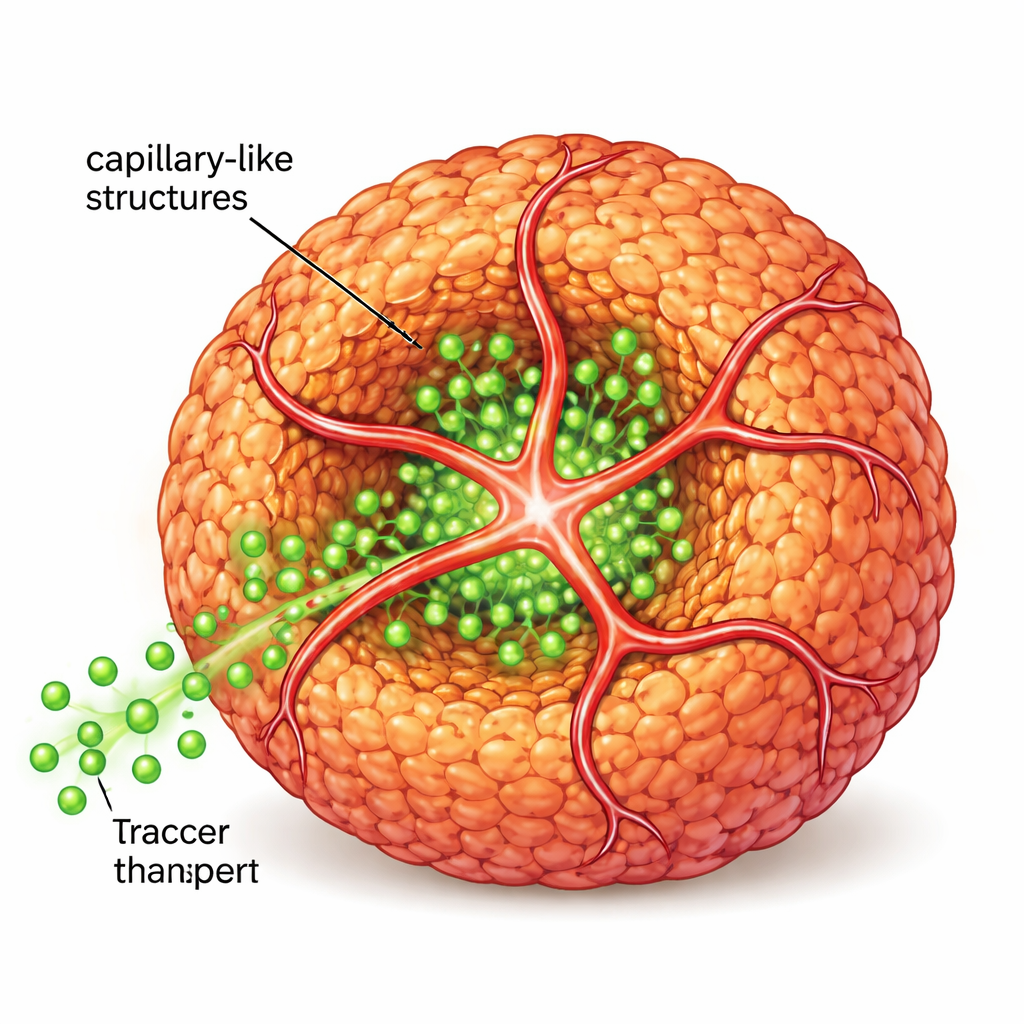
Gerçek Tümörlere ve Çalışan Adacıklara Daha Yakın
Gen aktivite profillemesi, kapiller benzeri yapılara sahip tümör kürelerinin geleneksel düz kültürlere veya damarsız kürelere göre hasta glioblastoma örneklerine daha yakın olduğunu ortaya koydu. Farelerde, bu ilkel damar ağlarını içeren küreler daha büyük ve daha damarlanmış tümörlere dönüştü; bu da in vitro modelin gerçek tümör davranışının temel özelliklerini yakaladığını gösteriyor. Aynı strateji, normalde yoğun şekilde damarlanmış adacıklarda bulunan ve glikoza yanıt olarak insülin salgılayan pankreatik beta hücrelerine uygulandı. Beta hücre küreleri peptit sistemi ve endotelyal hücrelerle kapiller benzeri yapılarla donatıldığında, çok daha güçlü ve hassas ayarlanmış insülin salınımı gösterdiler; bu da diyabet araştırmaları ve rejeneratif tıp için güçlü bir araç olduğunu düşündürüyor.
Gelecek Tedaviler İçin Bunun Önemi
Basit peptitlerin canlı hücreler arasında kendi kendine örgülenmesine izin vererek, bu çalışma vücut içindekilere daha çok benzeyen, küçük, damarlanmış dokular inşa etmek için genel bir tarif sunuyor. Ortaya çıkan küreler hasta tümörlerini ve çalışan adacıkları daha iyi yansıtıyor; bu da onları ilaç testi, hastalık mekanizmalarının incelenmesi ve yeni hücre tabanlı tedavilerin tasarımı için değerli kılıyor. Uzman olmayanlar için ana çıkarım, laboratuvarda yetiştirilen hücrelere “doğru hissi” vermenin ve küçük damar benzeri ağlar eklemenin, insan dokularını ne kadar sadık şekilde taklit ettiklerini dramatik biçimde iyileştirebileceği ve temel araştırmadan etkili tedavilere giden yolu hızlandırabileceğidir.
Atıf: Lu, H., Li, Y., Yang, X. et al. Mechanical forces from intercellular peptide self-assembly drive spheroid formation. Nat Commun 17, 1801 (2026). https://doi.org/10.1038/s41467-026-68513-1
Anahtar kelimeler: doku mühendisliği, kanser modelleri, anjiyogenez, organoidler, peptit kendi kendine örgülenme