Clear Sky Science · tr
TET1, akut miyeloid lösemide GPX4-bağımlı ve -bağımsız ferroptozis gözetimini kontrol eden ana düzenleyici olarak
Bu araştırma kanser tedavisi için neden önemli
Birçok yeni kanser ilacı, kötü huylu hücreleri demir ve yağ hasarının yol açtığı bir hücre ölümü türü olan ferroptozis adı verilen bir intihar modu başlatmaya yöneliktir. Ancak bazı tümörler bu yaklaşıma direnç gösterir. Bu çalışma, TET1 adlı DNA’yı değiştiren bir proteinin lösemi hücrelerinin ferroptozisten iki ayrı biyokimyasal savunma sistemi aracılığıyla kaçmasına nasıl yardım ettiğini ortaya koyuyor—ve bu savunmaların engellenmesinin, dirençli kanserleri bile hassas hale getirebileceğini gösteriyor.
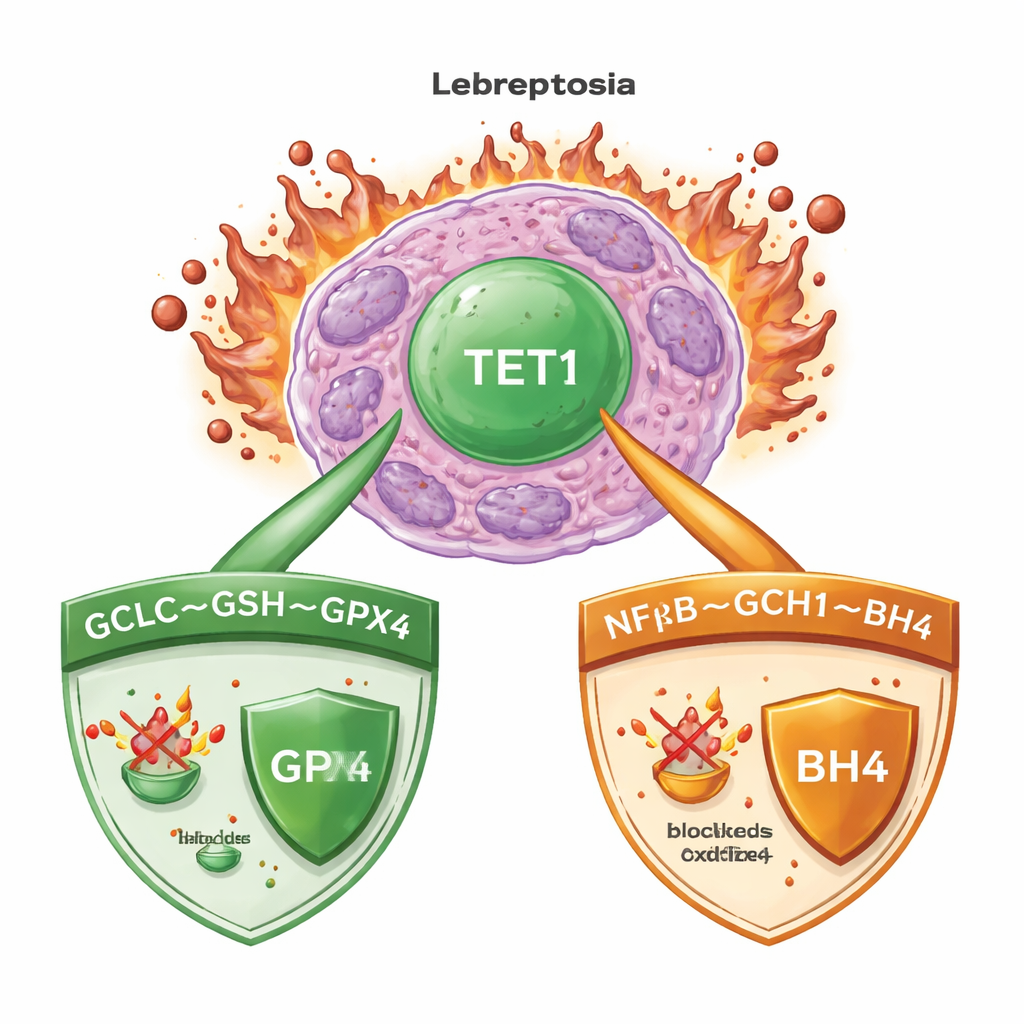
Demir ve hasarlı yağların ölümcül karışımı
Ferroptozis, demirin hücre zarlarındaki yağların kontrolsüz oksidasyonunu beslemesi ve nihayetinde hücrelerin parçalanmasına yol açmasıyla gerçekleşir. AML’de (akut miyeloid lösemi) ve birçok kanserde hücreler bu süreci denetim altında tutmak için güçlü gözetim sistemleri kullanır. Ana koruyuculardan biri, zararlı lipid peroksitlerini nötralize etmek için küçük bir molekül olan glutatyonu kullanan GPX4 enzimidir. Yedek diğer sistemler, GPX4 bozulduğunda bile tehlikeli radikalleri yakalayabilen antioksidan moleküller üretir. Hangi anahtar anahtarların bu savunmaları koordine ettiğini anlamak, kanser hücrelerinde güvenilir bir şekilde ferroptozis tetikleyen ve sağlıklı dokuyu koruyan tedaviler tasarlamak açısından çok önemlidir.
TET1 merkezi kontrol düğümü olarak öne çıkıyor
Araştırmacılar, birçok AML hattı ve hastadan türetilen hücreler de dahil olmak üzere onlarca kanser hücre örneğini karşılaştırdı ve belirgin bir desen fark ettiler: ferroptozise dirençli hücrelerde TET1 düzeyleri daha yüksekti. TET1, DNA kimyasal işaretlerini değiştiren ve gen etkinliğini etkileyen bir enzimdir. Genetik araçlarla TET1 seviyelerini azalttıklarında veya küçük bir molekülle aktivitesini engellediklerinde, kanser hücreleri ferroptozis tetikleyici ilaçlara karşı belirgin şekilde daha hassas hale geldi. Bu durum hem laboratuvar kaplarında hem de AML’nin fare modellerinde gözlendi. Tersine, TET1 ifadesinin artırılması hücreleri ferroptotik ölümden korudu ve zar hasarına yol açan kimyasal olarak agresif yan ürünlerin (reaktif oksijen türleri) birikimini sınırladı.
Ana antioksidan kalkanın güçlendirilmesi
Daha derine indiklerinde, ekip TET1’in genom üzerindeki etkilediği yerleri haritaladı ve doğrudan GCLC adlı bir geni aktive ettiğini buldu. GCLC, GPX4 için yakıt olan glutatyon üretimini başlatan kritik bir enzimi kodlar. GCLC promotorunda belirli bir DNA işareti (5-hidroksimetilsitozin) artışı yaparak TET1, glutatyon sentezini artırır. Normal besin koşullarında bu, hücrenin ana antioksidan deposunu güçlendirir. Sistin yetersizliğinde aynı enzim kompleksi, fazladan glutamati temizlemeye yardımcı olan olağandışı γ-glutamil–peptitler de üretir; bu da ferroptozisi zayıflatmanın başka bir yoludur. Hem kültürdeki hücrelerde hem de farelerde TET1 kaybı veya glutatyon sentezinin farmakolojik olarak inhibisyonu, glutatyon düzeylerini ve bu koruyucu peptitleri keskin şekilde düşürdü ve lösemi hücrelerini ferroptozis tetikleyicilerine karşı çok daha savunmasız bıraktı.
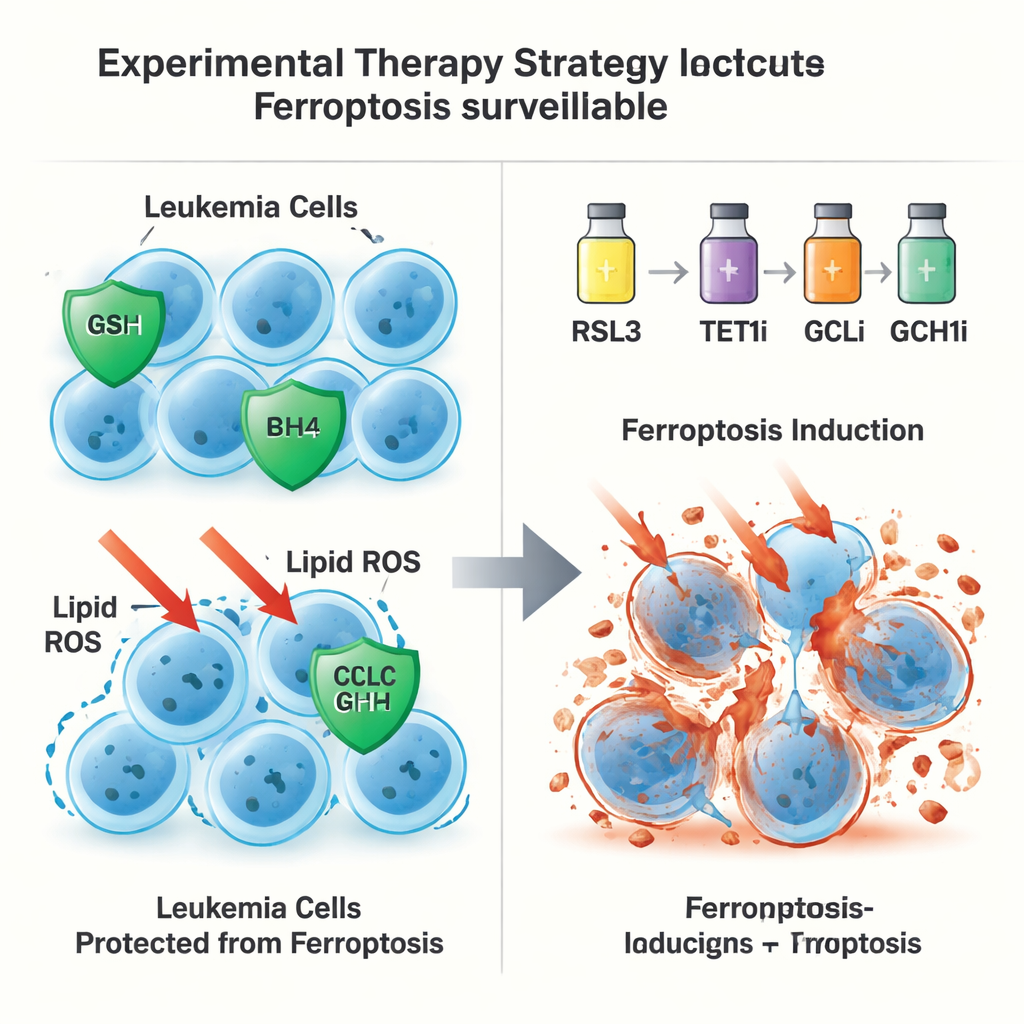
İkinci, GPX4-bağımsız kaçış yolu
Şaşırtıcı biçimde, TET1’in koruyucu rolü glutatyon–GPX4 ekseniyle sınırlı kalmadı. GPX4 lösemi hücrelerinden çıkarıldığında bile fazladan TET1 ferroptotik ölümü önleyebiliyordu; bu da ikinci bir savunma hattına işaret ediyordu. Yazarlar bunun, TET1’in NFκB sinyal yolunu, özellikle NFKB2 adlı bileşeni aktive etmesine dayandığını izledi. Bu da GCH1 ifadesini artırır; GCH1, antioksidan molekül BH4’ü üreten bir enzimi kodlar. BH4, GPX4’e ihtiyaç duymadan zar lipidlerini oksidasyondan koruyabilir. GCH1 genetik olarak susturulduğunda veya kimyasal olarak bloke edildiğinde, TET1’in ferroptozisten hücreleri koruma yeteneği kısmen kayboldu. Birlikte, bu bulgular TET1–NFKB2–GCH1 yolunu GPX4-bağımsız bir ferroptozis gözetim sistemi olarak tanımlar.
Bir zayıflığı terapi fırsatına dönüştürmek
Çift yollu haritaya sahip olan araştırmacılar, aynı anda ferroptozisi teşvik etmenin ve TET1 kontrollü savunmaları zayıflatmanın terapötik bir avantaj sağlayıp sağlamayacağını test etti. Fare AML modellerinde ve farelerdeki hasta kaynaklı lösemi greftlerinde, düşük doz ferroptozis tetikleyici bir ilaç TET1, GSH sentezi (GCLC üzerinden) veya GCH1 inhibitörleri ile birlikte verildiğinde lösemi yükü dramatik şekilde azaldı, yaşam süresi uzadı ve lösemi başlatıcı hücre popülasyonları tükendi. Önemli olarak, ferroptozisi tetikleyen ilaç önceki çalışmalarda bildirilen dozların bir kısmı düzeyinde kullanıldı; bu da normal kan kök hücrelerine yönelik toksisite endişelerini azaltıyor.
Geleceğin kanser tedavileri için ne anlama geliyor
Uzman olmayanlar için ana mesaj, lösemi hücrelerinin TET1 tarafından koordine edilen iki örtüşen antioksidan “kalkan” sistemi çalıştırarak hayatta kaldığıdır: biri glutatyon ve GPX4 merkezli, diğeri GCH1 ve BH4 temelli. Bu çalışma, ferroptozisi ılımlı şekilde aktive ederken aynı zamanda TET1 ve onun aşağı akış ortaklarını engellemenin, doktorların bir gün direnci aşarak kanser hücrelerini seçici olarak öldürebilmelerini sağlayabileceğini, sağlıklı dokuyu fazla zorlamadan gösterebileceğini ortaya koyuyor. Bu stratejiler henüz klinikte hazır olmasa da çalışma, TET1’i güçlü bir kontrol düğümü ve AML ile potansiyel olarak tedavisi zor diğer kanserlerde kombinasyon tedavileri için ümit vaat eden bir hedef olarak tanımlıyor.
Atıf: Yang, L., Lu, J., Yun, W. et al. TET1 as a master regulator controlling GPX4-dependent and -independent ferroptosis surveillance in acute myeloid leukemia. Nat Commun 17, 1800 (2026). https://doi.org/10.1038/s41467-026-68509-x
Anahtar kelimeler: ferroptozis, akut miyeloid lösemi, TET1, glutatyon, kanser epigenetiği