Clear Sky Science · tr
Mono-alkil-hidroksilamin ve siklooktin kimyası kullanan tıklama-serbest bırakma sistemi ile zamansal ve mekânsal kontrollü ilaç salımı
Güçlü İlaçları Sadece Gerektiği Yerde Açık Hale Getirmek
Günümüzün birçok ilacı son derece etkili; bu, kanserle mücadele veya ağrı gidermede avantaj sağlasa da vücudun geri kalan kısmı için risk oluşturur. Bu çalışma, bilim insanlarının ilaçları etkisiz, zararsız bir biçimde “park etmelerine” ve sonra yalnızca seçilmiş bir yer ve zamanda—örneğin bir tümörün içinde ya da lokal anestezi gereken küçük bir bölgede—etkinleştirmelerine olanak veren kimyasal tabanlı bir “açma-kapama anahtarı”nı anlatıyor.
Yeni Bir Kimyasal Anahtar Türü
Araştırmacılar, hızlı, hassas ve canlı organizmalar içinde güvenle çalışabilen reaksiyonlar olarak değer verilen “tıklama kimyası” kavramının üzerine inşa ediyor. Klasik tıklama reaksiyonları iki molekülü kalıcı olarak birleştirir. Burada ekip bu mantığı tersine çeviriyor: onların tıklama reaksiyonu doğrudan bir bağı kırmaya ve bir ilacı ya da sinyal molekülünü serbest bırakmaya bağlı. Kilit bileşenler, siklooktin adlı halka şeklinde bir molekül ile mono-alkil-hidroksilamin adlı küçük bir ortak. Bu ikisi karşılaştığında, hızla birbirine bağlanıyor ve ardından bağlı “yük” serbest bırakılacak şekilde yeniden düzenleniyor. Farklı ilaçlar veya floresan boyalar yük olarak bağlandığında, aynı temel reaksiyon birçok amaç için yeniden kullanılabiliyor. 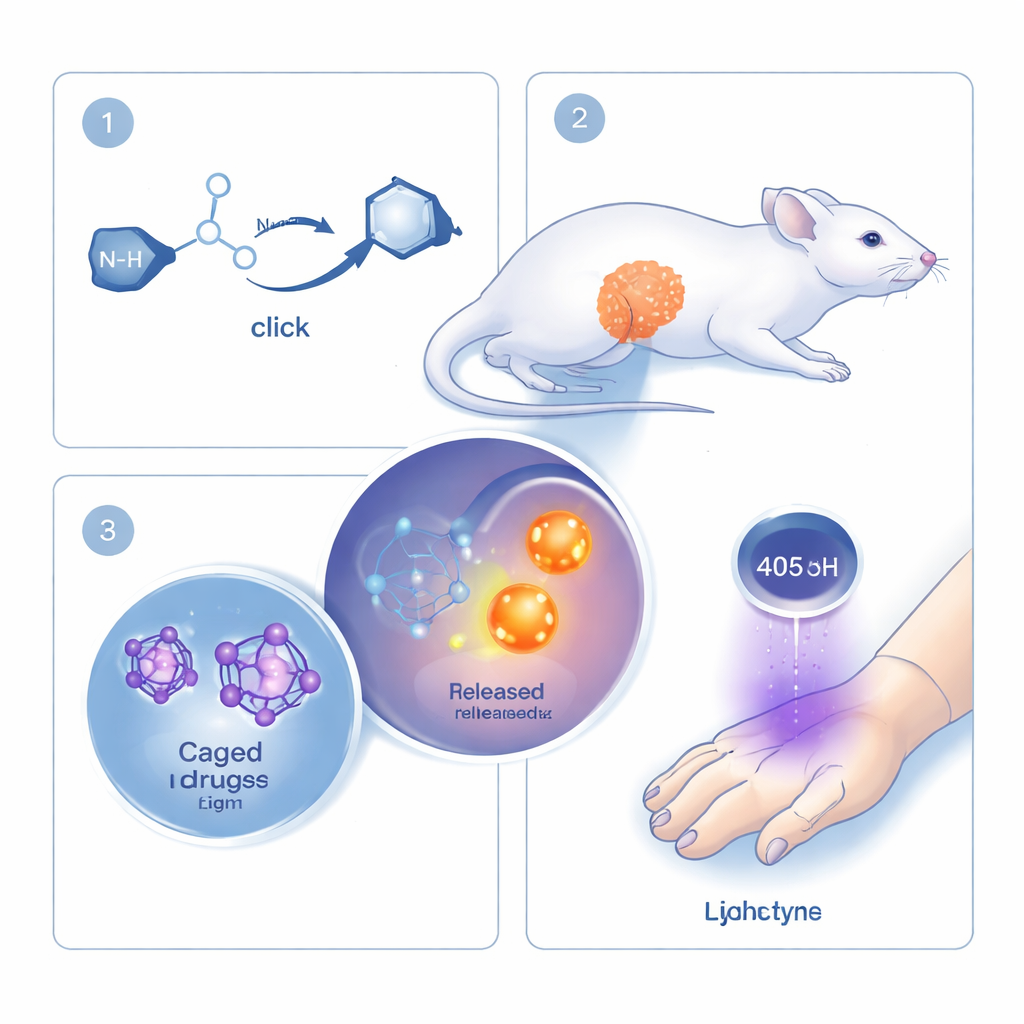
Hücre İçinde ve Dışında Hızlı, Temiz Salım
Bu anahtarın uygulanabilir olduğunu doğrulamak için ekip, reaksiyonun ne kadar hızlı ilerlediğini ve bağlı yükü ne kadar eksiksiz serbest bıraktığını ölçtü. Özenle seçilmiş mono-alkil-hidroksilaminlerin basit hidroksilamine göre çok daha hızlı reaksiyona girdiğini ve yapıya bağlı olarak dakikalar ila saatler içinde neredeyse tam dönüşüm sağladığını buldular. Önemli olarak, yükü gerçekten serbest bırakmaya yol açan kimyasal adımlar o kadar hızlı ve seçiciydi ki bağlı molekülün neredeyse tamamı açığa çıkıyor ve atık yan ürün neredeyse yok denecek kadar az. Yazarlar floresan boyalar ve hatta florür iyonu gibi çeşitli yükleri test etti ve sistemin karbamatlar ve eterler gibi ilaç tasarımında sık kullanılan birkaç ortak bağ türünü koparabildiğini gösterdi.
Hücreleri Aydınlatmak ve Kanser İlaçlarını Talep Üzerine Aktive Etmek
Ardından araştırmacılar canlı hücrelere geçti. Önce parlak floresan boyaları kimyasal anahtarın arkasına sakladılar ve bu “kafeslenmiş” probları kanser hücrelerine eklediler. Tek başına prob karanlık kaldı; bu, hücrelerin bunları kazara aktive etmediğini gösterdi. Mono-alkil-hidroksilamin ortağı eklendiğinde boyalar serbest kaldı ve hücreler mavi, yeşil veya yakın kızılötesi renklerde ışıldadı; bu, reaksiyonun biyolojik bir ortam içinde güvenilir şekilde çalıştığını doğruladı. Aynı fikri yaygın kullanılan kemoterapi ilacı doksorubisine uyguladılar. Kafeslenmiş formunda doksorubisin proilacı hücreler için çok daha az toksikti. Ancak tıklama ortağı mevcut olduğunda etkin ilaç verimli biçimde serbest kaldı ve serbest doksorubisin kadar güçlü olmasa da neredeyse aynı düzeyde kanser hücrelerini öldürme yeteneğini geri getirdi.
Yer ve Zaman İçin Akıllı Tetikleyiciler Oluşturma
Mevcut birçok tıklama tabanlı sistemin sınırlamalarından biri, reaktif parçaların her zaman “açık” olmasıdır; bu da tam olarak nerede ve ne zaman devreye gireceklerini kontrol etmeyi zorlaştırır. Bunu çözmek için ekip, mono-alkil-hidroksilaminin reaktivitesini küçük koruyucu kapaklarla geçici olarak bloke etti; bu kapaklar yalnızca belirli tetikleyicilerle çıkarılıyordu. Yüksek glutatyon düzeylerine (birçok tümörde bol bulunan küçük bir molekül), enzimlere ve menekşe ışığı flaşlarına yanıt veren versiyonlar yarattılar. Hücrelerde ve tümörlü farelerde glutatyon-duyarlı versiyon normal koşullarda sessiz kaldı ama tümörün kimyasal olarak indirgenmiş ortamında açıldı; floresan boyaları serbest bıraktı veya doksorubisin proilacını tümörün bulunduğu yerde aktive etti. Proilac artı tetikleyici kombinasyonuyla tedavi edilen farelerde, standart doksorubisine kıyasla tümör küçülmesi daha güçlü olurken kalp gibi hassas organlarda ilaç maruziyeti daha azdı.
Işıkla Uzaktan Kontrollü Lokal Anestezi
Zaman kontrolünü sergilemek için yazarlar ikinci bir uygulama tasarladı: ışıkla yönlendirilen lokal anestezi. Ağrı giderici tetrakaini siklooktin iskeletlerine bağlayarak onu inaktif hale getirdiler ve bu proilacı sıcaklık-duyarlı bir jeldeki ışığa duyarlı hidroksilamin versiyonuyla karıştırdılar. Bir sıçan patisine enjekte edildiğinde, karışım deri 405 nanometre ışıkla aydınlatılana kadar hiçbir etki göstermedi. Aydınlatma, tıklama-serbest bırakma reaksiyonunu tetikledi, tetrakaini serbest bıraktı ve doğrudan tetrakain enjeksiyonundan elde edilene benzer bir uyuşukluk üretti. Işığın süresini ve yoğunluğunu değiştirerek araştırmacılar sinir bloğunun ne kadar sürdüğünü ayarlayabildiler ve tek bir enjeksiyondan tekrar eden anestezi dalgaları tetikleyebildiler. 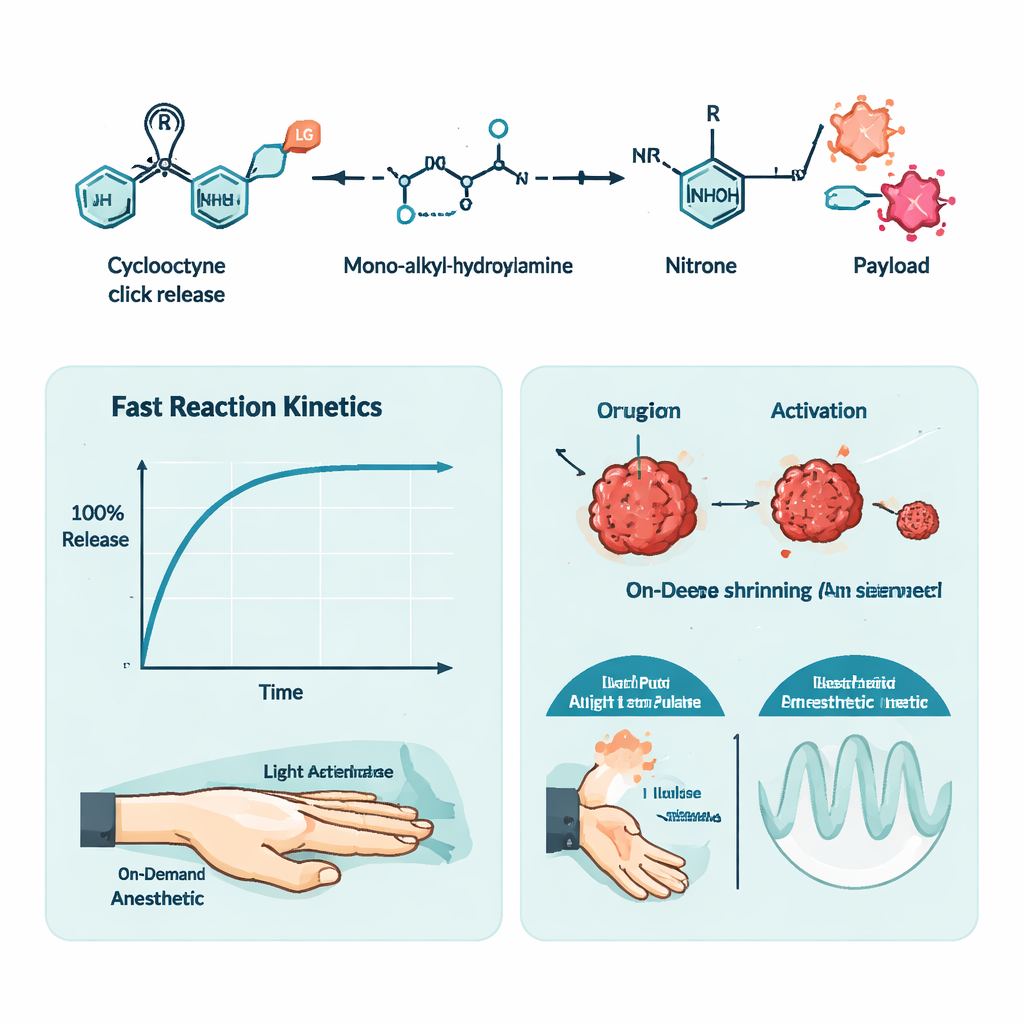
Gelecek Tedaviler İçin Ne Anlama Gelebilir
Uzman olmayanlar için ana mesaj, bu çalışmanın ilaçlar için esnek bir kimyasal uzaktan kumanda sunduğudur: ilaçlar güvenli, sessiz bir formda verilip yalnızca doğru yer ve zamanda, ya vücudun kendi sinyalleriyle ya da dış kaynaklı bir ışıkla aktive edilebilir. Klinik kullanıma geçmeden önce daha fazla test gerekse de, bu yaklaşım nihayetinde kanser tedavilerini daha hedefli ve daha az toksik hale getirebilir, ameliyat sonrası kişiselleştirilebilir ağrı kontrolü sağlayabilir ve hassas zamansal ve mekânsal kontrolden yararlanacak başka birçok tedaviye destek verebilir.
Atıf: Xu, X., Tong, X., Shi, Y. et al. Spatiotemporally controlled drug release via a click-release system utilizing mono-alkyl-hydroxylamine and cyclooctyne chemistry. Nat Commun 17, 1794 (2026). https://doi.org/10.1038/s41467-026-68502-4
Anahtar kelimeler: tıklama kimyası, hedefe yönelik ilaç teslimi, proilaçlar, tümör mikroçevresi, ışık kontrollü anestezi