Clear Sky Science · tr
UFL1-AKT kaskadını hedeflemek üçlü negatif meme kanseri ilerlemesini baskılıyor
Bu araştırma neden önemli
Üçlü negatif meme kanseri (TNBC), birçok modern ilacın hedeflediği hormon ve büyüme faktörü anahtarlarından yoksun olduğu için en ölümcül meme kanseri türlerinden biridir. Hastalar sıklıkla yalnızca geleneksel kemoterapi alır; ancak tümörler direnç geliştirdikçe bu tedaviler etkisini yitirebilir. Bu çalışma, TNBC hücrelerinin büyümesine ve kemoterapiye karşı direnmelerine yardımcı olan daha önce gizli bir moleküler “motoru” ortaya koyuyor ve bu motoru doğrudan kilitleyen yeni bir ilaç türü öneriyor.
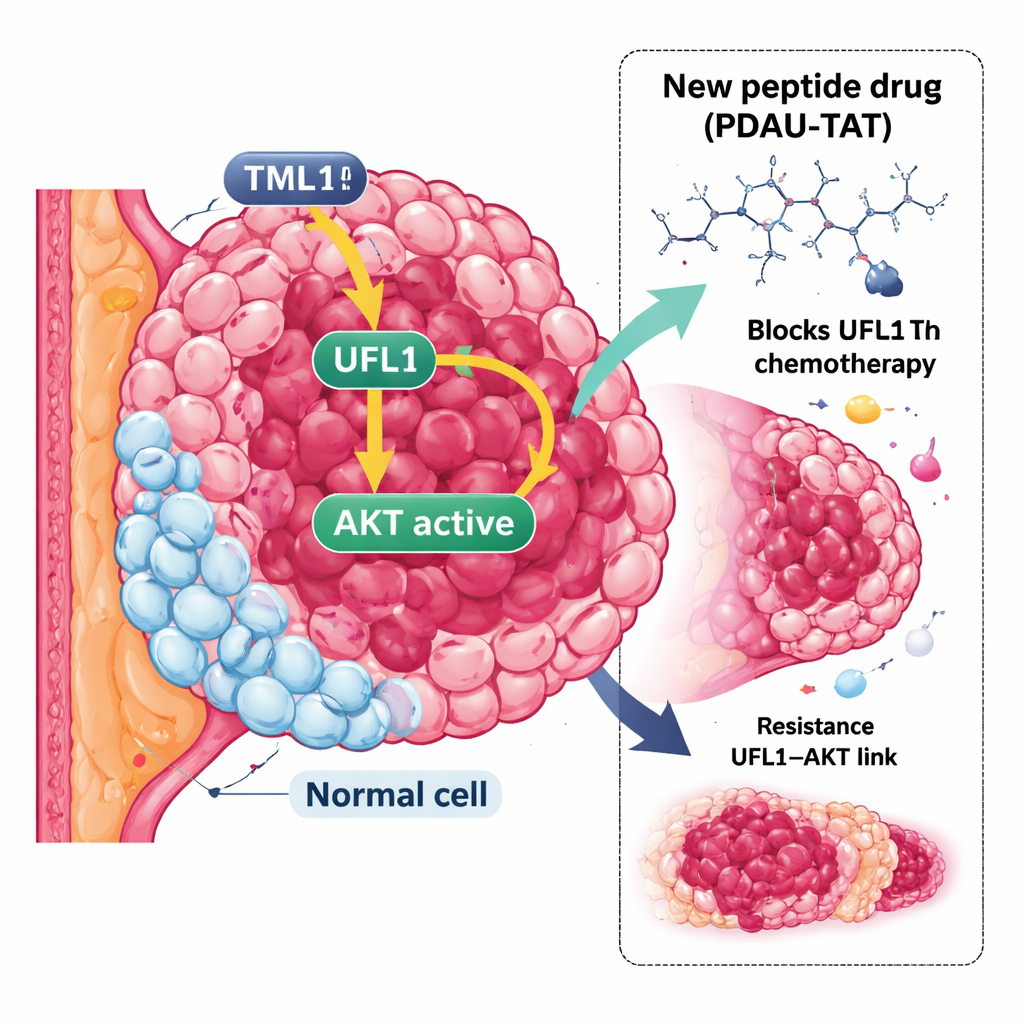
Müdahaleye dirençli bir meme kanseri türü
TNBC, üç yaygın belirteçten — östrojen reseptörü, progesteron reseptörü ve HER2 büyüme reseptörü — yoksun olmasıyla tanımlanır. Bu belirteçler olmadığında, birçok başarılı hedefe yönelik tedavi uygulanamaz. Bunun yerine cisplatin ve doksorubisin gibi standart ilaçlar kullanılır, ancak TNBC tümörleri sıklıkla bu tedavilere direnç gösterir veya hızla uyum sağlar ve daha kolay yayıldıkları görülür. Bu durum, sıradan hedeflerin ötesine geçip tümörün kontrol sistemlerindeki başka zayıf noktaları arayan yeni stratejilere acil ihtiyaç olduğunu ortaya koyar.
Az bilinen ama büyük etkili bir protein
Araştırmacılar, diğer proteinlere UFM1 adında küçük bir etiketi takan ve UFMylasyon olarak bilinen süreçte rol oynayan UFL1 proteinine odaklandı. Bu etiketleme sistemi yeni keşfedildi ve kanser bağlamındaki rolü belirsiz ve bazen çelişkiliydi. Hasta verilerini ve tümör örneklerini analiz ederek ekip, UFL1’in normal meme dokusuna kıyasla TNBC’de belirgin şekilde yükseldiğini gösterdi. TNBC hücre hatlarında ve fare tümör modellerinde UFL1 düzeylerini azaltınca, kanser hücreleri daha yavaş çoğaldı ve kemoterapiye karşı çok daha duyarlı hale geldi; bu da UFL1’in bu bağlamda tümörü destekleyen bir rol oynadığını düşündürüyor.
UFL1’i bir ana büyüme anahtarıyla bağlamak
Daha derine inen bilim insanları, UFL1’in hücre büyümesini, hayatta kalmayı ve metabolizmayı yönlendiren merkezi bir sinyal proteini olan AKT’ye doğrudan bağlandığını keşfettiler. AKT genellikle kanserlerde aşırı aktiftir; TNBC’de ise olağan yukarı akıştaki mutasyonlar yokken bile sıklıkla fazla aktiftir. Ekip, UFL1’in AKT’i üç belirli konumda kimyasal olarak etiketlediğini ve bunun da AKT’nin etkinleştiriciler tarafından açılmasını kolaylaştırdığını, aynı zamanda normalde onu kapatacak enzimlerden koruduğunu buldu. UFL1’den yoksun hücreler veya bu etiketleri alamayan tasarımlı AKT ifade eden hücreler, hem hücre kültürlerinde hem de hayvan modellerinde çok daha düşük AKT aktivitesi, daha yavaş büyüme ve kemoterapiye karşı artmış hassasiyet gösterdi.
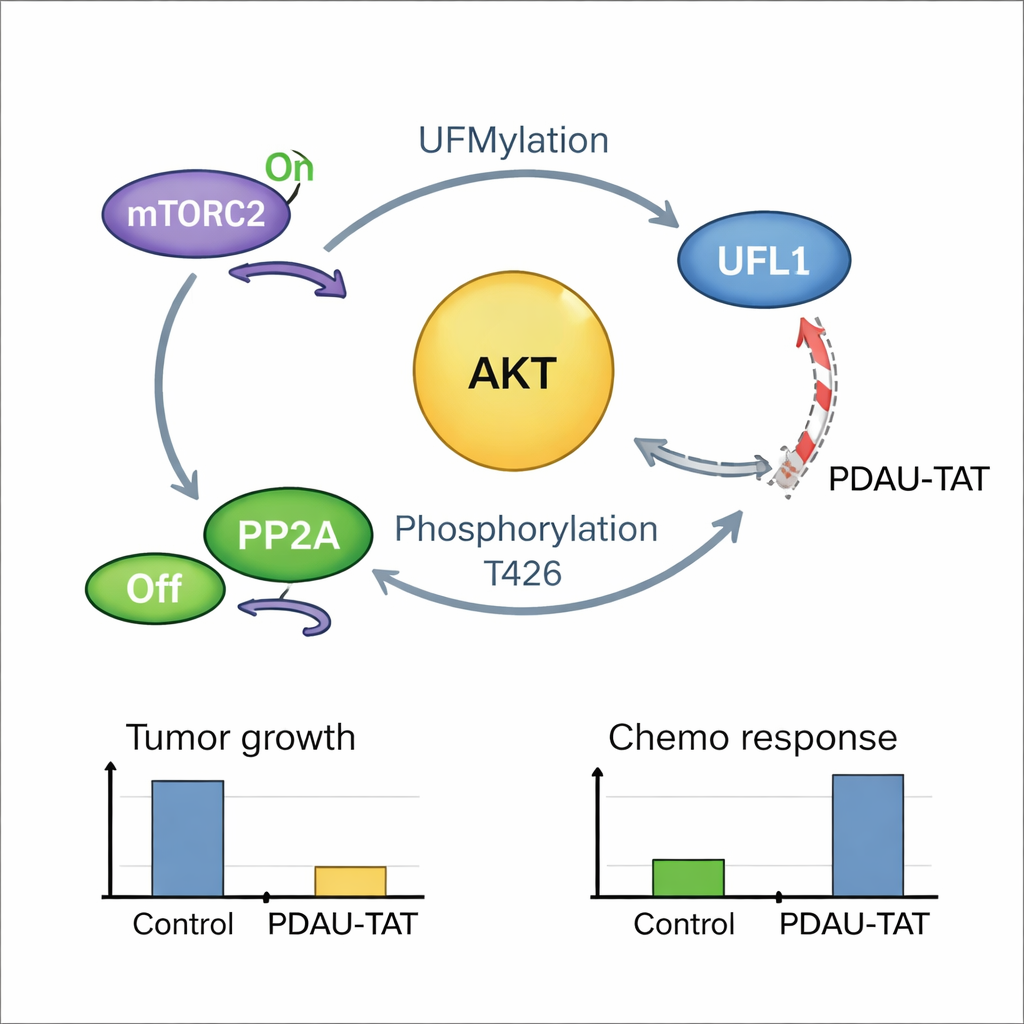
Kendini güçlendiren bir kanser döngüsü ve bunu kırmanın yolu
Hikâye daha da sıkı bağlandı: AKT bir kez aktifleştiğinde, UFL1’i tek bir kritik bölgede geri beslemeyle modifiye ederek UFL1’in AKT ve diğer hedefler üzerindeki etiketleme aktivitesini artırıyor. Bu, UFL1’in AKT’yi aktifleştirdiği ve aktif AKT’nin karşılığında UFL1’i süper şarj ettiği pozitif bir geri besleme döngüsü yaratıyor. Hasta tümör örnekleri, modifiye olmuş yüksek düzeyde UFL1’in yüksek düzeyde aktif AKT ile güçlü bir korelasyon gösterdiğini ortaya koyarak bu döngünün insan hastalığında da varlığını destekliyor. Bu zayıflıktan yararlanmak için ekip, UFL1’in küçük bir bölgesini taklit eden ve UFL1 ile AKT arasına giren kısa, hücre geçirgen bir peptid olan PDAU-TAT’ı tasarladı. Bu peptid, etkileşimi bozuyor, AKT aktivasyonunu azaltıyor, tümör büyümesini yavaşlatıyor ve TNBC hücrelerini ile hasta kaynaklı tümörleri kemoterapiye daha duyarlı hale getiriyor; farelerde önemli organlara belirgin zarar vermedi.
Bu hastalar için ne anlama gelebilir
Basitçe söylemek gerekirse, araştırmacılar TNBC hücrelerinin içinde gizli bir devre şeması keşfettiler: UFL1 ve AKT, büyüme sinyallerini sürekli “açık” konumda tutan ve tümörlerin tedaviye direnmesine yardımcı olan kendini güçlendiren bir döngüde kilitlenmiş durumda. UFL1’i AKT’ten ayıran küçük bir peptid geliştirerek, araştırmacılar normal hücrelere göre genellikle daha düşük UFL1 düzeyine sahip olan sağlıklı dokuları korurken TNBC tümörlerini zayıflatmanın makul bir yolunu gösteriyor. Bu çalışma hâlâ preklinik aşamada olmasına rağmen, sıradan reseptörleri hedef almak yerine bazı agresif meme kanserlerini güçlendiren protein–protein bağlantılarına yönelik yeni bir hedefli terapi sınıfına işaret ediyor.
Atıf: Yang, X., Wen, Y., Ma, X. et al. Targeting the UFL1-AKT cascade suppresses triple-negative breast cancer progression. Nat Commun 17, 613 (2026). https://doi.org/10.1038/s41467-026-68493-2
Anahtar kelimeler: üçlü negatif meme kanseri, AKT sinyalleşmesi, UFMylasyon, UFL1, peptid kanser tedavisi