Clear Sky Science · tr
UFL1‑AKT pozitif geri besleme döngüsü, lipid sentezini artırarak meme kanseri ilerlemesini destekliyor
Neden kanser hücreleri yağla bu kadar ilgilenir
Meme kanseri hücreleri, tüm hızlı büyüyen hücreler gibi, yeni zarlar ve haberci moleküller üretmek için sürekli bir yapı taşı kaynağına ihtiyaç duyar. Yağlar yani lipidler bu kaynağın önemli bir parçasıdır. Bu çalışma, az bilinen bir protein sisteminin kanser hücrelerini “yağ üretiminde vites büyütme” moduna nasıl soktuğunu açığa çıkarıyor; bu durum tümörlerin büyümesine ve tedaviden kaçmasına yardımcı oluyor. Bu gizli yakıt hattını anlamak, meme kanserlerini yavaşlatmak veya aç bırakmak için yeni yollar açabilir.
Büyük sonuçları olan gizli bir protein etiketi
Hücrelerimiz, proteinlerinin davranışını küçük kimyasal etiketlerle sürekli ayarlar. UFM1 adı verilen ve UFL1 adlı bir enzim tarafından eklenen bir etiket bunlardan biridir. UFM1 etiketlemesi (UFMylasyon), DNA onarımı ve stres yanıtlarıyla ilişkilendirilmişti, ancak kansere katkısı belirsizdi. Yazarlar, UFL1’in insan meme tümörlerinde normal meme dokusuna göre çok daha aktif olduğunu, başlıca tüm alt tipler boyunca bu artışın gözlendiğini gösteriyor. Tümörlerinde daha yüksek UFL1 düzeyleri taşıyan hastalar genelde daha kötü sağkalıma sahip. Araştırmacılar UFL1’i meme kanseri hücrelerinde veya fare tümörlerinde azalttıklarında, kanser büyümesi yavaşlıyor, hücre bölünmesi azalıyor ve hücre ölümü artıyordu; bu da UFL1’in kanser‑destekleyici bir faktör gibi davrandığını düşündürüyor.
Bir sinyal merkezinin yağ yapım moduna çevrilmesi
UFL1’in tümörlere nasıl yardımcı olduğunu anlamak için ekip moleküler ortaklarını aradı ve AKT1 adlı önemli bir sinyal kontrol proteinini buldu. AKT1, hücrelere büyümelerini ve yeni lipidler üretmelerini söyleyen merkezi bir anahtardır. Çalışma, UFL1’in AKT1’e fiziksel olarak bağlandığını ve onu birkaç belirli noktada UFM1 etiketleriyle süslediğini gösteriyor. Bu etiketleme AKT1’in şeklini değiştirerek normalde onu sessiz tutan içsel bir “freni” gevşetiyor. Ayrıca AKT1’in hücre içindeki bir membran bölgesi olan endoplazmik retiküluma (ER) taşınmasını kolaylaştırıyor; burada diğer enzimler AKT1’i fosfat grupları ekleyerek tam olarak aktive edebiliyor. Bu bölgelerde UFM1 etiketleri olmadığında, AKT1’in aktive edilmesi çok daha zor oluyor.
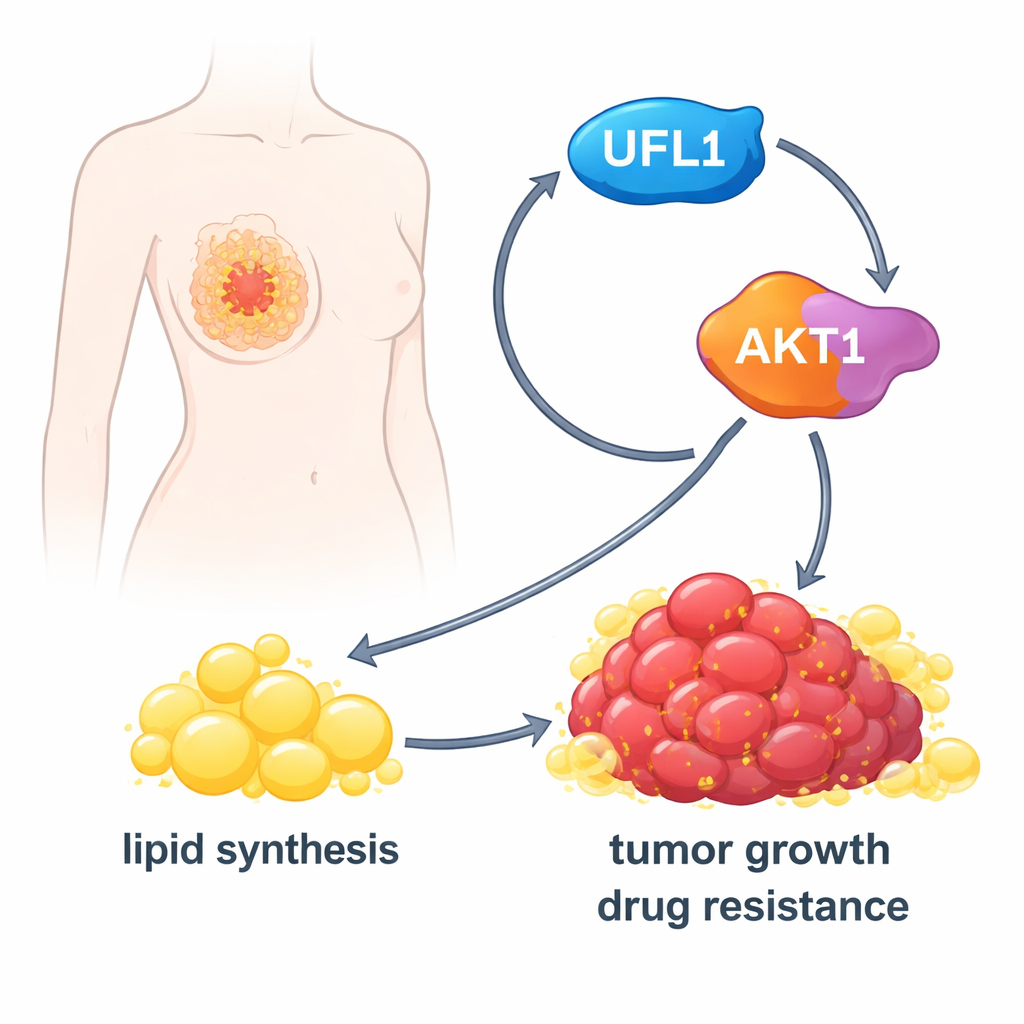
Kanserin yağ fabrikasını çalıştırmak
Aktive olduğunda AKT1 hücreleri yağ üretimini artırmaya zorluyor. Önemli bir metabolik enzim olan ACLY’nin aktivitesini yükseltiyor ve pek çok yağ‑yapım genini açan SREBP1 gibi ana düzenleyicilerin düzeylerini artırıyor. Laboratuvarda yetiştirilen meme kanseri hücrelerinde UFL1, hücrelerin daha fazla yağ damlası, serbest yağ asidi ve kolesterol biriktirmesine neden oldu. UFL1’in uzaklaştırılması bu lipid depolarını hem kültür ortamında hem de farelerde büyüyen tümörlerde belirgin şekilde azalttı. Hücre dışından ek yağ asitleri sağlanması, UFL1 eksikliğindeki kanser hücrelerinin büyümesini büyük ölçüde kurtarabiliyordu; bu da UFL1’in asıl etkinliğinin tümör genişlemesini sürdürmek için yeterli lipidi güvence altına almak olduğunu gösteriyor.
Tümör büyümesini sürükleyen kendini güçlendiren döngü
Şaşırtıcı biçimde UFL1 ile AKT1 arasındaki ilişki çift yönlü işliyor. Araştırmacılar, AKT1 aktif hale geldikten sonra kendi karşısında UFL1’e belirli bir noktada bir fosfat etiketi eklediğini keşfettiler. Bu modifikasyon UFL1’in AKT1’i UFM1 ile etiketleme yeteneğini daha da artırıyor ve pozitif bir geri besleme döngüsü oluşturuyor: UFL1 AKT1’i aktive ediyor, AKT1 ise UFL1’i aktive ediyor. AKT1 üzerindeki UFM1‑etiketi bölgelerinden ya da UFL1 üzerindeki fosfat bölgesinden herhangi biri mutasyona uğratıldığında bu döngü kırılıyor. Farelerde bu mutant versiyonları taşıyan tümörler zayıf büyüdü, daha az lipit içerdi ve daha fazla ölen hücre gösterdi. Üçlü negatif meme kanseri hastalarından alınan örneklerde, aktive olmuş UFL1 ve aktive AKT1’in yüksek düzeyleri genelde birlikte görüldü; bu da döngünün gerçek tümörlerde işlediğini vurguluyor.
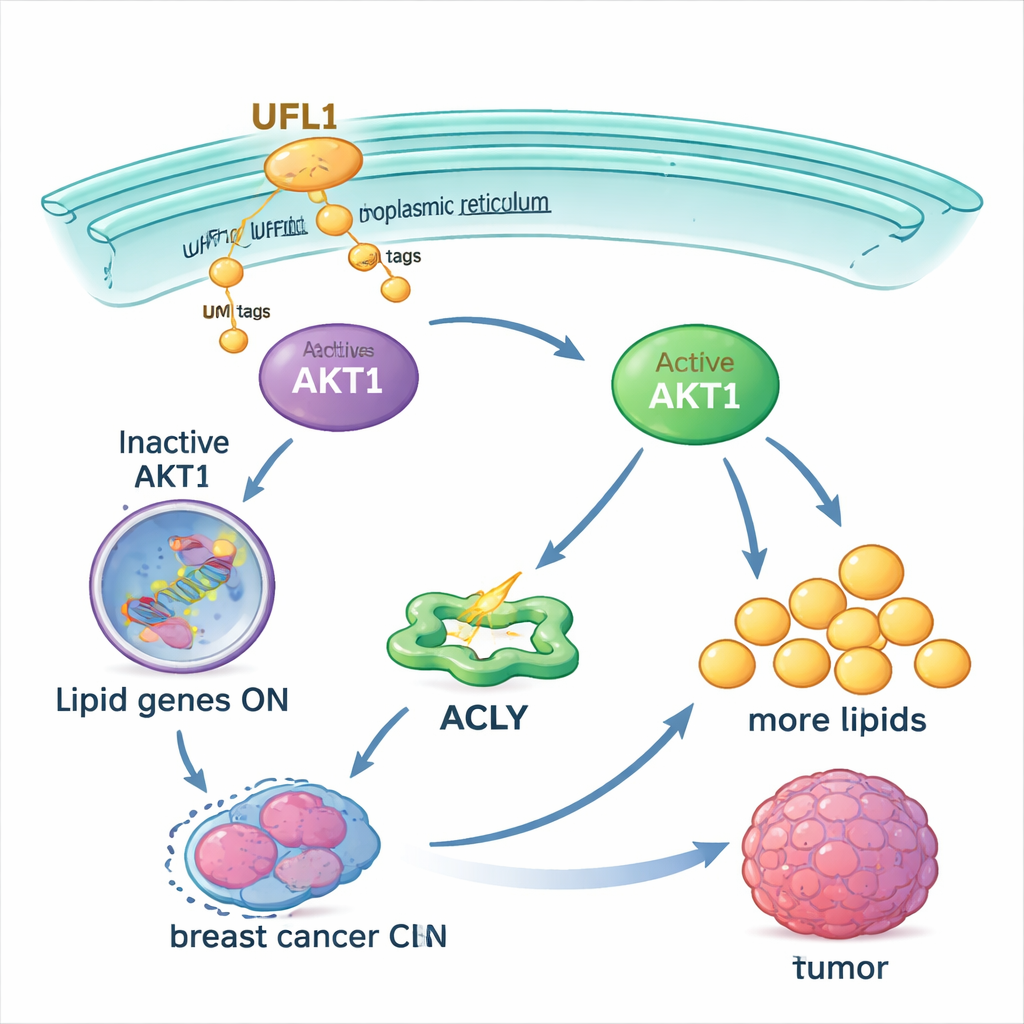
Döngüyü zayıflatarak tedavilerin etkisini artırmak
Birçok ilaç denemesi zaten AKT’i hedef aldığı için yazarlar UFMylasyonu engellemenin bu tedavileri daha etkili kılıp kılamayacağını test etti. Meme kanseri hücrelerinde küçük moleküllü bir UFMylasyon inhibitörü ve bir AKT inhibitörü her biri AKT1 aktivitesini ve lipid birikimini düşürdü, ancak birlikte kullanıldıklarında tek başlarına olduğundan çok daha iyi sonuç verdi. Kombinasyon aynı zamanda fare tümörlerinde tümör büyümesini yavaşlattı ve yağ içeriğini azalttı; hayvanlarda belirgin kilo kaybı gözlenmedi. UFMylasyonun bloke edilmesi ayrıca kanser hücrelerini cisplatin ve etoposid gibi sıkça başarısız olan standart kemoterapilere karşı daha duyarlı hale getirdi; bu ilaçlar AKT çok aktif olduğunda sıklıkla etkisiz kalıyor.
Bu hastalar için ne anlama geliyor
Basit bir ifadeyle, çalışma bazı meme kanserlerinin büyümelerini ve yağ tedariklerini besleyen kendini güçlendiren bir döngüyle kendilerini kabloladığını gösteriyor. UFL1 ve AKT1 birlikte iki pedalı aynı anda bastıran oyuncular gibi davranıyor: biri etiketliyor, diğeri sinyal veriyor ve birlikte lipid üretimini ve tümör genişlemesini yönlendiriyorlar. Bu döngüyü bozacak —UFMylasyonu, AKT1’i veya bunların etkileşimini engelleyecek— ilaçlar bulunursa, gelecekteki tedaviler tümör büyümesini yavaşlatabilir ve özellikle agresif meme kanseri tiplerinde mevcut tedavilerin etkinliğini artırabilir.
Atıf: Meng, F., Du, Y., Liang, J. et al. The UFL1-AKT positive feedback loop promotes breast cancer progression by enhancing lipid synthesis. Nat Commun 17, 614 (2026). https://doi.org/10.1038/s41467-026-68492-3
Anahtar kelimeler: meme kanseri, lipid metabolizması, AKT sinyalizasyonu, UFMylasyon, hedefe yönelik terapi