Clear Sky Science · tr
Hücresel mekân transkriptomik verilerinden gen belirteçleri ve hücre tiplerinin sağlam ve yorumlanabilir tahmini
Rutin Doku Lamlarını Moleküler Haritalara Dönüştürmek
Bir biyopsi alındığında doktorlar genellikle mikroskobun gösterdiğiyle yetinir: pembe-mor boyamalarda hücrelerin şekilleri ve düzenleri. Oysa bu renklerin altında, bir kanserin nasıl büyüdüğünü ve tedaviye nasıl yanıt verdiğini etkileyen açılıp kapanan genlerin gizli dünyası yatar. Bu çalışma, standart patoloji görüntülerinden doğrudan o moleküler metni okumayı hedefleyen STimage adlı yeni bir yapay zeka (YZ) sistemini tanıtıyor; bu sayede ek laboratuvar testleri olmadan daha hızlı ve daha ucuz bilgiler sağlanabilir.
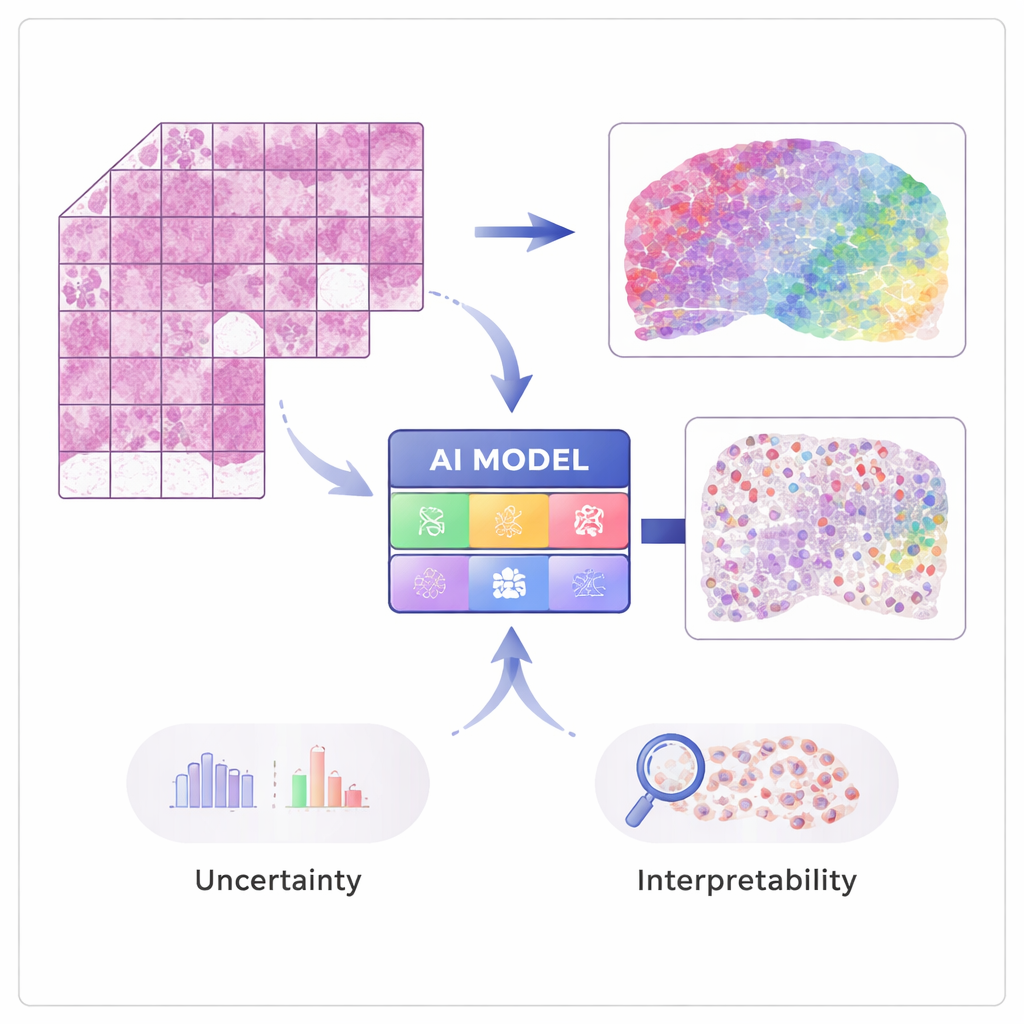
Görüntülerden Gen Aktivitesine
“Mekânsal transkriptomik”teki modern teknikler, her bir sinyalin doku içindeki kaynağını koruyarak on binlerce genin aktivitesini ölçebilir. Bu yöntemler güçlüdür ama pahalıdır ve henüz hastanelerde rutin değildir. STimage, her doku görüntüsünün birçok küçük noktadaki ayrıntılı gen ölçümleriyle eşlendiği sınırlı sayıda mekânsal veri kümesi üzerinde eğitildi. YZ, H&E (hematoksilin ve eozin) lamasındaki yerel görsel desenleri—örneğin çekirdeklerin yoğunluğu veya düzensizliği gibi—altyapıdaki gen aktivitesiyle ilişkilendirmeyi öğrenir; böylece daha sonra yalnızca sıradan görüntülerden gen ekspresyonunu ve hücre tiplerini tahmin edebilir.
Daha Güvenilir Bir YZ Patoloğu İnşa Etmek
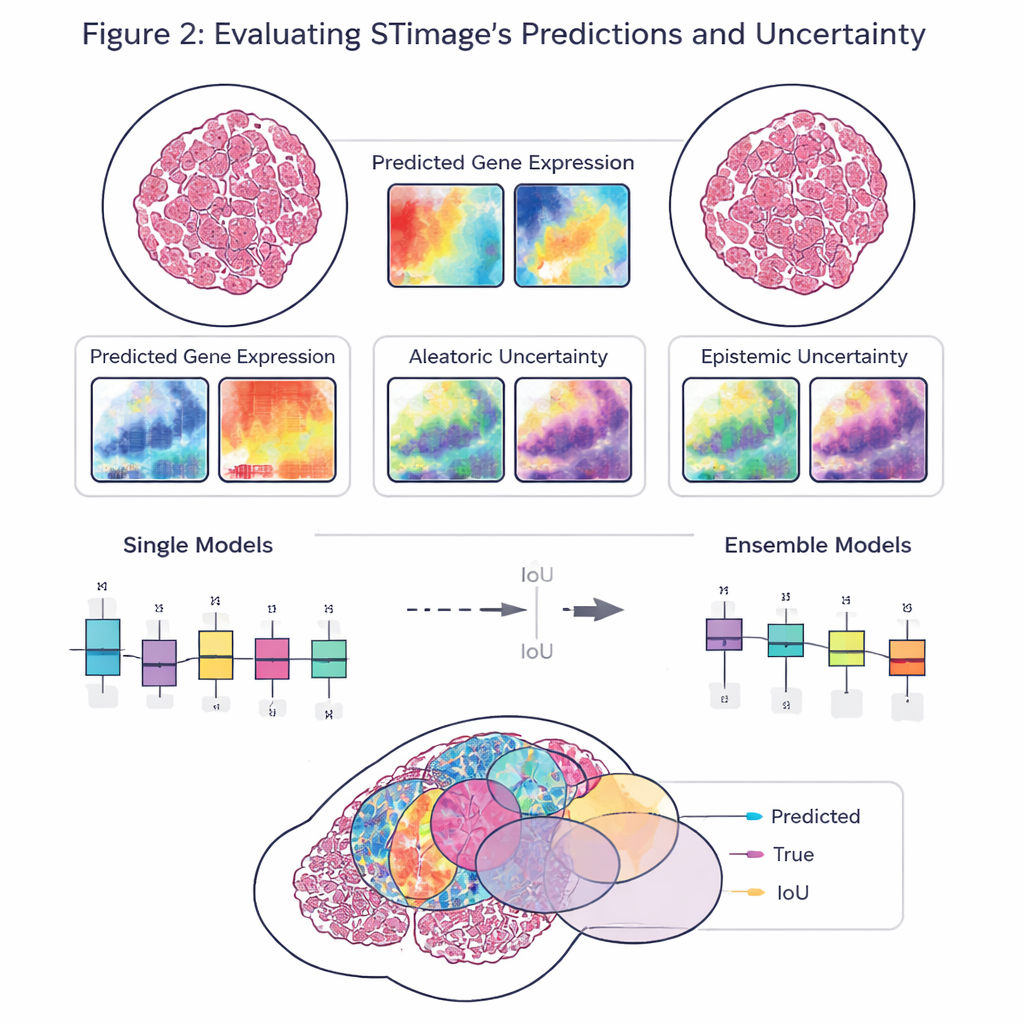
Çalışmanın temel hedefi yalnızca doğruluk değil, güvenilirlik ve açıklanabilirliktir. STimage her gen için tek bir sayı vermek yerine, her konumdaki olası gen aktivitesi aralığını tanımlayan tam bir olasılık dağılımı öngörür. Ayrıca iki tür belirsizliği ayırır: biri gürültülü veya değişken veriden kaynaklanan, diğeri ise modelin kendi bilgi eksikliğini yansıtan belirsizlik. Birbirinden hafifçe farklı birçok model eğitip bunların ortalamasını almak—yani bir “ensemble” yaklaşımı—araştırmacıların hem performansı artırmasını hem de sistemin nerede kendinden emin olup olmadığını daha net görmesini sağlar; bu, klinik karar verme için kritik öneme sahiptir.
Kanserler, Teknolojiler ve Hastaneler Arasında Test Etme
Ekip, STimage’i meme, deri ve böbrek kanserleri ile bağışıklık ilişkili bir karaciğer hastalığından elde edilen çeşitli veri kümeleri üzerinde değerlendirdi. Model, önemli kanser ve immün belirteçleri tahmin etmeyi öğrendi ve genellikle bağımsız deneylerde görülen gerçek mekânsal desenlerle eşleşti. Farklı laboratuvarlardan, örnek hazırlama yöntemlerinden ve hatta tek hücre çözünürlüğüne sahip platformlar ile daha eski, daha düşük çözünürlüklü sistemler gibi farklı temel teknolojilerden gelen verilerle sınandığında model performansını korudu. Birkaç mevcut YZ aracıyla yapılan doğrudan karşılaştırmalarda STimage ve ensemble varyantları genellikle üst sıralarda yer aldı; özellikle tahmin edilen desenlerin doku genelindeki gerçek gen aktivitesi dağılımıyla ne kadar iyi uyuştuğu değerlendirildiğinde.
Tümörlerin İçini Görmek: Hücreler, Sağkalım ve İlaç Yanıtı
STimage, gen tahmininin ötesine geçerek her bölgeyi hangi hücre tiplerinin kapladığını yüksek çözünürlüklü, her hücrenin kimliğinin bilindiği veri kümelerini kullanarak çıkarsadı. Model, kanser hücrelerini immün ve destekleyici hücrelerden ayırabildi ve bunların lam üzerindeki düzenini haritalandırdı. Yazarlar daha sonra STimage’i The Cancer Genome Atlas’tan gelen büyük rutin kanser görüntüsü koleksiyonlarına uyguladı. Mekânsal ölçümler olmadan bile YZ’nin tahmin ettiği gen profilleri gerçek toplu (bulk) gen verileriyle yakından örtüştü. Bu tahminler hastaları daha yüksek ve daha düşük riskli gruplara ayıracak kadar güçlüydü ve belirli meme kanseri tedavilerine tamamen yanıt verme olasılığı daha yüksek olanları ayırt etmede yardımcı oldu.
Gelecekteki Hastalar İçin Bunun Önemi
Hastalar ve klinisyenler için STimage’in vaadi, tanıdık patoloji lamı üzerinde bir tür “moleküler katman” sunmaktır. Birden fazla pahalı test sipariş etmek yerine tek bir taranmış görüntü bir gün nerede agresif gen programlarının aktif olduğunu, immün hücrelerin nasıl dağıldığını ve hangi belirteçlerin daha iyi veya daha kötü sonuçlara ya da farklı ilaç yanılarına işaret ettiğini ortaya çıkarabilir. Yöntem hâlâ geliştiriliyor ve gerçek ölçümlerle korelasyon mükemmel olmasa da, mekânsal desenleri yakalama, kendi belirsizliğini tahmin etme ve tahminlerini hangi hücrelerin etkilediğini vurgulama yeteneği, daha bilgilendirici ve şeffaf dijital patolojiye doğru pratik bir adım sunar.
Atıf: Tan, X., Mulay, O., Xie, J. et al. Robust and interpretable prediction of gene markers and cell types from spatial transcriptomics data. Nat Commun 17, 1781 (2026). https://doi.org/10.1038/s41467-026-68487-0
Anahtar kelimeler: dijital patoloji, mekânsal transkriptomik, kanser belirteçleri, derin öğrenme, tümör mikroçevresi