Clear Sky Science · tr
İnsan GABA taşıyıcısı GAT3’ün seçici inhibisyonunun yapısal temeli
Sinir sinyallerini yatıştırmanın önemi
Beynimiz, uyarıcı sinyaller ile yatıştırıcı sinyaller arasındaki hassas bir dengeye dayanır. Önemli bir yatıştırıcı haberci olan GABA, epilepsi, inme hasarı ve Alzheimer hastalığı gibi durumlarla ilişkili kontrolsüz aktiviteyi önlemeye yardımcı olur. Bu çalışma, sinir hücrelerinin çevresinden GABA’yı temizleyen GAT3 adlı bir proteine odaklanıyor. Araştırmacılar, yeni bir molekülün GAT3’e nasıl bağlanıp onu kapattığını atomik ayrıntıda ortaya koyarak, beynin doğal fren sistemini nazikçe güçlendirebilecek yeni nesil ilaçların tasarımı için yapısal bir yol haritası sunuyor.
Beynin kendi fren pedalı
GABA, merkezi sinir sisteminde başlıca inhibitör yani yatıştırıcı nörotransmitterdir. GABA sinir uçlarından salındıktan sonra, beyin devrelerinin yeniden ayarlanabilmesi için hızla uzaklaştırılması gerekir. Bu temizliği, GABA’yı hücre içine pompalayan taşıyıcı proteinler gerçekleştirir. Beyinde iki taşıyıcı öne çıkar: ağırlıklı olarak nöronlarda bulunan GAT1 ve astroasit adı verilen destek hücrelerinde bulunan GAT3. GAT1’i engelleyen bir ilaç (tiagabin) onlarca yıldır epilepsi tedavisinde kullanılsa da, GAT3’e özgü karşılaştırılabilir ilaçlar geride kalmıştır. Buna karşın GAT3, sinapsların dışındaki GABA düzeylerini kontrol etmesi ve beyni ince ayarla şekillendiren uzun süreli, arka plan inhibisyonunu belirlemesi nedeniyle özellikle ilgi çekicidir. 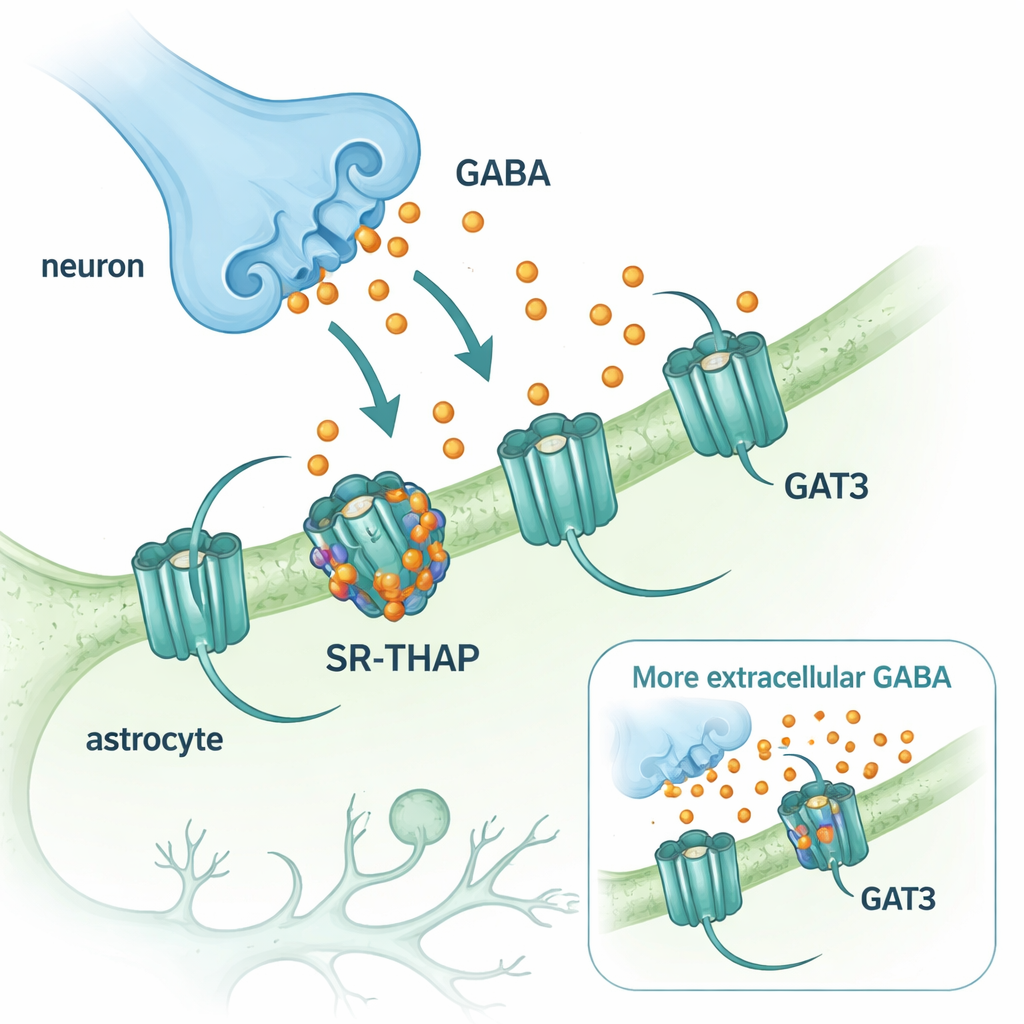
Daha hassas bir moleküler kilit tasarlamak
GAT3’ü engelleme çabaları, ayrıntılı yapısal bilgi eksikliğinden dolayı zorluklarla karşılaştı. Geçmişteki birçok bileşik, çoğunlukla bilinen GABA benzeri moleküllerin hacimli varyantları yapılarak deneme‑yanılma ile geliştirildi. En bilinenlerden biri olan (S)‑SNAP‑5114 kimyasal olarak kararsız çıktı ve canlı hayvanlarda kullanımı zordu. Bu bileşiğin daha dayanıklı bir yakını üzerine inşa ederek, yazarlar GAT3’e daha sıkı uyacak ve parçalanmaya daha dirençli olacak yeni küçük molekül SR‑THAP’ı geliştirdiler. İnsan hücre kültürlerindeki deneyler, SR‑THAP’ın GAT3’ü güçlü biçimde engellediğini ve bunun rekabetçi olmayan bir şekilde gerçekleştiğini gösterdi: yani SR‑THAP, GABA ile alışılmış bağlanma noktasında doğrudan yarışmak yerine taşıyıcının işleyişini değiştiriyor ve maksimum taşıma kapasitesini azaltıyor.
GAT3’ü yakın‑atomik çözünürlükte görmek
SR‑THAP’ın tam olarak nasıl çalıştığını anlamak için ekip, elektronlarla dondurulmuş proteinlerin üç boyutlu şeklini yeniden inşa eden cryo‑elektron mikroskobu yöntemine başvurdu. İnsan GAT3’ün üç versiyonunu çözdüler: SR‑THAP bağlı, GABA bağlı ve substrat içermeyen durumda. Üçü de ilgili nörotransmitter taşıyıcılarında görülen tipik mimariyi ortaya koyuyor: zar boyunca sıkıca paketlenmiş 12 heliks ve GABA ile eşlikçi iyonlar olan sodyum ve klorür için merkezi bir yol oluşturan yapılar. GABA bağlı yapıda taşıyıcı “içe‑kilitli” (inward‑occluded) durumda—GABA ve bir sodyum iyonu ortada sıkıştırılmış halde, hem dışarıdan hem de içeriden izole edilmiş. Anahtar bir aromatik amino asit, GABA’nın amino grubuyla özel bir etkileşim kuruyor; bu, GAT3’ün substratını nasıl tanıdığını açıklamaya yardımcı oluyor.
SR‑THAP taşıyıcıyı nasıl açık konuma takıyor
Çarpıcı bir karşıtlık olarak, SR‑THAP bağlı yapı GAT3’ü “içe‑açık” (inward‑open) halde yakalıyor; proteinin iç yüzü hücre içi tarafa doğru genişlemiş görünüyor. SR‑THAP, bu iç boşluğun derinliklerine yerleşmiş ve taşıma döngüsü sırasında normalde hareket eden birkaç heliksin arasına takılmış durumda. Farklı kimyasal karakterlere sahip üç küçük cebi işgal ediyor ve hidrojen bağları ile hidrofobik temaslardan oluşan bir ağla etkileşime giriyor. Bu konumlanma, taşıyıcıyı etkili biçimde kilitliyor ve böylece GABA ile iyonların yolculuklarını tamamlamasını engelliyor. Yazarlar, bu boşluğu hizalayan birkaç spesifik amino asidin GAT3 ile yakın akrabaları arasında farklılık gösterdiğini; bu kalıntılardan birinin yer değiştirilmesinin hem taşıma aktivitesini hem de SR‑THAP etkinliğini değiştirdiğini gösteriyor; bu da inhibitörün GAT3 üzerinde GAT1 veya ilgili taşıyıcılara göre neden çok daha seçici olduğunu açıklamaya yardımcı oluyor. 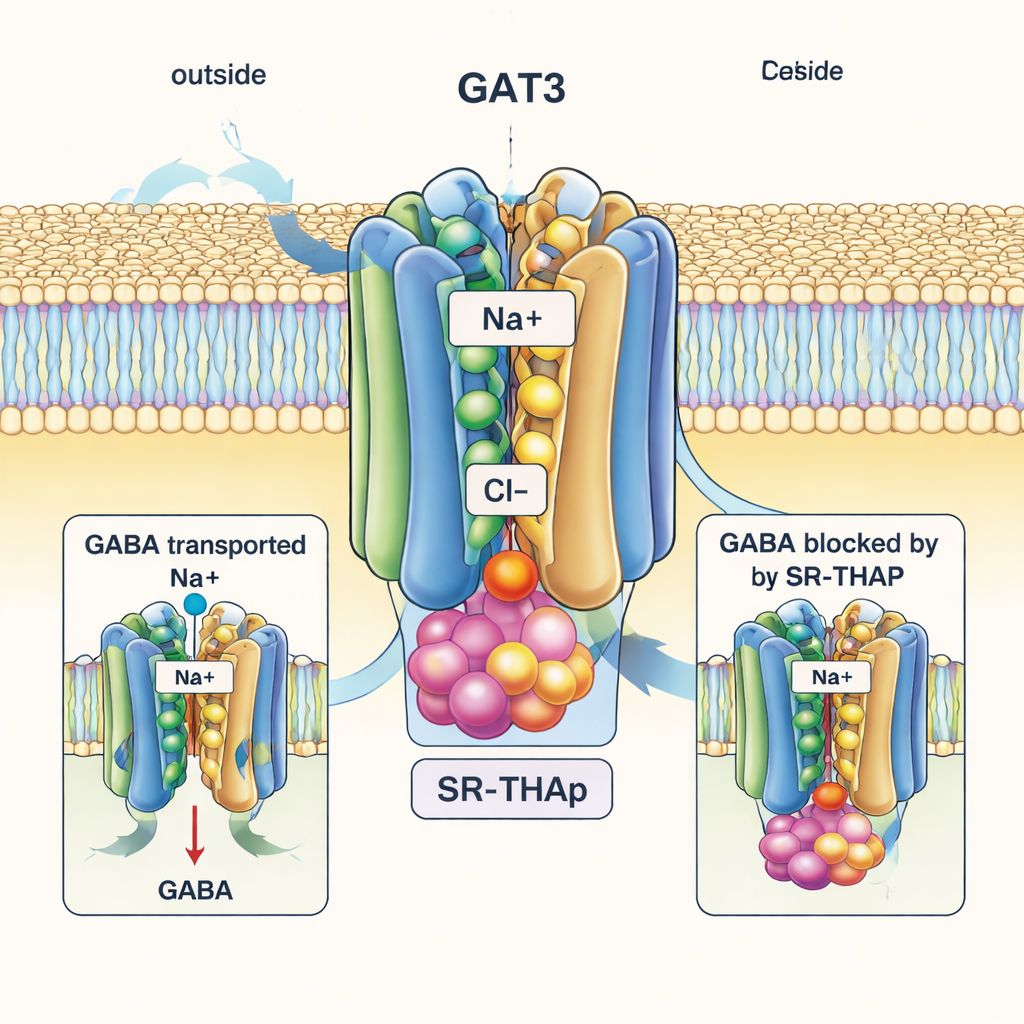
Yeni epilepsi ve beyin sağlığı ilaçlarına kapı açmak
Bu yapılar bir araya geldiğinde, GAT3’ün GABA’yı taşımak için farklı şekiller arasında nasıl döndüğünü ve SR‑THAP’ın daha az korunmuş iç bir cebin nasıl avantajını kullanarak bu döngüyü nasıl dondurduğunu ortaya koyuyor. Uzman olmayanlar için temel çıkarım, çalışmanın GAT3’ü yüksek derecede seçici bir şekilde kapatmak için detaylı bir moleküler plan sunduğudur. Bu tür bileşikler, mevcut ilaçlardan daha ince ayarlı bir şekilde yatıştırıcı GABA düzeylerini yükseltebilir ve potansiyel olarak epilepsi, inme iyileşmesi, Alzheimer hastalığı ve inhibe edici sinyal iletiminin bozulduğu diğer durumlar için yeni tedavilere veya araştırma araçlarına yol açabilir.
Atıf: Mortensen, J.S., Bavo, F., Jensen, M.H. et al. Structural basis for selective inhibition of human GABA transporter GAT3. Nat Commun 17, 1774 (2026). https://doi.org/10.1038/s41467-026-68479-0
Anahtar kelimeler: GABA taşıyıcısı, GAT3, epilepsi, cryo-EM, nörotransmitter inhibitasyonu