Clear Sky Science · tr
Rastlantısal bir mekanizma, AAA+ makine ClpB’de hızlı substrat aktarımını yönlendirir
Hücresel Makineler Proteinleri Nasıl Hareket Ettirir
Her hücrenin içinde, küçük moleküler makineler proteinlerin topaklaşmasını önlemek ve hasarı onarmak için sürekli çekip çeker ve yeniden şekillendirir. ClpB adlı bu makinelere biri, düğümlenmiş proteinleri kurtarmaya yardım eder—stres altında hücre yaşamı için hayati bir görev. Bu çalışma basit ama derin bir soruyu soruyor: ClpB, kimyasal yakıt ATP’yi merkezsel gözenekten bir protein zincirini çekme mekanik işine nasıl dönüştürüyor ve bunu düzgün, senkron adımlarla mı yoksa daha rastgele, difüzif bir şekilde mi yapıyor?
Çalışan Bir Protein Kurtarma Halkası
ClpB, halka şeklinde yapılar oluşturan ve merkezinde bir tünel barındıran büyük bir enzim ailesi olan AAA+ makinelerine aittir. Birçoğu kriyo-elektron mikroskobu ile ayrıntılı biçimde görüntülenmiş ve popüler bir "el-den-ele" modeli ortaya çıkmıştır: yakılan her ATP molekülü, sırayla bir ipi çeken bir ekip gibi küçük, kesin bir adımı tetikler. Buna karşın diğer deneyler ClpB’nin proteinleri, ATP tüketim hızının yavaşlığına göre çok daha hızlı taşıyabileceğine işaret etmişti. Bu bilmeceyi çözmek için yazarlar, tek tek ClpB moleküllerini esnek bir test proteini olan κ-casein’i gözeneklerinden geçirirken gerçek zamanlı izlediler.
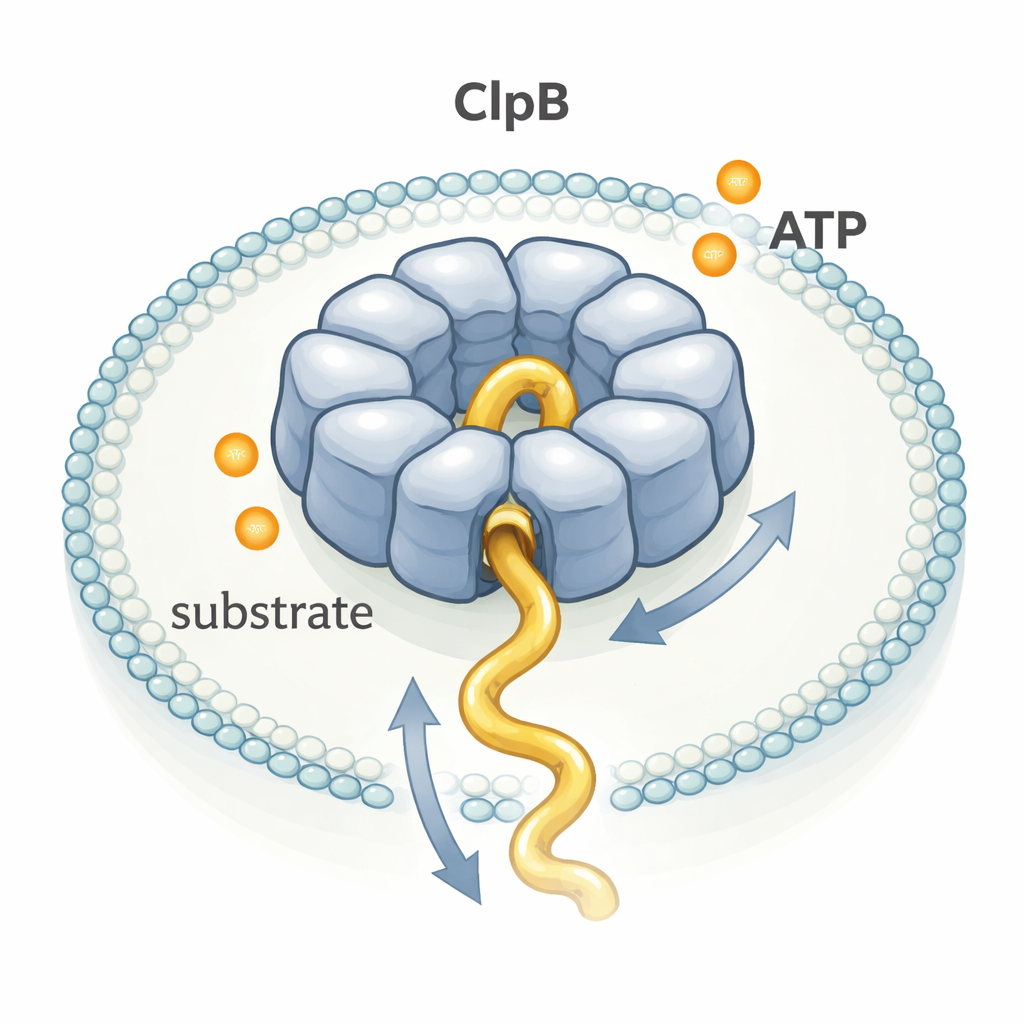
Bir Molekülü Bir Kerede İzlemek
Araştırmacılar bireysel ClpB halkalarını ve tek κ-casein moleküllerini cam yüzeye yapışmış küçük lipid kabarcıkların içine tuzakladılar. ClpB’nin ve protein zincirinin belirli noktalarına floresan boyalar bağladılar ve ardından nanometre ölçeğinde boya çiftleri arasındaki uzaklık değişimlerini rapor eden tek-molekül FRET tekniğini kullandılar. κ-casein gözenek içine kaydığında boyalar birbirine yaklaşır ve FRET kısa bir sıçrama ile yükselirdi; zincir çıktığında sinyal tekrar düşerdi. Binlerce böyle sıçramanın süresini ve yüksekliğini ölçerek, protein segmentlerinin gözenekten ne kadar hızlı ve ne kadar uzağa geçtiğini çıkarabildiler.
Hızlı, Zayıf Yakıtlanan ve Neredeyse Sıcaklıktan Bağımsız
Şaşırtıcı biçimde, translokasyon olayları son derece hızlı oldu: etiketli κ-casein segmenti tipik olarak gözenekten birkaç nanometreyi yaklaşık 1–2 milisaniyede kat etti—bu, ClpB’deki ATP hidrolizmi olayları arasındaki ortalama zamandan yaklaşık bin kat daha hızlıdır. Olayların çoğu bu kadar kısaydı ve tek bir karakteristik zaman ölçeğinden ziyade geniş, kuvvet-yasası (power-law) dağılımı izlediler. Sıcaklığı 10’dan 32 °C’ye değiştirmek bu hareketleri neredeyse yavaşlatmadı; bu da hareket için gereken enerji bariyerinin, kinesin gibi klasik "güç darbesi" motorlarına göre çok küçük olduğunu gösterir. Benzer şekilde, ATP konsantrasyonunun düşürülmesi olayların ne sıklıkta gerçekleştiğini güçlü şekilde azalttı, ancak her bir olayın süresini neredeyse etkilemedi. Başka bir deyişle ATP, ClpB’nin ne zaman devreye girdiğini ve ne sıklıkta hareket ettiğini bireysel geçiş patlamalarının hızından daha çok kontrol ediyordu.
İleri-Geri Hareket, İleri Yönlü Bir Eğimle
Zincirlerin her zaman tek yönde ilerleyip ilerlemediğini görmek için ekip daha karmaşık üç renkli FRET deneyleri yaptı; hem gözenek uçlarını hem de substratı boyadılar. Bu, κ-casein’in halkaya üstten mi yoksa alttan mı girdiğini ve tamamen geçip geçmediğini ya da geri çekilip çekilmediğini ayırt etmelerini sağladı. Altı ayrı desen keşfettiler: tam ileri ve geri geçişler, zincirin gitmeden önce gözenek uçlarını örneklediği daha uzun "kısmi" ziyaretler ve sadece bir uç yakınındaki kısa karşılaşmalar. Tam olayların yaklaşık dörtte üçü ileri yöndeydi, fakat önemli bir kısmı geriye gidiyordu; bu, ClpB’nin substratının iki yönlü difüzyonuna izin verdiğini ve yalnızca ılımlı bir ileri eğilim gösterdiğini ortaya koydu. ATP yavaşça hidrolize olan bir analogla değiştirildiğinde, olaylar nadir ve çok daha yavaş hale geldi ve ileri tercih neredeyse kayboldu.
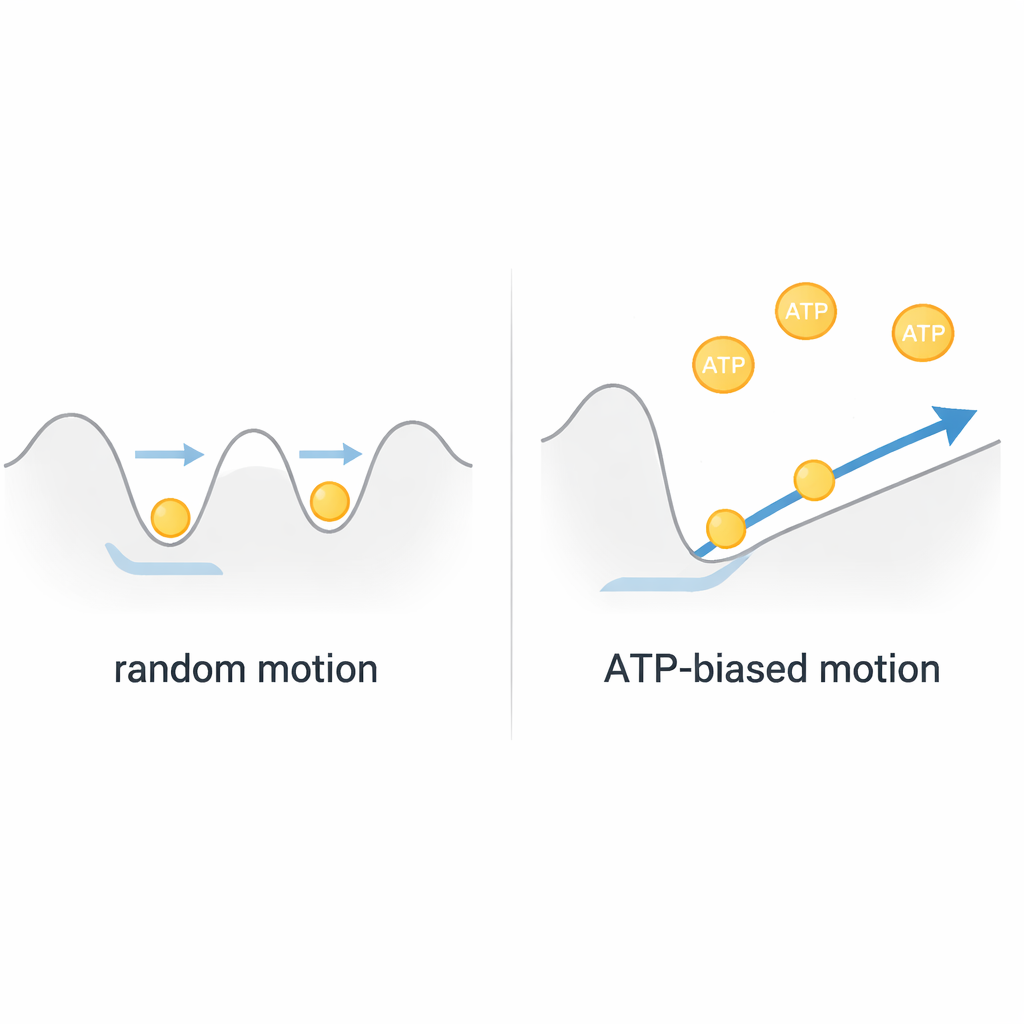
Basit Bir Vinç Değil, Bir Brown Hareket Motoru
Bu gözlemleri birleştirerek yazarlar, ClpB’nin katı, yakıtla çalışan bir vinçten ziyade bir Brown hareket motoruna daha çok benzediği sonucuna varıyorlar. Protein zinciri gözenek içinde sığ bir enerji manzarası içinde termal olarak titrer ve yüksek hızda ileri geri hareket eder. ATP doğrudan büyük, ayrık çekme darbelerine güç vermez; bunun yerine içsel "gözenek döngülerinin" hızlı hareketleri yoluyla bu manzarayı ayarlar ve hareketi hafifçe bir yönde lehine çevirir. Her tam geçiş olayı yalnızca bir veya iki ATP molekülü tüketimiyle ilişkili olduğundan, ClpB rastgele hareketi düzeltip yönlendirerek olağanüstü verimli, hızlı taşıma sağlıyor. Bu görüş, birçok AAA+ makinesi hakkındaki düşüncemizi yeniden şekillendiriyor ve biyolojik nanomotorların sıklıkla rastlantısallıktan kaçınmak yerine ondan yararlanabileceğini öne sürüyor.
Atıf: Casier, R., Levy, D., Riven, I. et al. A stochastic mechanism drives fast substrate translocation in the AAA+ machine ClpB. Nat Commun 17, 1773 (2026). https://doi.org/10.1038/s41467-026-68478-1
Anahtar kelimeler: protein translokasyonu, AAA+ makine, Brown hareket motoru, moleküler şaperon, tek-molekül FRET