Clear Sky Science · tr
İnsan küçük iletkenlikli Ca2+ ile aktive potasyum kanalı SK2'nin inhibisyon ve aktivasyonu için yapısal mekanizmalar
Neden küçük potasyum kanalları önemli
Her düşünceniz ve hissettiğiniz her kalp atışı, hücrelerinizdeki elektriksel sinyallere bağlıdır. Bu sinyaller, yüklü atomların içeri girip çıkmasına izin veren iyon kanalı denilen mikroskobik gözenekler tarafından biçimlendirilir. Küçük iletkenlikli kalsiyumla aktive potasyum kanalları (SK kanalları) adı verilen aile, sinir hücrelerinin ateşleme biçimini ve kalbin ritmini kontrol etmeye yardımcı olur. Bu makale, ailenin önemli üyelerinden insan SK2 kanalının farklı ilaçlar ve bir arı toksini tarafından atomik ayrıntıda nasıl ya kapatıldığını ya da güçlendirildiğini ortaya koyuyor—atriyal fibrilasyondan tremor ve hafıza sorunlarına kadar uzanan bozukluklar için yeni tedavilere yol gösterebilecek içgörüler.
SK2 kanalları hücresel fren görevi görür
SK2 kanalları hücre zarında yer alır ve elektriksel aktivite üzerinde küçük frenler gibi davranır. Bir elektriksel sinyal sırasında hücrenin içi kısa süreli olarak kalsiyum iyonlarıyla dolduğunda, bu artışı algılayan yardımcı bir protein olan kalmodulin devreye girer. Kalmodulin SK2'nin iç tarafına bağlıdır ve kalsiyumu bağladığında, kanalın bir bölümünü bir çekiç ipi gibi çekerek potasyum iyonlarının dışarı akmasına izin veren bir kapıyı açar. Bu dışa akış, hücre ateşlendikten sonra sessizleşmesine yardımcı olur; nöronların ne sıklıkta sinyal gönderebileceğini ve kalp hücrelerinin ne kadar güvenilir atacağını şekillendirir. SK1–3 kanalları beyin ve kalpte yaygın olduğundan ve SK2 özellikle önemli bir alt tip olduğundan, bu kanalların tam olarak nasıl açılıp kapandığını ve ilaçlara nasıl yanıt verdiklerini anlamak hassas ilaç tasarımı için hayati önemdedir.
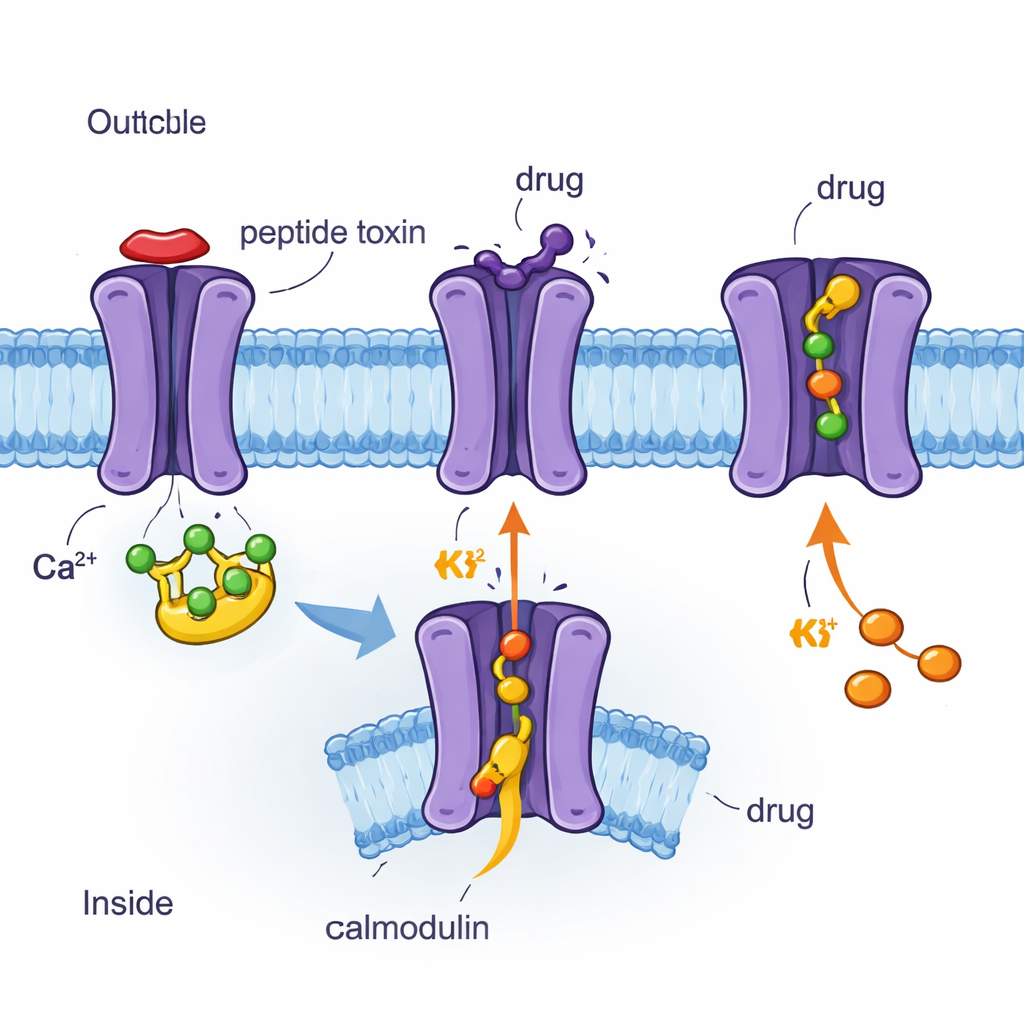
Kanal ve ilaçları atom atom görmek için cryo‑EM kullanımı
Yazarlar, neredeyse atomik çözünürlükte dondurulmuş proteinleri görüntüleyen bir teknik olan cryo‑elektron mikroskobu (cryo‑EM) kullanarak, kalmodulin ve farklı moleküllerle bağlı insan SK2 kanalının dört üç boyutlu yapısını belirlediler. Bunlar arasında arı zehri peptidi apamin, sentetik bloke edici UCL1684, klinik inhibitör AP30663 ve klinik aktivatör CAD‑1883 bulunuyordu. Dört yapının tamamı SK2'yi zarı geçen dört parçalı bir montaj olarak ve kalmodulinin iç tarafta bağlanmış halde olduğunu gösteriyor. Bu görüntülerin karşılaştırılması, kanalın hangi bölgelerinin sert, hangilerinin esnek olduğunu ve kanal kapalı veya açık durumda iken kalmodulinin nasıl hareket ettiğini ortaya koydu. Araştırmacılar ayrıca bu görüntüleri hücrelerdeki elektriksel ölçümlerle birleştirerek, belirli amino asit değişikliklerinin her bileşiğe kanalın yanıtını nasıl etkilediğini test ettiler.
Dış ağzı tıkayan bir arı toksini ve bir laboratuvar ilacı
Arı zehrinden gelen küçük bir peptid olan apamin, uzun zamandır araştırmalarda kullanılan son derece güçlü ve seçici bir SK2 engelleyicisi olarak biliniyor. Yeni yapılar apaminin SK2 gözenek dış ağzına bir tıpa gibi bağlandığını gösteriyor. Apamin, SK2'de iyi düzenlenmiş fakat ilgili bir kanal olan SK4'te gevşek olan iki heliks arasındaki kısa bir döngü (S3–S4 bağlayıcısı) tarafından oluşturulan kupa şeklindeki bir vestibüle yuvalanıyor; bu da SK4'ün apamine karşı duyarsız olmasını açıklıyor. Apaminin anahtar pozitif yük taşıyan kalıntıları kanalın dört aromatik yan zinciri arasına ulaşıp güçlü elektrostatik ve istifleme etkileşimleri kurarak potasyum yolunu tamamen mühürlüyor. Sentetik bis‑kinolinyum bileşiği UCL1684 esasen aynı dış cebi dolduruyor ve iyon çıkışını da engelliyor, ancak daha küçük boyutu apaminin kritik pozitif yüklerinin pozisyonunu taklit edecek şekilde daha derine yerleşmesine izin veriyor. Bu vestibülü şekillendiren kanal kalıntılarının değiştirilmesi, apamina ve daha az ölçüde UCL1684'e duyarlılığı keskin şekilde azaltıyor; bu da şekillendirilmiş dış döngünün toksin ve ilacın etkisinde ana belirleyici olduğunu doğruluyor.
Aktiviteyi ayarlayan merkezi tıpa ve iç kama
Bunun aksine, klinik aday AP30663 SK2'nin seçicilik filtresinin hemen altında, kanalın merkez boşluğunun içinde bağlanıyor. Orada belirli yan zincirlerin arasında sıkışarak fiziksel bir tıpa görevi görüyor. Bu astlayıcı residülerde yapılan değişiklikler AP30663'ün SK2'yi engelleme yeteneğini zayıflatıyor ve dizi karşılaştırmaları neden yakın analoglarının SK1–3 ile SK4'ü ayırt edebildiğini açıklıyor. Hareket bozuklukları için geliştirilen pozitif modülatör CAD‑1883 ise bambaşka bir strateji kullanıyor. CAD‑1883, kalmodulinin N‑lobu ile kalmodulinin hareketini kanal kapağına bağlayan kısa bir bağlayıcı (S4–S5) arasındaki arayüzdeki bir cebe kayıyor. Bu cebdeki teması güçlendirerek CAD‑1883, kalmodulini ve SK2'yi iç kapıyı açan ve gözenegi genişleten bir konfigürasyonda etkili bir şekilde birbirine yapıştırıyor. Yapısal karşılaştırmalar CAD‑1883 bağlanmış durumun tam açık bir kanala benzediğini gösteriyor; ancak selektivite filtresinin uzamış açılma sonrası inaktive bir form alabileceği belirtiliyor.
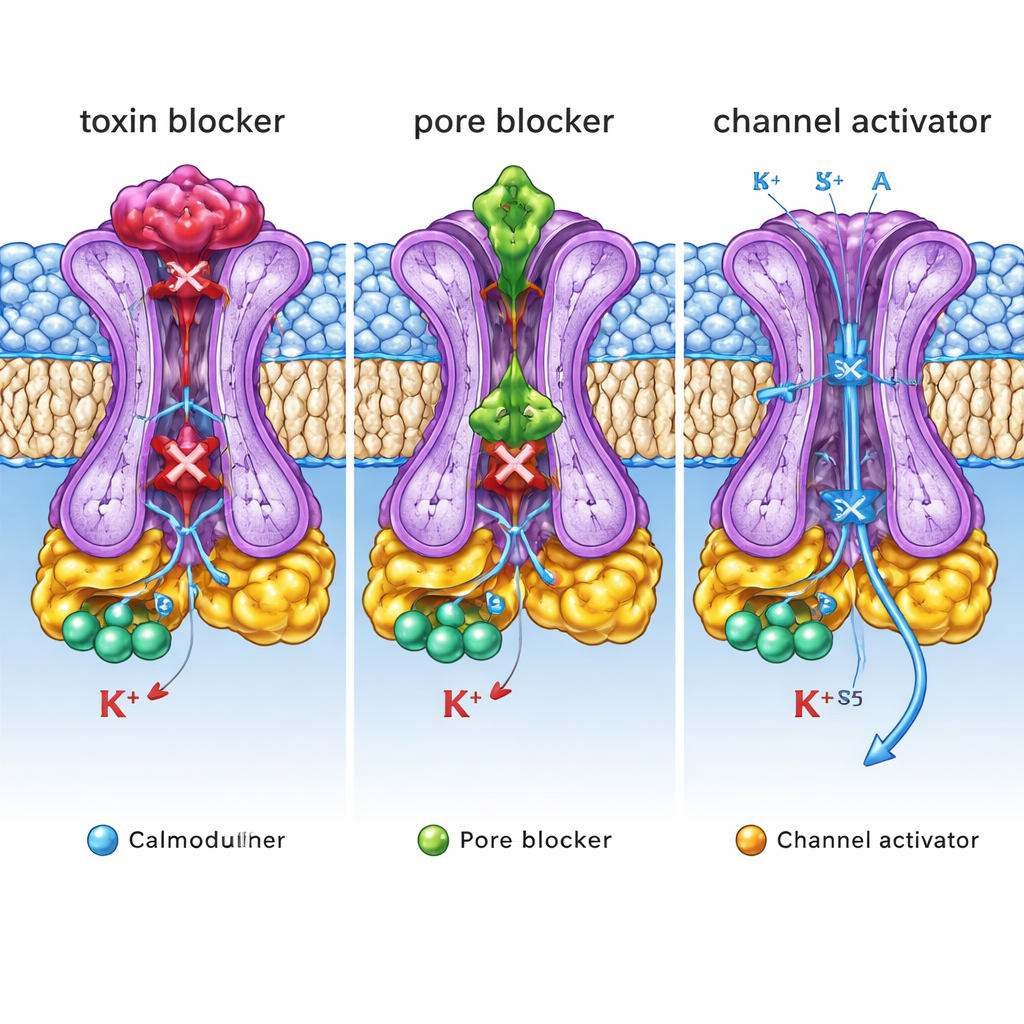
Bu yapısal taslakların tıp için anlamı
Bir araya getirildiğinde, bu yapılar tek bir SK2 kanalında üç ayrı “kontrol düğmesi” olduğunu ortaya koyuyor: toksinlerin ve bazı bloke edicilerin oturduğu dış kapak, diğer inhibitörlerin akışı tıkadığı iç pore boşluğu ve aktivatorlerin açılmayı stabilize ettiği yan cep. Uzman olmayanlar için ana mesaj, aynı iyon kanalının çok farklı yapısal kavrama noktalarını tutan ilaçlarla yukarı veya aşağı ayarlanabileceğidir. Bu kavrama noktalarını atomik hassasiyetle haritalandırıp bunları fonksiyonel etkilerle ilişkilendirerek, bu çalışma SK2 aktivitesini seçici olarak azaltacak veya artıracak yeni nesil moleküller tasarlamak için ayrıntılı bir taslak sağlıyor. Bu tip özel ilaçlar bir gün anormal beyin ritimlerini normalize etmeye, tremorları hafifletmeye veya düzensiz kalp atışlarını daha az yan etkiyle düzeltmeye yardımcı olabilir.
Atıf: Ma, B., Wu, D., Cao, E. et al. Structural mechanisms for inhibition and activation of human small-conductance Ca2+-activated potassium channel SK2. Nat Commun 17, 1770 (2026). https://doi.org/10.1038/s41467-026-68475-4
Anahtar kelimeler: SK2 potasyum kanalları, kalsiyumla aktive kanallar, cryo-EM yapıları, iyon kanal modülatörleri, atriyal fibrilasyon ve tremor