Clear Sky Science · tr
Koil‑kıvrım heterodimer aracılı bölünmüş baz düzenleme sistemleri esnek ve sağlam nükleotid değişimlerine olanak tanır
Daha Az Yan Etkiyle DNA’yı Düzeltmek
Birçok hastalık DNA’mızdaki küçük yazım hatalarından—tek harfli yanlışlıklardan—kaynaklanır ve bunlar hayati sonuçlara yol açabilir. Bilim insanlarının, DNA’yı kesmeden bu hataları düzeltebilen güçlü araçları var; bunlara baz düzenleyiciler denir. Ancak bu araçlar hacimce büyük olup vücuda güvenli şekilde ulaştırmak zordur. Bu çalışma, baz düzenleyicileri daha küçük, akıllı parçalara bölmenin yeni bir yolunu tanıtıyor; bu parçalar orijinalleri kadar iyi — hatta bazen daha iyi — çalışıyor ve karaciğer, kaslar ve ötesindeki genetik hastalıkları tedavi etme yollarını açıyor.
Neden Boyut Gen Düzeltme Araçları İçin Sorun Oluşturuyor
Baz düzenleyiciler, CRISPR sisteminin parçalarını bir harfi başka bir harfe çevirebilen enzimlerle birleştirir; örneğin A’yı G’ye veya C’yi T’ye dönüştürmek gibi. Bu kesin değişimler, yüksek kolesterol veya musküler distrofi gibi durumların tedavisi için ümit vericidir. Ancak gen terapisi için önde gelen taşıyıcı araçlardan biri olan adeno‑ilişkili virüs (AAV) yalnızca yaklaşık 4,7 bin DNA harfi taşıyabilir; oysa standart baz düzenleyiciler bundan daha büyüktür. Daha önceki çalışmalar, bu düzenleyicileri intein gibi özel protein “makasları” ile bölmeyi ya da enzimleri küçülterek çözmeyi denedi; fakat bu yaklaşımlar sıklıkla verimi düşürdü, tasarım karmaşıklığı getirdi veya araçların genomda nerede etkili olabileceğini sınırladı.
Düzenleyiciyi Yeniden Birleştirmek İçin Moleküler Cırt Cırt Kullanmak
Bunu çözmek için araştırmacılar, koil‑kıvrım heterodimerleri olarak bilinen küçük protein fermuarlarıyla bir arada tutulan “bölünmüş” bir baz düzenleyici tasarladı—moleküler cırt cırt benzeri. Baz düzenleyiciyi iki parçaya ayırdılar: birinde DNA hedefleme Cas9 nickazı, diğerinde ise düzenleme enzimi bulunuyor. Her yarıda bulunan kısa koil‑kıvrım peptitleri birbirlerini arayıp aynı DNA bölgesine ulaştıklarında birbirine kenetleniyor. Bu, C‑düzenleyici (CC‑CBE), A‑düzenleyici (CC‑ABE) ve farklı tür harf değişimleri yapabilen daha karmaşık varyantları içeren koil‑kıvrım baz düzenleyiciler (CC‑BEs) oluşturuyor. 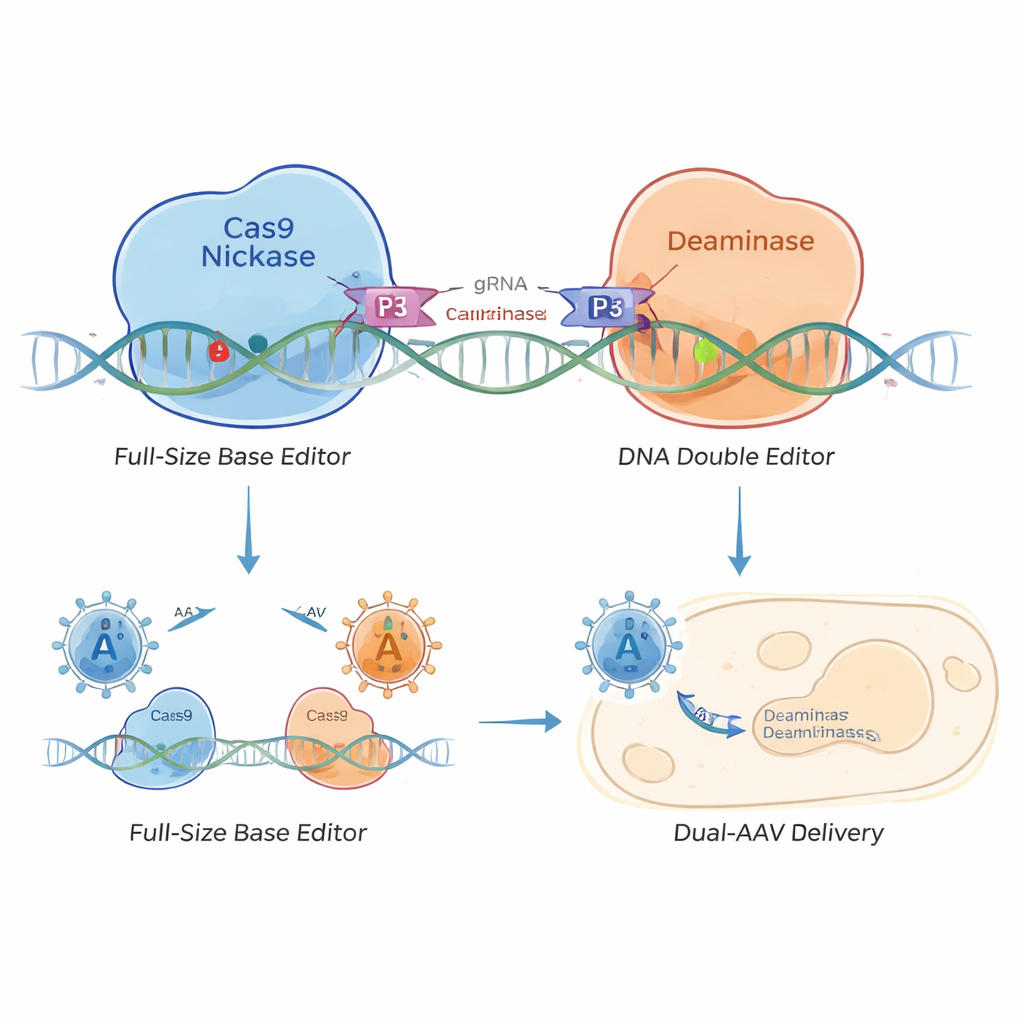
Esnek, Güçlü ve Hassas Düzenleme
Takım, CC‑BEs’i insan hücreleri ve primer domuz hücreleri de dahil çeşitli hücre tiplerinde ve daha geniş bir DNA dizisini tanıyabilen farklı Cas9 formlarıyla test etti. CC‑CBE varyantları birçok bölgede güvenilir biçimde çalışmakla kalmadı, aynı zamanda daha geniş bir “düzenleme penceresi” göstererek hedef harfleri DNA boyunca daha geniş bir aralıkta değiştirebildi; bu da araştırmacılara kılavuz RNA seçiminde daha fazla esneklik sağladı. CC‑ABE varyantları mevcut en iyi adeninin düzenleyicilerine benzer verimlere ulaştı ve genellikle daha az yan ürün üretti. Araştırmacılar ayrıca koil‑kıvrım stratejisini, kompakt TadCBE ve hassas ABE9 gibi daha yeni düzenleyici tasarımlarına uyarladı ve koil‑kıvrım çiftleriyle bölmenin performansı koruduğunu veya artırdığını yine gözlemledi.
Hücre Kabından Canlı Farelere
En önemlisi, yazarlar bu bölünmüş düzenleyicilerin, her viral parçacığın düzenleyicinin yarısını taşıdığı çift‑AAV teslimi kullanılarak canlı hayvanlarda çalıştığını gösterdi. Farelerde karaciğerde Pcsk9 genini hedefleyen bir CC‑ABE, A‑den‑G’ye değişimleri yaklaşık %70’e varan oranlarda elde etti, Pcsk9 proteinini ve kan LDL kolesterolünü keskin şekilde düşürdü ve karaciğer hasarına dair belirti göstermedi. 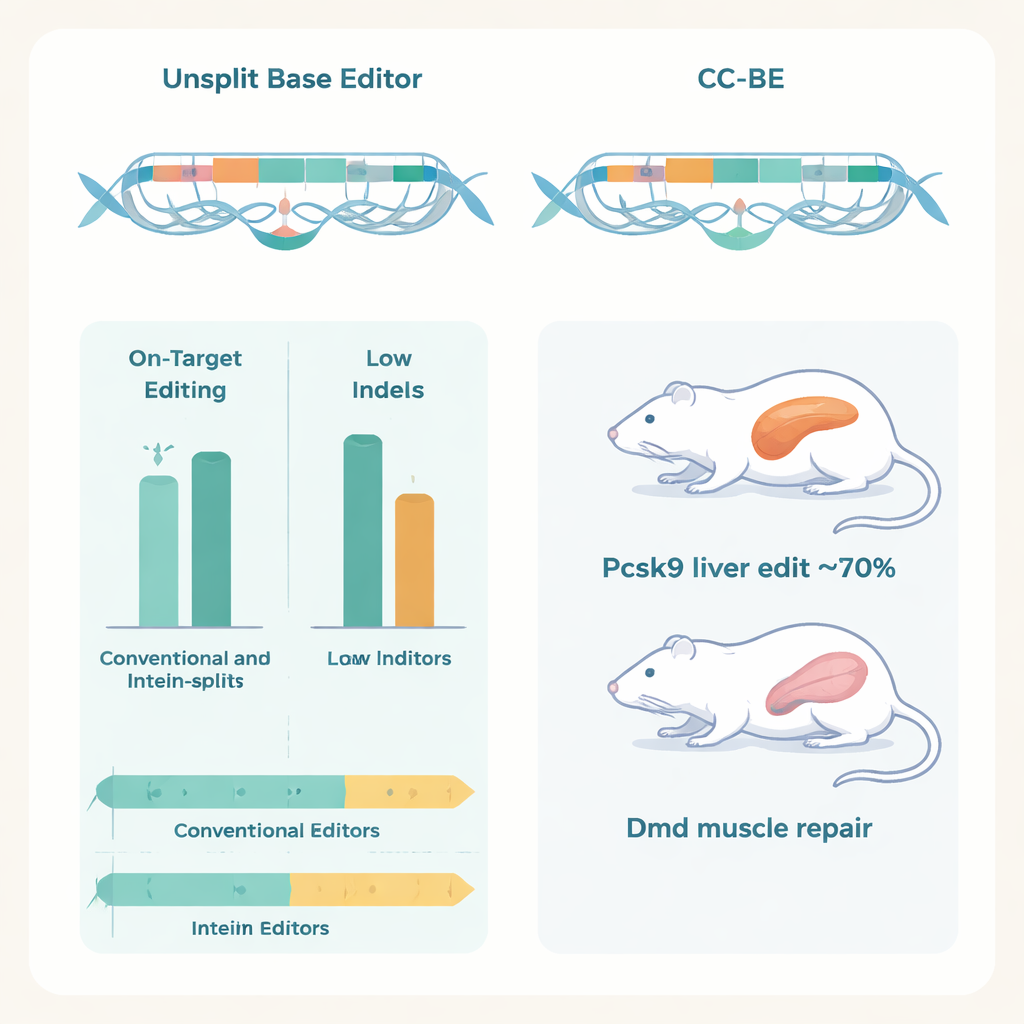
Pratik DNA Onarımına Doğru Yeni Bir Yol
Özetle, bu çalışma basit ama güçlü bir mühendislik numarası sunuyor: büyük baz düzenleyicileri, ihtiyaç duyuldukları yerde yeniden birleşecek şekilde AAV‑boyutunda modüllere bölmek için küçük koil‑kıvrım “kancalar” kullanın. Uzman olmayanlar için çıkarım şu: bilim insanları artık yüksek kapasiteli DNA onarım araçlarını klinik olarak kanıtlanmış viral taşıyıcılara paketleyebiliyor; doğruluk veya gücü feda etmeden. Bu koil‑kıvrım yaklaşımı, karaciğer, kalp ve kas gibi organlarda tek harfli genetik hastalıkların tedavilerini tasarlamayı kolaylaştırarak hassas gen düzeltmeyi gerçek dünya terapilerine bir adım daha yaklaştırabilir.
Atıf: Mu, S., Li, Q., Chen, M. et al. Coiled-coil heterodimer-mediated split base editing systems enable flexible and robust nucleotide substitutions. Nat Commun 17, 1765 (2026). https://doi.org/10.1038/s41467-026-68469-2
Anahtar kelimeler: baz düzenleme, gen terapisi, CRISPR, AAV ile teslim, genetik hastalık