Clear Sky Science · tr
Kolorektal kanser aşı yanıtını artırmak için makrofajların epigenetik ve metabolik yeniden programlanmasında glukanla indüklenen eğitilmiş bağışıklığın kullanımı
Vücudun İlk Müdahale Edenlerini Yeniden Uyandırmak
Kolorektal kanser, dünyadaki en ölümcül kanserlerden biridir ve çoğu hasta bugünkü immünoterapilerden fayda görmemektedir. Bu çalışma ilginç bir fikri araştırıyor: ya doğuştan gelen bağışıklık sistemini—vücudun ilk müdahale edenlerini—"eğiterek" tehlikeyi hatırlamasını sağlayıp aşıların kolorektal tümörlere karşı daha etkili olmasına yardımcı olabilseydik? Mayadan elde edilen doğal bir şeker olan beta‑glukanı kullanarak, araştırmacılar erken bağışıklık hücrelerinin yeniden programlanabileceğini ve böylece kanser aşılarının tümörlere karşı daha güçlü, daha uzun süreli saldırılar başlatmasını sağlayabileceğini gösteriyorlar.
Kolorektal Kanserin Yeni Savunmalara İhtiyacı Neden Var
Kolorektal kanser dünya çapında yılda neredeyse bir milyon ölüme yol açıyor ve genç yetişkinlerde vakalar artıyor. Cerrahi, kemoterapi ve radyasyon gibi standart tedaviler etkili olabiliyor, ancak birçok hasta nüks yaşıyor ve ciddi yan etkilerle karşılaşıyor. Checkpoint inhibitörleri gibi daha yeni bağışıklık temelli ilaçlar, yalnızca özel DNA tamir kusurlarına sahip dar bir kolorektal kanser alt grubunda çok iyi çalışıyor. Hastaların çoğu için bu ilaçlar ve deneysel kanser aşıları bile, tümör ortamının bağışıklık saldırısını baskılayan hücreler ve sinyallerle dolu olması nedeniyle yetersiz kalıyor.
Doğuştan Gelen Bağışıklığa Yeni Beceriler Öğretmek
Vücudun doğuştan gelen bağışıklık hücreleri—özellikle makrofajlar—genellikle tehditlere hızlı ama kısa süreli yanıt verir ve hafızadan yoksun oldukları düşünülür. Ancak son on yılda yapılan çalışmalar, güçlü bir ilk uyarının bu hücrelerde kalıcı izler bırakarak daha sonra daha güçlü yanıt vermelerini sağlayan "eğitilmiş bağışıklık"ı ortaya koydu. Yazarlar bu eğitilmiş durumu indüklemek için maya hücre duvarı bileşeni olan beta‑glukanı kullandılar. Farelerde, bütün beta‑glukan partikülleriyle kısa süreli tedavi, makrofajları hem gen aktivitesi hem de hücre metabolizması düzeyinde yeniden programladı. Bu eğitilmiş hayvanlar daha sonra mühendislik ile hazırlanmış bir adenovirüs tabanlı kolorektal kanser aşısı (PeptiCrad) aldığında, bağışıklık sistemleri tümör‑spesifik hedefleri tanımada ve onlara saldırmada daha yetkin öldürücü T hücreleri üretti. 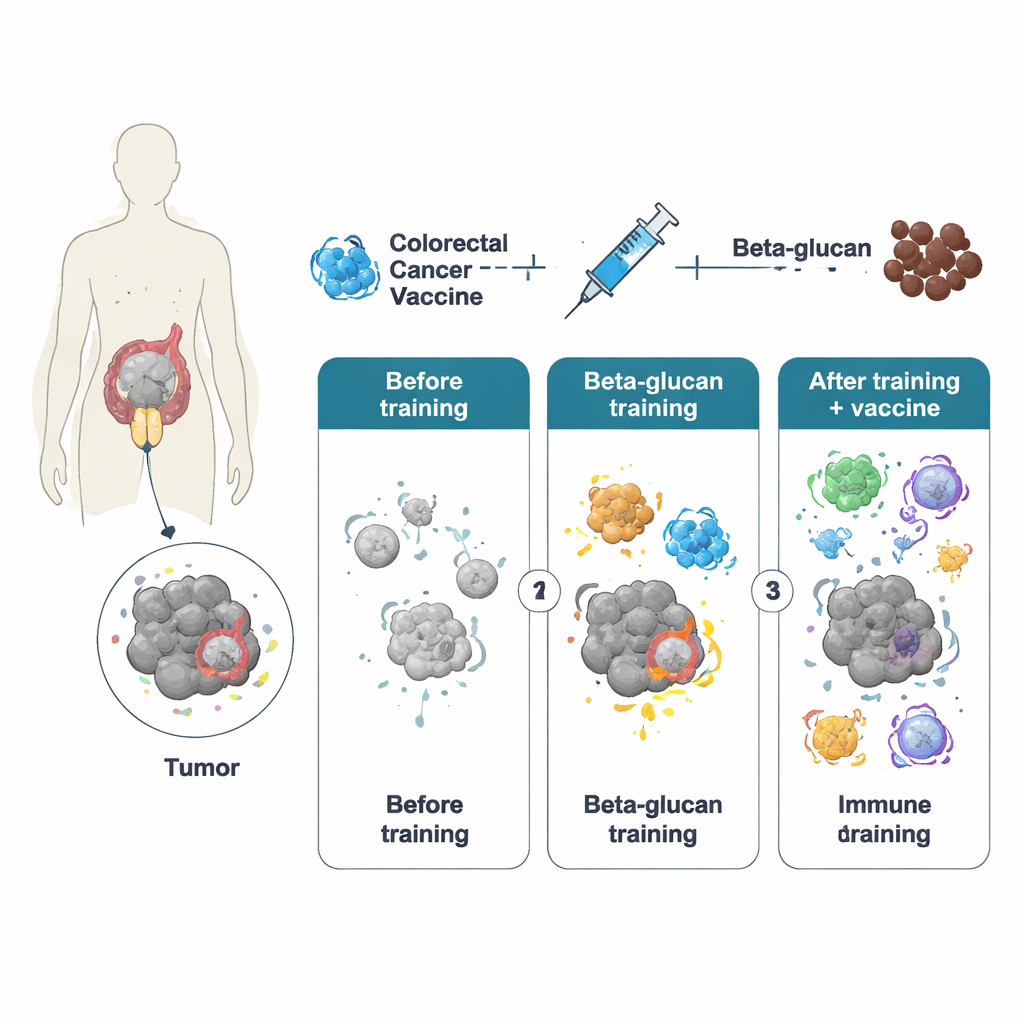
Tümör İçinde Enerji ve İletişimi Yeniden Kurmak
Daha derinlemesine inmek için araştırmacılar tümörlerden bağışıklık hücrelerini izole edip her birinin metabolizmasını ve gen aktivitesini tek tek profillendirdiler. Eğitilmiş makrofajların şekerleri hızla yakan ve kaynakları büyüme ve işlev için yapı taşlarına yönlendiren "Warburg etkisi"ni andıran yüksek devirli bir metabolik moda geçtiklerini buldular. Bu hücreler ayrıca daha çok bilinen kreatin metabolizmasını artırdı—spor takviyelerinden bilinen bir yol—ve bu, inflamatuar moleküller üretmek için gereken ekstra enerjiyi sağlamaya yardımcı oldu. Aynı zamanda DNA'ya bağlı proteinler üzerindeki belirli kimyasal işaretler (özellikle H3K4me3 artışı) kemokin üretiminde yer alan genleri işaretleyerek, zaman içinde devam eden pro‑inflamatuar ve tümörle savaşan bir programı etkin bir şekilde kilitledi.
Bir Bağışıklık Bayraklaşma Ekibi Kurmak
Tek hücre dizilemesi, tümör içindeki farklı bağışıklık hücreleri arasında adım adım bir bayraklaşma olduğunu ortaya koydu. İlk olarak, eğitilmiş makrofajlar iki ana sinyal olan CXCL9 ve CXCL10'u yüksek düzeyde salgıladı ve bunlar CXCR3 adlı bir reseptör aracılığıyla doğal öldürücü (NK) hücreleri çekti. Bir kez görevlendirildiklerinde, bu NK hücreleri sadece kanser hücrelerini öldürmekle kalmadı; ayrıca uzman bir dendritik hücre alt kümesi olan cDC1'i çeken başka bir haberciyi, CCL5'i salgıladı. Bu dendritik hücreler tümör parçalarını T hücrelerine sunmada ustadır. Sonuç olarak, daha fazla CD8 T hücresi aktive oldu ve tekrar tümörle karşılaştıklarında hızlı ve güçlü yanıt veren efektör bellek hücrelerine dönüştü. Kreatin kullanımının engellenmesi, makrofajların veya NK hücrelerinin yok edilmesi ya da bu kemokin yollarının kesilmesi tümör kontrolünü zayıflattı; bu da aşı başarısının bu makrofaj–NK–dendritik hücre–T hücresi devresine ne kadar bağımlı olduğunu vurguladı. 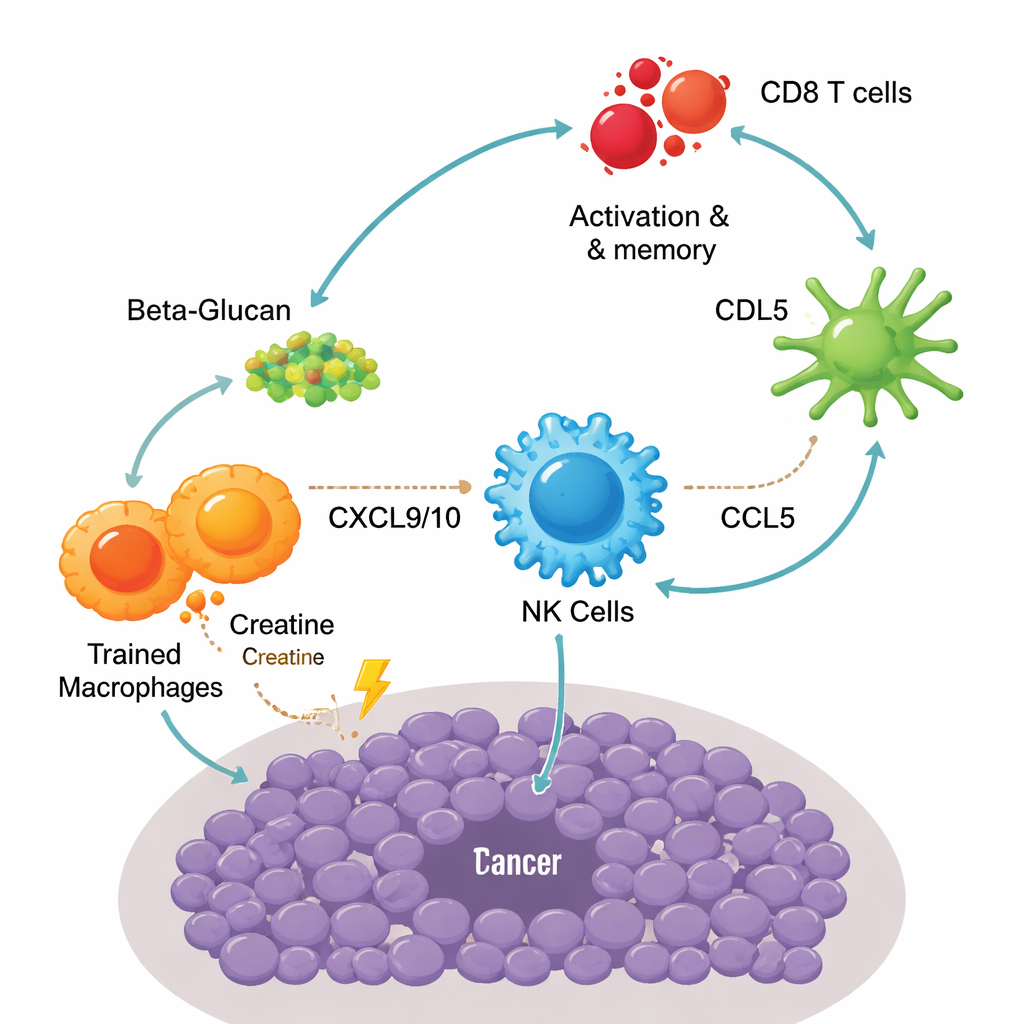
Fare Modellerinden İnsan Tümör Organoidlerine
Ekip yaklaşımını, yaygın immünoterapilere dirençli özellikle inatçı bir tür de dahil olmak üzere birkaç kolorektal kanser fare modelinde test etti. Her durumda, beta‑glukan eğitimi ile aşının kombinasyonu tek başına verilen tedavilerden daha etkili bir şekilde tümör büyümesini yavaşlattı. Önemli olarak, çalışmayı farelerin ötesine taşıdılar. Beta‑glukana maruz bırakılan insan kan hücreleri, kolorektal kanser aşı peptidine daha iyi yanıt vererek daha fazla immün‑uyaran sitokin üretti. Bu eğitilmiş bağışıklık hücreleri genişletilip hasta kaynaklı mini kolorektal tümörler (organoidler) ile birlikte kültürlendiğinde, eğitilmemiş hücrelerden daha fazla kanser hücresini öldürdüler. İnsan monositleri ve makrofajları sistemden çıkarıldığında bu fayda ortadan kalktı; bu da bu eğitilmiş hücrelerin doğrudan tümör katilleri olmaktan çok, vazgeçilmez organize ediciler olduğunu doğruladı.
Geleceğin Kanser Aşıları İçin Anlamı Ne Olabilir
Basitçe söylemek gerekirse, bu çalışma güvenli, mayadan türetilmiş bir şekerin doğuştan gelen bağışıklık hücrelerini daha etkili kolorektal kanser aşılama süreçlerini destekleyecek şekilde "eğitebileceğini" gösteriyor. Makrofajların enerji kullanımını ve hangi genleri harekete hazır tuttuklarını yeniden düzenleyerek, beta‑glukan eğitimi bir domino etkisi başlatıyor: makrofajlar NK hücrelerini çağırıyor, NK hücreleri uzman dendritik hücreleri işe alıyor ve birlikte bellek CD8 T hücrelerinden daha güçlü bir ordu inşa ediyorlar. Güvenlik, zamanlama ve en iyi aşı kombinasyonları dahil olmak üzere klinik denemelerde test edilmesi gereken çok şey kalsa da—eğitilmiş bağışıklık burada, daha soğuk, baskıcı kolorektal tümörleri bağışıklık sisteminin tanıyıp kontrol edebileceği hale getirme yönünde umut verici bir adjuvan strateji olarak ortaya çıkıyor.
Atıf: Hamdan, F., Gandolfi, S., D’Alessio, F. et al. Leveraging glucan-induced trained immunity for the epigenetic and metabolic rewiring of macrophages to enhance colorectal cancer vaccine response. Nat Commun 17, 1757 (2026). https://doi.org/10.1038/s41467-026-68466-5
Anahtar kelimeler: kolorektal kanser immünoterapisi, eğitilmiş bağışıklık, beta‑glukan, makrofajlar ve NK hücreleri, kanser aşıları