Clear Sky Science · tr
ClpC1 hedefleyen peptid doğal ürünleri Mycobacterium tuberculosis proteomunu farklı biçimlerde bozar
Neden bakteriyel temizlik ekiplerini bozmak önemlidir
Tüberküloz dünyadaki en ölümcül enfeksiyon hastalıklarından biri olmaya devam ediyor ve Mycobacterium tuberculosis’in ilaç dirençli suşları tedaviyi zorlaştırıyor. Mevcut antibiyotiklerin çoğu bakterinin hücre duvarına veya enerji üretme ve genetik materyali kopyalama yeteneğine saldırır. Bu çalışma çok farklı bir zayıf noktayı araştırıyor: hücrenin protein sağlığını koruyan iç “temizlik ekibi.” Yeni doğal ürün türevi moleküllerin bu temizlik sistemini nasıl bozduğunu anlayarak, bilim insanları TB bakterilerini yeni ve daha kalıcı yollarla öldürebilecek ilaçlar tasarlamayı hedefliyor.
Hücrenin protein ev temizliği merkezi
Tüm canlı hücreler gibi TB bakterisi de sürekli olarak proteinler üretir, katlar, onarır ve geri dönüştürür. Bu protein bakım ağının merkezi bir oyuncusu ClpC1–ClpP1P2 adlı büyük bir makinedir. Bir parça (ClpC1) şaperon gibi davranarak hasarlı veya gereksiz proteinleri tanır ve içeri çeker, diğer parça (ClpP1P2) ise bunları geri dönüşüm için parçalara ayırır. Bu sistem, özellikle ısı veya antibiyotik saldırısı gibi stres altında bakterinin hayatta kalması için esastır. Birkaç doğal peptid bileşik—ecumicin, ilamysinler (rufomysinler) ve cyclomarinler—zaten ClpC1’e bağlandığı ve güçlü TB öldürücü aktivite gösterdiği biliniyor; bu da bu kompleksin güçlü bir ilaç hedefi olabileceğini düşündürüyor. 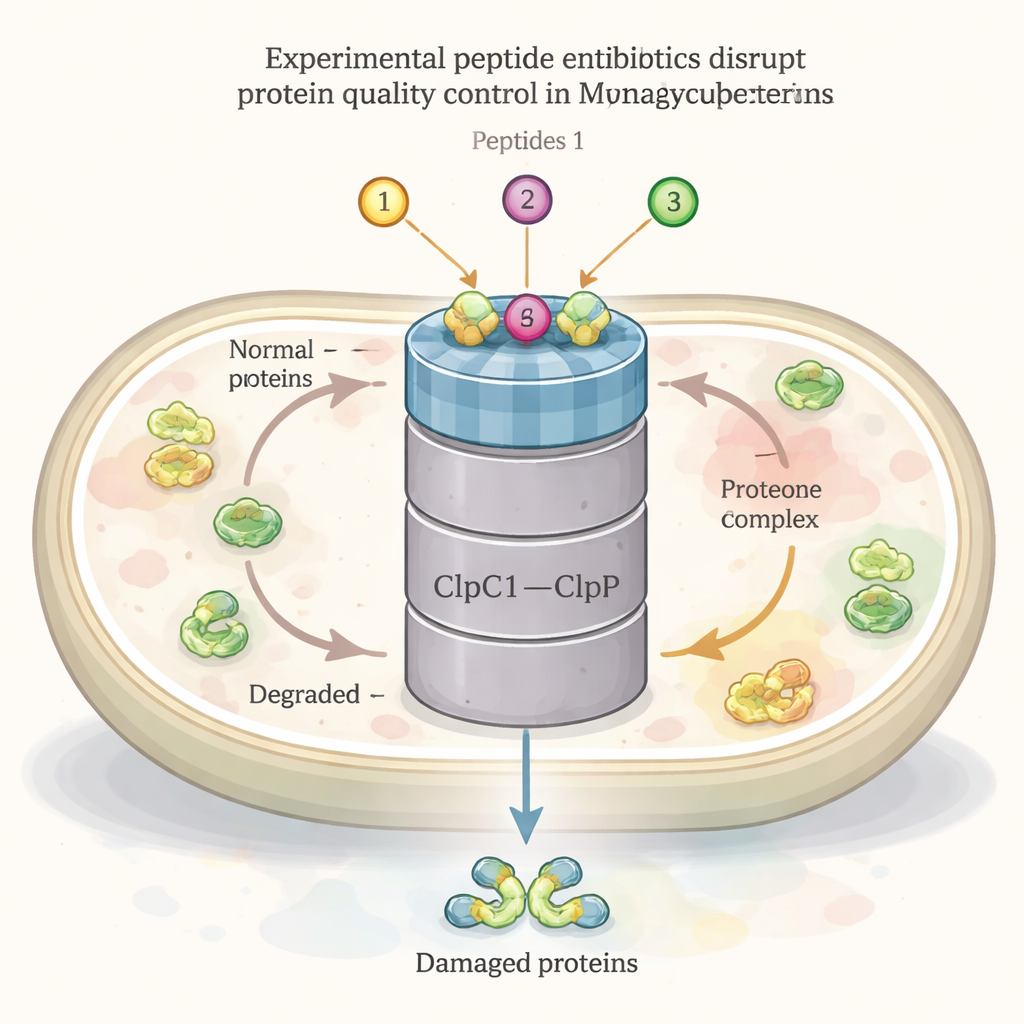
Üç akraba ilaç, üç farklı etki
Araştırmacılar üç peptid ailesinden birer temsilci incelediler: bir ecumicin analoğu (Ecu*), ilamycin E (IlaE) ve bir cyclomarin türevi (desoxycyclomarin, dCym). Hepsi ClpC1’in aynı bölgesine tutunmasına rağmen, hücre içinde aynı şekilde davranmıyorlar. Binlerce proteini aynı anda ölçen nicel proteomik kullanarak, Ecu*’un en geniş bozulmayı tetiklediğini; tüm bakteri proteinlerinin yaklaşık %17’sinin seviyelerini önemli ölçüde değiştirdiğini saptadılar. IlaE yaklaşık %12, dCym ise yaklaşık %7 oranında değişime yol açtı. Sadece 72 protein üç bileşik tarafından tutarlı şekilde etkilendi ve bunların çoğu bollukta azalma gösterdi. Bu, her molekülün ClpC1 makinesini farklı bir yöne ittiğini; makineyi basitçe “kapamak” yerine hücrenin protein manzarasını özgün biçimlerde yeniden şekillendirdiğini gösteriyor.
Rendeyi tıkamak mı yoksa gücü kesmek mi
Bu etkileri bağlam içinde değerlendirmek için ekip peptidleri, protein parçalayan enzimleri geniş biçimde engelleyen kanser ilacı bortezomib ile karşılaştırdı. TB bakterilerinde bortezomib, rendeler kapatıldığında beklendiği üzere birçok proteinin genel birikimine yol açtı. Buna karşılık peptidler daha seçici desenler üretti: bilinen bazı ClpC1 hedefleri birikti, bazıları tükenmişti ve tüm protein parçalanmasının küresel olarak inhibe edilmesi gözlenmedi. Saf bileşenlerle yapılan detaylı laboratuvar testleri her peptidin belirli substratların nasıl işlendiğini değiştirdiğini gösterdi. Örneğin, üçü de bir düzenleyici proteinin (PanD) yıkımına müdahale etti, ama yalnızca Ecu* model bir düzensiz proteinin parçalanmasını engelledi ve yalnızca dCym stres koruyucu protein Hsp20’nin yıkımını bozdu. Bu farklılıklar, hedef proteinin genel şekli ve esnekliğinin, ClpC1’in belirli bir bileşik tarafından “yanlış ayarlandığında” nasıl etkilendiğini belirlemede rol oynadığını düşündürür. 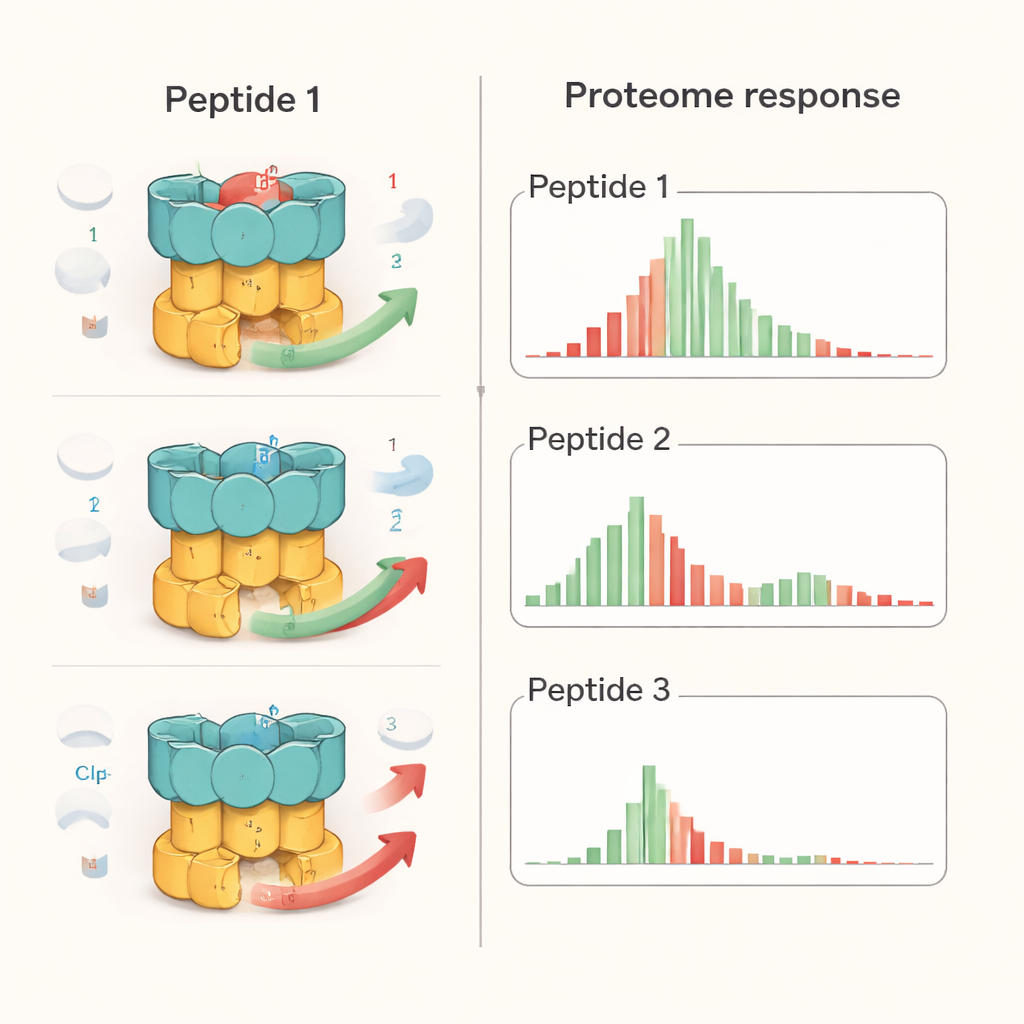
Stres yanıtlayıcılar ve bakterinin kendi kendini kurtarma yolları
Protein hasarı ana temizlik makinesinin üstesinden geldiğinde TB bakterisinin başa çıkmak için yedek sistemleri vardır. Bu sistemlerden biri, cyclomarin-benzeri moleküllere bağlanabilen ve bunların ClpC1 üzerindeki etkisini azaltabilen başka bir şaperon olan ClpC2’yi içerir. Bu çalışma, üç peptidin de deney tüpünde ClpC2’ye bağlanabildiğini buldu; ama sadece cyclomarin türevi (dCym) canlı bakterilerde ClpC2 düzeylerini yükseltti ve ClpC2 deneysel olarak azaltıldığında daha güçlü hale geldi. Buna karşılık Ecu* ve IlaE, ClpC2 azaltıldığında bile etkili kalmaya devam etti; bu da bunların büyük ölçüde bu kendi kendini kurtarma yolunu atlatabildiğini düşündürüyor. Ekip ayrıca Hsp20 ile güçlü, bileşik-spesifik bir bağ keşfetti: Ecu* (ve daha az ölçüde IlaE) Hsp20 seviyelerinde dramatik artışlara yol açtı ve Ecu* doğrudan Hsp20’ye bağlandı; bu da bu ilaç adayları ile hücrenin stres yanıt ağı arasında yeni bir bağlantıyı ortaya koyuyor.
Stresi terapötik avantaja dönüştürmek
ClpC1 sistemi özellikle zor koşullar altında önemli olduğundan, araştırmacılar bakterilere hafif ısı stresi uygulanırken ilaçları test ettiler; bu koşul yanlış katlanmış protein yükünü artırır. Bu koşullar altında Ecu* ve dCym çok daha öldürücü hale geldi ve daha seçici etki göstermelerine rağmen bortezomib’e benzer toksisite düzeylerine ulaştılar. Bu, protein kalite kontrol mekanizmasını dikkatli şekilde hedeflemenin, tüm büyük proteazları kapatmak kadar etkili olabileceğini, fakat potansiyel olarak daha hassas kontrol sunabileceğini gösteriyor. Çalışma ayrıca Ecu*’un neden olduğu birçok protein düzeyi değişiminin yalnızca gen aktivitesindeki değişiklikleri yansıtmadığını; ClpC1’in bozulmasının esas olarak proteinler üretildikten sonra düzenlemede bozulmaya yol açtığını vurguladı.
Gelecekteki TB tedavileri için ne anlama geliyor
Uzman olmayanlar için ana mesaj şudur: TB bakterileri hayatta kalmak için hassas dengedeki bir iç temizlik ve stres yanıt sistemine güvenir. Burada test edilen üç doğal ürün türevi peptid hepsi aynı merkezi makineye tutunuyor, ama onu farklı modlara iterek bakterinin protein yapısında çeşitli ve son derece özgül bozulmalara yol açıyor. Önemli olarak, ecumicin-benzeri ve ilamycin-benzeri bileşikler, cyclomarin’in etkisini azaltabilen dahili bir bakteriyel kurtarma mekanizmasından kaçınıyor, yine de patojeni stres altında çökertiyor. Bu özellikler onları gelecekteki tüberküloz ilaçları için umut verici iskeletler yapıyor; örneğin TB hücrelerini seçici olarak hayati proteinlerini yok etmeye zorlayacak tasarım moleküller veya bakterinin kendi kendini sindirmesini hassas biçimde yönlendirecek “protein-hedefleyen kimera”lara dönüştürülebilirler.
Atıf: Barter, I.K., Bedding, M.J., Leodolter, J. et al. ClpC1-targeting peptide natural products differentially dysregulate the proteome of Mycobacterium tuberculosis. Nat Commun 17, 1725 (2026). https://doi.org/10.1038/s41467-026-68423-2
Anahtar kelimeler: tüberküloz, protein kalite kontrolü, ClpC1, antibiyotik direnci, doğal ürün antibiyotikleri