Clear Sky Science · tr
e2MPRA kullanarak eşzamanlı epigenomik profilleme ve düzenleyici aktivite ölçümü
Hücresel Gizli Anahtarları Okumak
Vücudunuzdaki her hücre temelde aynı DNA’yı taşır, ancak bir beyin hücresi ile bir karaciğer hücresi çok farklı davranır. Sır, genleri açıp kapatan, kısan veya yükselten dimmer anahtarları gibi davranan kısa DNA dizilerindedir. Bu çalışma, bilim insanlarının bu anahtarlardan binlercesini aynı anda test etmesine olanak tanıyan ve aynı zamanda DNA’nın hücre içinde nasıl paketlendiğini ve işaretlendiğini izlemeyi sağlayan güçlü yeni bir araç, e2MPRA’yı tanıtıyor—gelişim, hastalık riski ve bazı genetik varyantların neden önemli olup bazılarının olmadığını anlamaya yönelik anahtar adımlar.
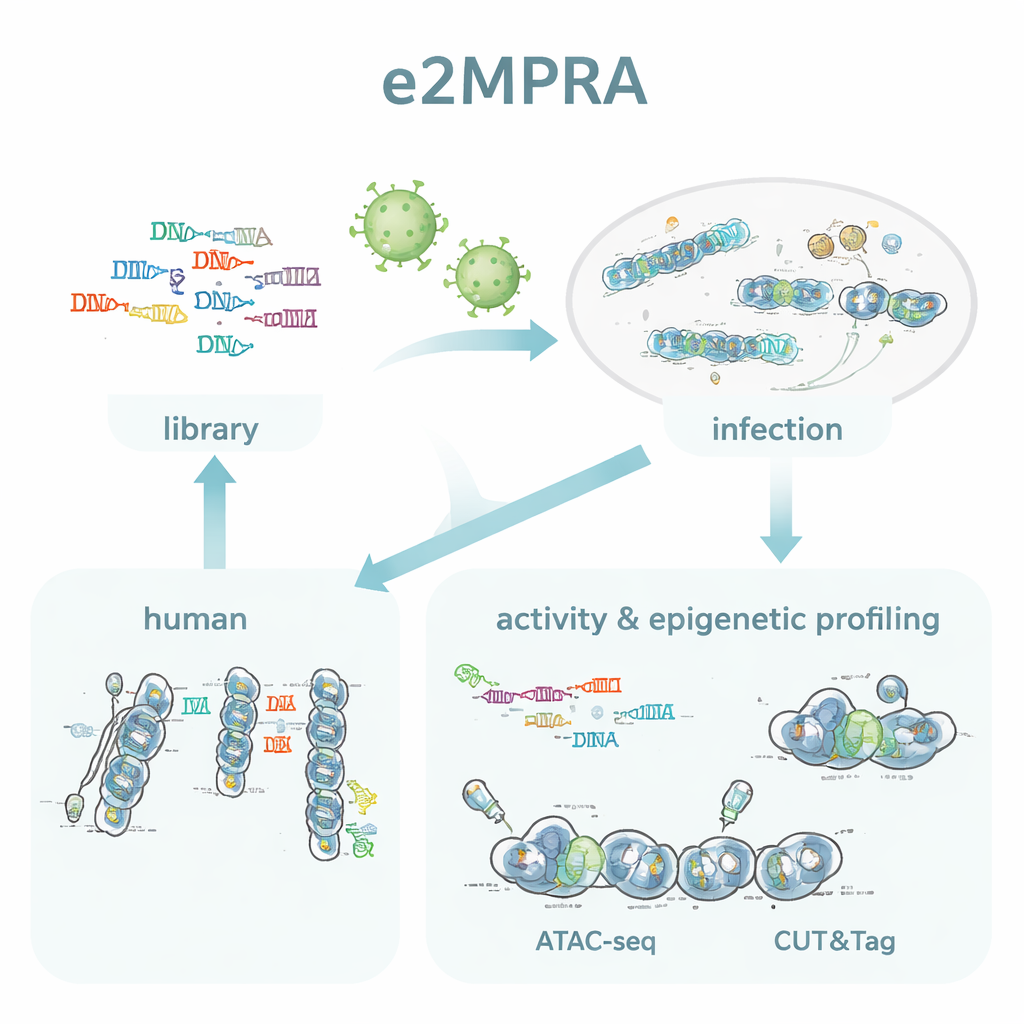
DNA Haritalarından DNA İşlevine
Son on yılda araştırmacılar, cis-düzenleyici elemanlar olarak bilinen "aday" düzenleyici anahtarların devasa haritalarını çıkardı. DNA’nın nerede gevşek paketlendiğini (açık kromatin), hangi proteinlerin bağlandığını ve çevreleyen DNA’yı hangi histon işaretlerinin süslediğini gösteren yöntemler kullanıyorlar. Bu haritalar etkileyici, ama çoğunlukla betimleyici: bir proteinin bağlanması veya bir işaretin görünmesi, bir dizinin gerçekten gen aktivitesini kontrol ettiğini kanıtlamaz. Geleneksel çoklu paralel raporlayıcı analizleri (MPRA’lar) binlerce DNA parçasının bir raporlayıcı geni güçlendirip güçlendirmediğini ya da susturup susturmadığını test edebilir, ancak orada hangi proteinlerin bağlandığını veya o aktiviteyle hangi epigenetik değişikliklerin eşlik ettiğini söylemezler.
Aktivite ve Epigenetik İşaretler için İki’si Bir Arada Bir Analiz
Yazarlar, lentiviral bir MPRA’yı ATAC-seq ve CUT&Tag adlı iki epigenomik teknikle harmanlayarak e2MPRA’yı oluşturdu. İlk olarak, her aday düzenleyici dizinin kısa bir barkodla ilişkili olduğu ve minimal bir promotör ile raporlayıcı genin yanında yer aldığı bir DNA kütüphanesi inşa ediyorlar. Bu kütüphane daha sonra lentiviralara paketlenip kültürdeki insan hücrelerinin genomlarına birçok kez entegre ediliyor. Aynı hücre havuzundan, düzenleyici aktiviteyi ölçmek için RNA’daki barkodları okuyorlar ve eklenen dizilerde kromatin açıklığını ve kritik bir histon işareti (H3K27ac) ölçmek için ATAC-seq ve CUT&Tag kullanıyorlar. Bu sinyalleri her dizinin gerçekte ne sıklıkta entegre olduğuna göre normalleştirerek, tek bir deneyde binlerce eleman için "açık/kapalı gücü" ve epigenetik durumu yan yana ölçmüş oluyorlar.
Transkripsiyon Faktörü Motiflerinin Birlikte Nasıl Çalıştığını Kod Çözme
Bu teknolojinin neler açığa çıkardığını görmek için ekip, karaciğer hücrelerinde kullanılan bilinen transkripsiyon faktörü motiflerinden sentetik enhancer’lar oluşturdu. Bu motifleri nötr DNA şablonları üzerine farklı sayı ve sırayla dizdiler. HNF1A ve XBP1 gibi bazı faktörler klasik aktivatörler gibi davrandı: daha fazla kopya eklemek raporlayıcı çıktısını artırdı. HNF1A ve ONECUT1 gibi diğerleri öncülük faktörleri olarak kapalı DNA’yı açma rollerine uygun şekilde esas olarak kromatin açıklığını güçlendirdi. PPARA farklı bir desen gösterdi; kendi başına güçlü şekilde kromatin ve histon işaretlerini değiştirdi ama tek başına transkripsiyonu çok etkilemedi, yine de diğer faktörlerle iş birliği yaparak gen aktivitesini artırdı. Bilinen bir baskılayıcı olan REST, aktivatörlerin yanına yerleştirildiğinde aktiviteyi azalttı. Dikkat çekici şekilde, dört motifin basitçe yeniden sıralanması enhancer gücünü önemli ölçüde değiştirebiliyordu ve aktivatörler promotöre daha yakın olduklarında genellikle daha iyi çalışıyordu; bu, bu motiflerin düzenlenmesinde bir tür dilbilgisel yapı olduğunu gösteriyor.
Pluripotensite Enhancer’larında Hassas Bazların Belirlenmesi
Araştırmacılar daha sonra kök hücre kimliği için önemli enhancer’lara, özellikle POU5F1 (OCT4 olarak da adlandırılır) ve SOX2 tarafından bağlanan bölgelere odaklandı. Her 100 baz çiftlik enhancer’ın her bazının sistematik olarak değiştirildiği yoğun mutasyon kütüphaneleri ve küçük altı bazlık pencerelerin rastgele karıştırıldığı diziler oluşturdular. İndüklenmiş pluripotent kök hücrelerde e2MPRA kullanarak hangi mutasyonların raporlayıcı aktivitesini zayıflattığını veya güçlendirdiğini ve bunların kromatin açıklığı ile asetilasyonu nasıl etkilediğini görebildiler. POU5F1::SOX2 bağlanma motifinin bozulması sıklıkla hem gen aktivitesini hem de epigenetik işaretleri azalttı ve bu motifin merkezi rolünü doğruladı. POU5F1 genine yakın iyi çalışılmış bir enhancer’da, bir YY1 motifinin değiştirilmesinin transkripsiyonu artırırken kromatin açılmasını azalttığını da buldular; bu, bazı faktörlerin açık bir durumu teşvik ederken ifadeyi yine de sınırlayabileceğine işaret ediyor.
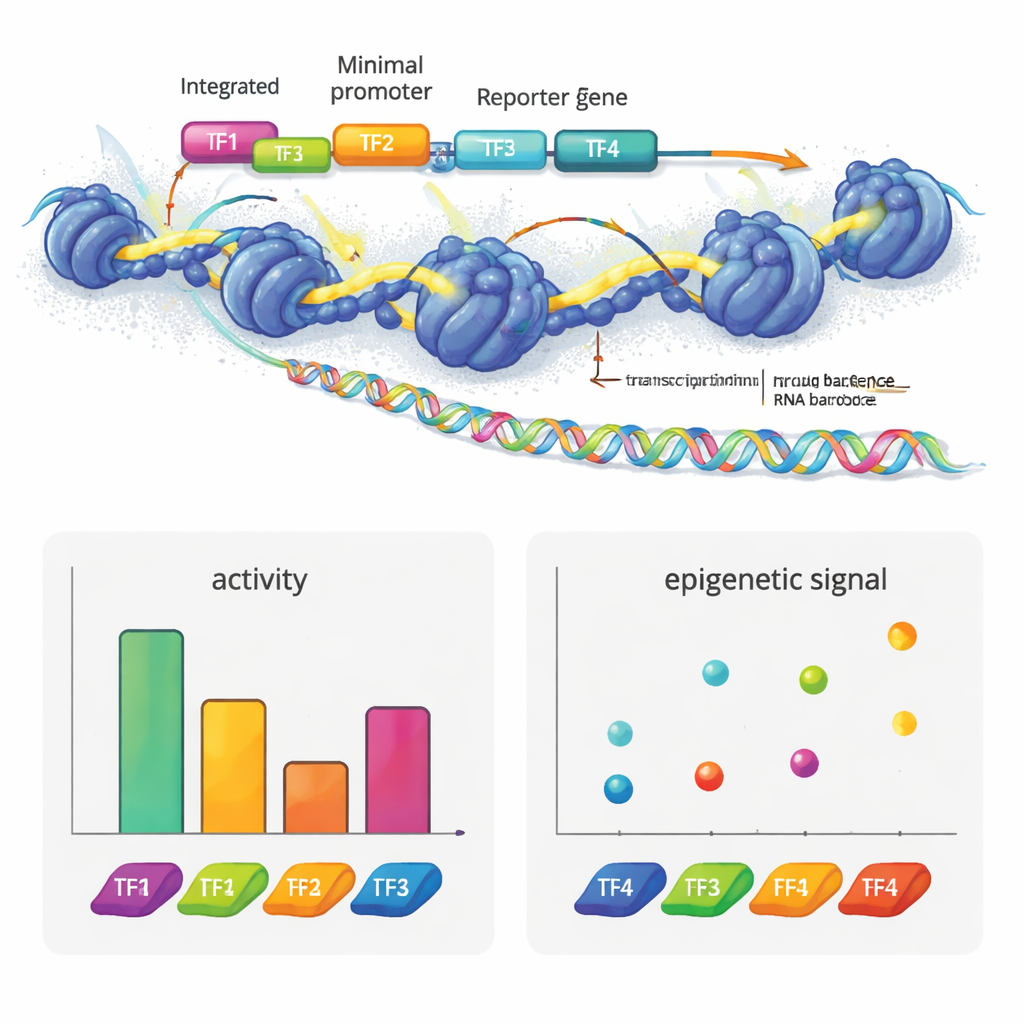
Genler ve Hastalık İçin Anlamı
e2MPRA genomun doğal üç boyutlu bağlantılarının her nüansını kusursuz şekilde yeniden üretmiyor, ancak binlerce düzenleyici dizi ve varyantı aynı koşullar altında karşılaştırmak için pratik bir yol sunuyor. Bir fonksiyonel ölçüm (bir DNA segmentinin bir geni ne kadar güçlü şekilde yönlendirdiği) ile epigenetik ölçümleri (o DNA’nın nasıl paketlendiği ve işaretlendiği) eşleştirerek bu yöntem, belirli transkripsiyon faktörü motiflerinin, kombinasyonlarının ve konumlarının neden bu kadar belirleyici olduğunu ortaya çıkarmaya yardımcı oluyor. Uzun vadede, e2MPRA gibi araçlar hastalıkla ilişkili kodlayıcı olmayan genetik varyantların yorumlanmasını kolaylaştırabilir, gen terapisi için sentetik enhancer’ların tasarlanmasını destekleyebilir ve DNA dizisini hücresel davranışa bağlayan daha tamamlayıcı bir "düzenleyici kod" inşa etmeyi hızlandırabilir.
Atıf: Zhang, Z., Georgakopoulos-Soares, I., Bourque, G. et al. Simultaneous epigenomic profiling and regulatory activity measurement using e2MPRA. Nat Commun 17, 1724 (2026). https://doi.org/10.1038/s41467-026-68422-3
Anahtar kelimeler: gen düzenlenmesi, enhancer’lar, epigenetik, transkripsiyon faktörleri, fonksiyonel genomik