Clear Sky Science · tr
Koruyucu ubiquitin E3 ligazları, kanserle ilişkili APOBEC3 deaminazlarını parçalanma için hedefleyerek insan genom bütünlüğünü destekler
DNA’mızı dost ateşinden korumak
Hücrelerimiz, viral DNA’yı zarar vererek enfeksiyonlarla mücadele etmemize yardımcı olan güçlü enzimler konuşlandırır. Ancak bu aynı enzimlerin bazıları denetimsiz kaldığında istemeden kendi genomumuza zarar verip kansere katkıda bulunabilir. Bu çalışma, insan hücrelerinin bu riskli enzimleri nasıl denetlediğini ortaya koyuyor ve tehlikeli formları DNA’yı yeniden yazmadan önce yok etmek için etiketleyen yerleşik bir “kalite kontrol” sistemini açığa çıkarıyor.
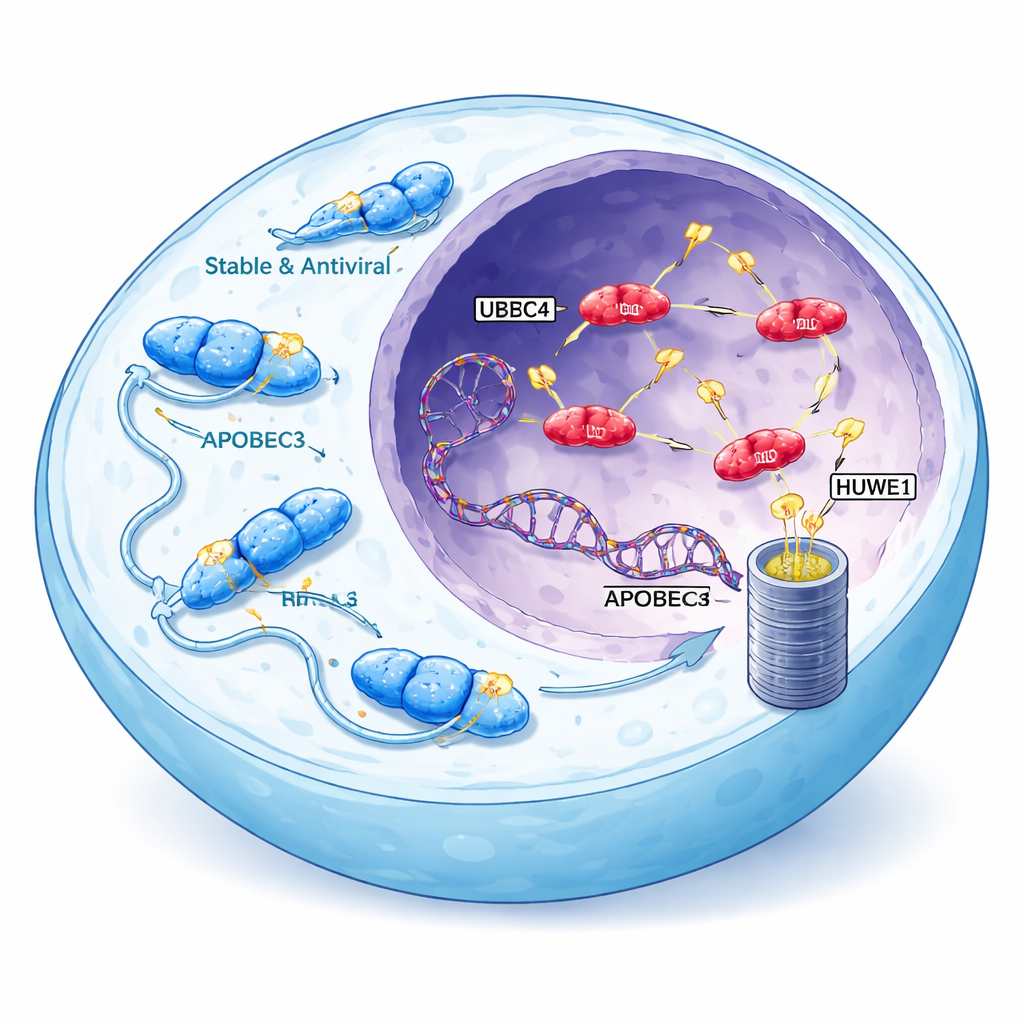
Bize karşı dönebilen virüs savaşçıları
APOBEC3 enzim ailesi, normalde HIV gibi virüslere karşı savunmaya yardımcı olur; viral DNA’yı kimyasal olarak değiştirerek ölümcül hatalar oluşturur. İnsanlarda yedi APOBEC3 varyantı bulunur ve bunların üçü—A3A, A3B ve A3H’nin haplotip I olarak adlandırılan bir formu (A3H-I)—birçok kanserde görülen mutasyon desenleriyle güçlü biçimde ilişkili bulunmuştur. Bu özel enzimler hücre çekirdeğine girerek kromozomlarımızda karakteristik mutasyon kümeleri oluşturabilir. APOBEC ile ilişkili bu imzalar, özellikle meme, akciğer ve mesane tümörlerinde, tüm insan kanserlerinin yarısından fazlasında görülür; bu imzalar tümörlerin uyum sağlamak ve tedaviye direnç geliştirmek için kullanabileceği genetik değişiklik havuzunu genişletir.
En tehlikeli formların neden şaşırtıcı şekilde kararsız olduğu
İlginç bir şekilde, kanserle en güçlü şekilde ilişkilendirilen APOBEC3 enzimleri aynı zamanda en az kararlı olanlardır. Virüslere karşı yüksek düzeyde biriken ve verimli şekilde engelleyen sitoplazmik akranlarının aksine, A3A, A3B ve A3H-I hızlıca parçalanır ve çekirdekte genellikle düşük konsantrasyonlarda bulunur. Araştırmacılar bu kararsızlığın kasıtlı olabileceğini düşündü: Hücreler çekirdekteki APOBEC3 proteinlerinin seviyelerini etkin şekilde sınırlıyorsa, bu kontrolün bozulması mutajenitenin patlamasına yol açabilir. A3H-I modelini kullanarak gösterdiler ki kanserle ilişkili APOBEC3’ler esas olarak proteazom tarafından, yani hücrenin protein öğütücüsü tarafından yok edilir; bu süreçte çoklu amino asit bölgelerine küçük moleküler “bayraklar” olan ubiquitin bağlanır.
Hücresel koruyucuları bulmak
A3H-I ve A3B’yi işaretleyen mekanizmayı belirlemek için ekip CRISPR taraması ile protein yakınlık haritalamayı birleştirdi. A3H-I ile zararsız varyantı A3H-II’nin ne kadar kararlı olduğuna bağlı olarak farklı şekilde parlayan hücreler tasarladılar ve ardından protein parçalanmasında rol alan genleri sistematik olarak bozup test ettiler. UBR4, UBR5 ve HUWE1 olmak üzere üç ubiquitin ligazı öne çıktı. Bu ligazlardan herhangi birinin ortadan kaldırılması, kararlı sitoplazmik A3H-II’yi etkilemeden kararsız, çekirdek A3H-I düzeylerini seçici olarak artırdı. Aynı ligazlar kolon ve bağışıklık hücresi hatlarında endojen A3B seviyelerini de bağımsız şekilde yükseltti ve üçünün aynı anda silinmesi A3B bolluğunda ek bir artış üretti. Biyokimyasal deneyler ayrıca UBR5 ve HUWE1’in A3B ve A3H-I’ye fiziksel olarak bağlandığını ve doğrudan ubiquitin zincirleri eklediğini, UBR4’ün ise bu zincirleri uzatarak proteinleri daha verimli biçimde yok edilmeye elverişli hale getirmede uzmanlaştığını gösterdi.
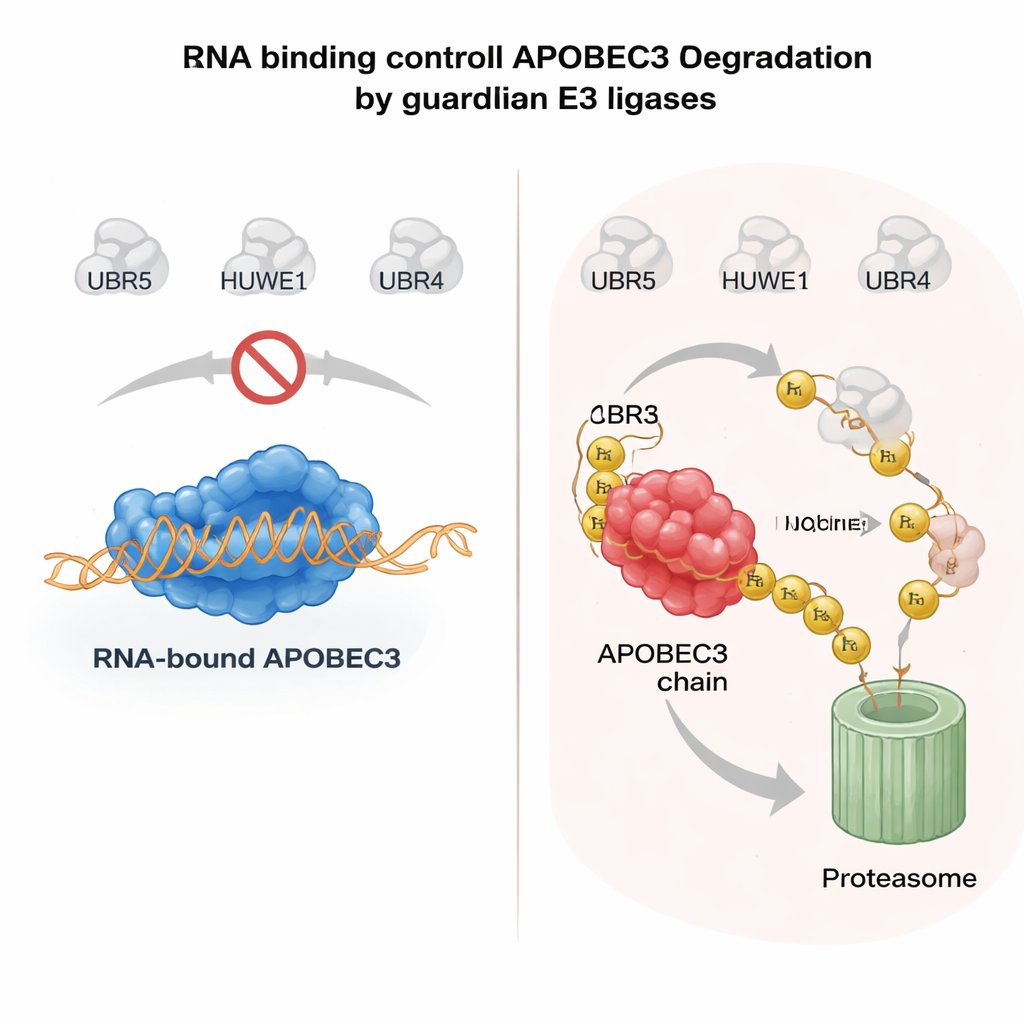
Riskli enzimler için RNA’nın emniyet kemeri rolü
Bir APOBEC3 enziminin korunup korunmayacağını ne belirler? Anahtar ipucu, APOBEC3 proteinlerinin sitoplazmadaki RNA moleküllerine bağlanma biçiminden geldi. A3H veya aileden bir başka üye olan A3G RNA’ya bağlandığında, genellikle sitozolde büyük komplekslerde kalır ve nispeten stabildir. RNA bağlanmasını zayıflatan mutasyonlar bu enzimlerin çekirdeğe kaymasına, koruyucu ortaklarını kaybetmesine ve oldukça kararsız hale gelmesine neden olur. Yazarlar, APOBEC3 proteinleri RNA’ya bağlı olmadığında UBR5 ve HUWE1’in enzimde açığa çıkan yüzeyleri tanıdığını, bunları ubiquitin ile süsleyip çekirdekte parçalanmaya yönelttiğini gösterdi. Saflaştırılmış sistemlerde RNA’yı uzaklaştırmak için RNase eklemek bu ligazların APOBEC3’e bağlanma ve ubikitinasyon yeteneğini büyük ölçüde artırdı; bu da RNA bağlanmasının moleküler bir kalkan görevi gördüğünü doğruladı. Bu mekanizma hücrelerin antiviral APOBEC3’leri sitoplazmada aktif tutmasına ve çekirdekteki bağlı olmayan, genom için tehdit oluşturan havuzları hızla temizlemesine olanak tanır.
Koruyucular başarısız olduğunda: kanser mutasyonlarıyla bağlantılar
UBR4, UBR5 ve HUWE1 koruyucu rolündeyse, bunların kaybı mutasyon düzeylerini artırmalıdır. Araştırmacılar bunu kolon kanseri hücrelerinde her ligazı devre dışı bırakarak ve zaman içinde hassas bir sekanslama yöntemiyle mutasyon “imzalarını” takip ederek test etti. Bu ligazların, özellikle A3H-I ifade eden hücrelerde, ortadan kaldırılması APOBEC’e özgü mutasyon desenlerini güçlendirdi—tam olarak insan tümörlerinde bulunan türden. Hastaya ait verileri genişleterek binlerce kanser genomunu analiz ettiklerinde, UBR5 veya HUWE1’de mutasyon taşıyan tümörlerin, ligazları sağlam olan tümörlere kıyasla APOBEC bağlantılı mutasyon imzalarının daha yüksek bir payına sahip olduğunu buldular; bu fark toplam mutasyon yükü hesaba katıldıktan sonra da anlamlı kaldı. Bu, hastalardaki bozuk koruyucu ligazların kanserle ilişkili APOBEC3 enzimlerinin kontrolsüz çalışmasına ve tümör genomunu yeniden şekillendirmesine izin verebileceğini düşündürür.
Gelecekteki kanser bakımına etkileri
Uzman olmayan biri için çıkarım şudur: Hücrelerimiz, faydalı antiviral enzimlerin yanlışlıkla kendi DNA’mızı sabote etmesini önlemek için sofistike bir denetim sistemi taşır. UBR4, UBR5 ve HUWE1, APOBEC3 enzimlerinin RNA’ya güvenli şekilde bağlanmadığını algılayan ve özellikle çekirdekte onları hücresel öğütücüye gönderen koruyucular olarak görev yapar. Bu kontrol sistemi ligazlarda meydana gelen mutasyonlarla veya protein parçalanmasını engelleyen ilaçlarla zayıfladığında, APOBEC3 aktivitesi kansere yol açan genetik kaosu ve tedaviye direnç gelişimini körükleyebilir. Bu koruyucu ağın anlaşılması, ligaz mutasyonları veya APOBEC protein düzeyleri gibi yeni tanı belirteçlerine kapı aralar ve bu yolak dikkatli biçimde ayarlanarak tümörlerde zararlı mutasyon patlamalarını antiviral savunmayı zayıflatmadan sınırlamaya yardımcı olunabileceğini düşündürür.
Atıf: Schwartz, I., Budroni, V., Meyenberg, M. et al. Guardian ubiquitin E3 ligases target cancer-associated APOBEC3 deaminases for degradation to promote human genome integrity. Nat Commun 17, 1723 (2026). https://doi.org/10.1038/s41467-026-68420-5
Anahtar kelimeler: APOBEC3, genom kararlılığı, ubiquitin ligaz, kanser mutagenezi, protein parçalanması