Clear Sky Science · tr
Otoorganizasyonla oluşan bir mekanogen aktivite gradyanı ile kasılganlığın uzaysal desenlenmesi Drosophila gastrulasyonunun temelini oluşturur
Dokular kendilerini nasıl şekillendirir
Erken embriyolar basit hücre tabakalarını nasıl olup da karmaşık üç boyutlu formlara dönüştürüyor, gizemini koruyor. Bu çalışma o sihirli işlemin arkasındaki temel soruyu soruyor: bir dokunun doğru yerde ve yönde katlanması için hücreler nerede sıkışıp büküleceklerini nasıl koordine eder? Sinek embriyolarını yüksek çözünürlükte izleyerek, yazarlar hücrelerin kendilerini çekmesi gereken yerleri doğrudan desenleyen “mekanik bir morfojen” gibi davranan kimyasal bir sinyali açığa çıkarıyorlar ve bunun gelişimdeki kritik bir katlanma olayını sürüklediğini gösteriyorlar.
Embriyoyu katlayan bir dalga
Sirke sineği Drosophila’da erken gelişimde önemli bir adım gastrulasyondur; düz bir hücre tabakası içeri doğru bükülerek bağırsak oluşumunu başlatır. Embriyonun arka kısmında, posterior endoderm primordiyumu adı verilen bir hücre yaması, apikal yani üst yüzlerinde kasılarak bu süreci başlatır. Bu ilk bükülme, komşu hücreler boyunca ilerleyen dokusal invaginizasyon (içeri çökme) dalgasını tetikler. Yazarlar bu dalganın, GPCR ailesi olarak bilinen reseptörleri aktive eden ve bunun sonucunda motor protein Myosin-II’den oluşan hücresel kasılma mekanizmasını devreye sokan salgılanan bir molekül olan Fog adlı bir sinyale bağımlı olduğunu gösteriyorlar.
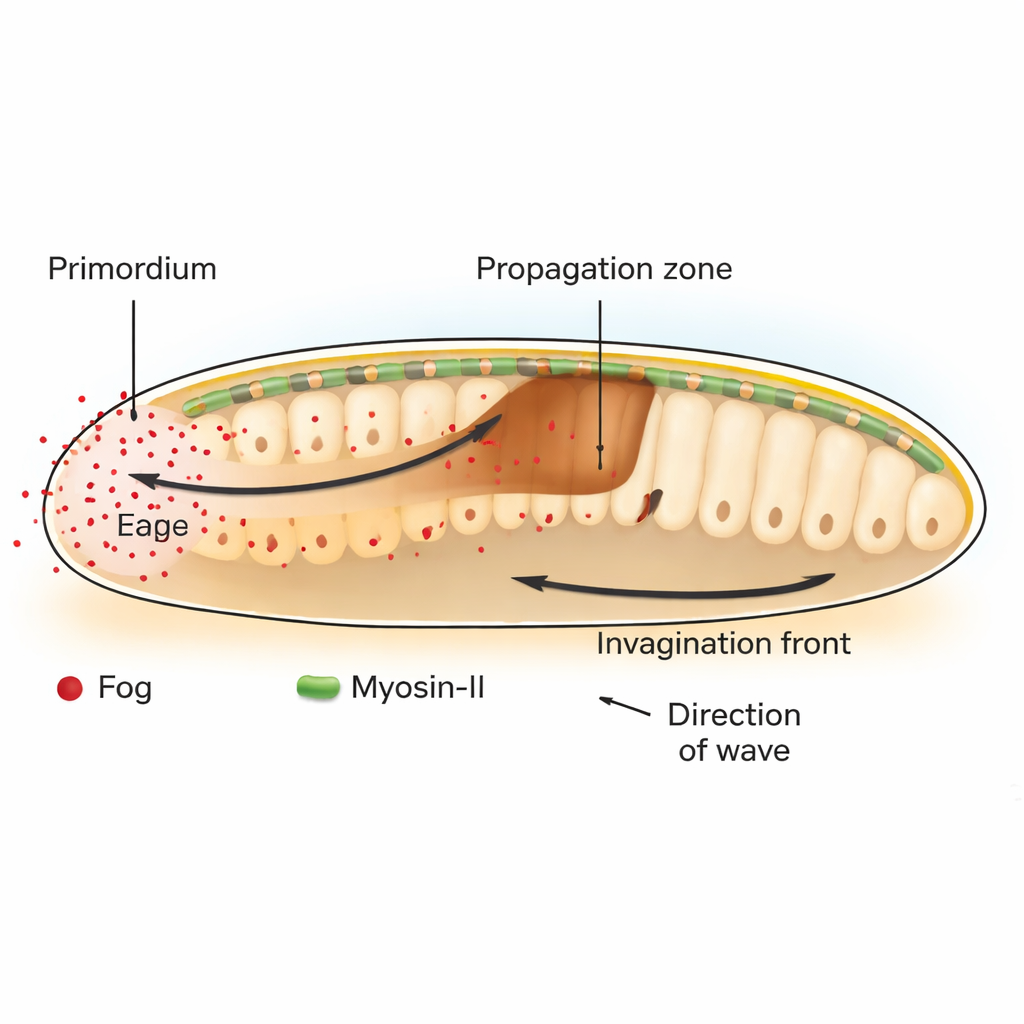
Kaderi değil gücü desenleyen bir kimyasal
Klasik olarak gelişim biyologları, konsantrasyon gradyanlarıyla hücrelere hangi kimliği benimseyeceklerini söyleyen difüze moleküller olan “morfojenler”e odaklanmışlardır. Burada Fog farklı davranır. Bir bölgenin ne tür bir hücreye dönüşeceğini değiştirmek yerine, Fog hücrelerin ne kadar güçlü kasılacağını doğrudan ayarlar. Araştırmacılar Fog ve onun aşağı akış habercisi Gα’yı seçici olarak sadece belirli bölgelerde geri kazandırıp bloke ederek, primordiumda üretilen Fog’un Myosin-II aktivasyonunu ve komşu propogasyon bölgesinde dokunun katlanmasını uzaktan tetiklemek için hem gerekli hem de yeterli olduğunu gösteriyorlar. Fog yayılmayacak şekilde bağlandığında (tether edildiğinde), yalnızca üreten hücreler büzülür ve invaginizasyon dalgası sadece bir veya iki hücre sırasından sonra durur.
Hücre yüzeyinde gizli bir gradyan
Doğal bir fikir Fog’un hücrelerin dışında klasik bir konsantrasyon gradyanı oluşturabileceğiydi. Fluoresanla etiketlenmiş bir Fog versiyonu ve hassas floresan ölçümleri kullanarak ekip tam tersini buluyor: doku ile onu saran kabuk (vitellin membranı) arasındaki ince sıvı katmanında Fog şaşırtıcı derecede uniform. Buna karşın Myosin-II aktivitesi açıkça güçlü bir, ilerleyen katlanmanın hemen önünde en kuvvetli olan ve birkaç hücre çapı uzaklıkta zayıflayan dik bir hareketli gradyan oluşturuyor. Eksik parça şu ki: Fog basit bir hacimsel konsantrasyon işareti gibi davranmıyor; bunun yerine Fog’un küçük bir fraksiyonu kısa süreliğine hücre yüzeyinde hapsolup GPCR reseptörlerine bağlanıyor ve serbest Fog molekülleri sıvıda eşit karışmış olsa bile yüzeye bağlı bir aktivite gradyanı oluşturuyor.
Reseptörler, endositoz ve adezyon dalgayı şekillendirir
Yazarlar gösteriyor ki bu yüzeye bağlı Fog, reseptörleriyle birlikte kendi kendine bir desen oluşturuyor. Fog tekrar tekrar reseptörlerle karşılaştığı yerlerde reseptör kümelenmesini ve aktivasyonunu teşvik ediyor, bu da daha fazla Myosin-II çekiyor. Bir hücresel “temizlik” süreci—GPCR endositozu—ardından aktif kompleksleri ortadan kaldırıyor, kontrolden çıkan aktivasyonu önlüyor ve sinyalin ne kadar yayıldığını ayarlamaya yardımcı oluyor. Bu endositoz genetik olarak yavaşladığında, Myosin-II gradyanı hem daha yüksek hem de daha geniş hale geliyor. İkinci kilit oyuncu integrinler olarak adlandırılan bir adezyon molekülleri kümesi. Doku büküldükçe, katlanmanın önündeki hücreler vitellin membrana bastırıyor; bu temas yerel olarak integrinleri aktive ediyor ve bunlar Fog–GPCR sinyalleşmesinin etkinliğini artırıyor. Güçlü integrin etkinleşmesinin alanı Myosin-II gradyanının kapsamıyla örtüşüyor ve integrinler olmadığında dalga zayıf ve kısa menzilli oluyor, Fog sinyalleşmesi başka yerlerde güçlendirilse bile.
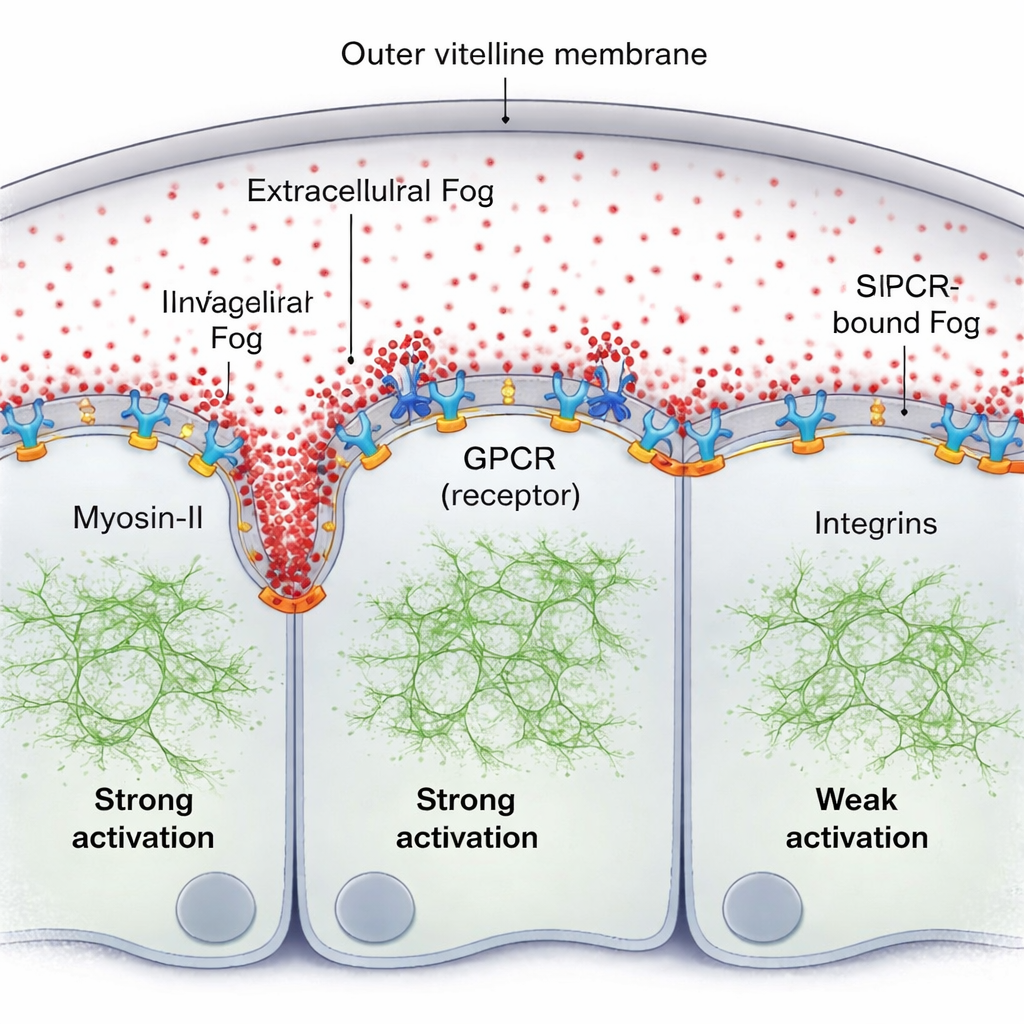
Kendi kendini yenileyen mekanik bir desen
Uzman olmayan biri için ana mesaj şudur: embriyo nereye katlanacağını karar vermede sadece önceden çizilmiş kimyasal haritalara güvenmiyor. Bunun yerine hareketli bir mekanik aktivite deseni anında inşa ediyor. Fog eşit olarak yayılıyor, ama etkili etkisi hücre yüzeyinde reseptör kümelenmesi, reseptörlerin uzaklaştırılması ve hücrelerin çevrelerine bastıkça değişen doku geometrisiyle şekillendiriliyor. Bu, dokuyu içeri doğru koordineli bir dalga halinde çeken kendi kendine organize olan, hareket eden bir kasılganlık gradyanı yaratıyor. Bu çalışma, difüze olan bir molekülün doku içindeki fiziksel kuvvetleri doğrudan desenlediği ve böylece canlı formların gelişim sırasında kendilerini bu denli güvenilir biçimde nasıl şekillendirdiklerini açıklamaya yardımcı olan uzun zamandır kuramsallaştırılmış bir “mekanogen”e somut bir örnek sunuyor.
Atıf: Mundhe, G., Dunsing-Eichenauer, V., Philippe, JM. et al. Spatial patterning of contractility by a self-organized mechanogen activity gradient underlies Drosophila gastrulation. Nat Commun 17, 1721 (2026). https://doi.org/10.1038/s41467-026-68418-z
Anahtar kelimeler: g astrulasyon, mekanogen, Drosophila embriyosu, doku mekaniği, Fog sinyalleşmesi