Clear Sky Science · tr
Plasmodium falciparum AP2‑G’nin DNA bağlanmasını tek bir valinden lösine geçiş bozar ve ap2‑g aktivasyonunda GDV1’in rolünü ortaya çıkarır
Sıtma Parazitleri Hayati Bir Seçimi Nasıl Yapıyor
Kana yerleşen sıtma parazitleri sürekli olarak hayatlarını değiştirebilecek bir kararın eşiğindedir: aynı kişi içinde çoğalmaya devam etmek mi, yoksa sivrisinek ısırığı yoluyla bir sonraki konağa sıçrayabilecek forma mı geçmek. Bu çalışma, parazitin tek bir küçük proteindeki değişikliğin enfektif, sivrisineğe hazır aşamayı tamamen nasıl kapattığını ortaya koyarak sıtma bulaşımını engellemek için yeni yaklaşımlar sunuyor.
Parazitin Yol Ayrımı
Kanda, Plasmodium falciparum parazitleri çoğunlukla hastalığa yol açan hızlı büyümeye odaklanır. Ancak küçük bir kesim, sadece sivrisineklerin alıp aktarabileceği cinsel formlar olan gametositlere dönüşür. Bir topluluk içindeki sadece bazı parazitlerin bu geçişi nasıl yaptığı uzun süredir bir bilmeceydi. Önceki çalışmalar, GDV1 ve AP2‑G adındaki DNA‑bağlayıcı bir proteinin bu kararın merkezinde yer aldığını göstermişti. GDV1, normalde sessiz olan ap2‑g genini uyandırmaya yardım eder; AP2‑G ise cinsel gelişimi yönlendiren bir dizi geni aktive eder. Mevcut çalışma, STK2 adlı bir kinazı incelemeyi amaçlamış, ancak AP2‑G’nin kendisinde çok daha çarpıcı bir keşfe rastlamıştır.
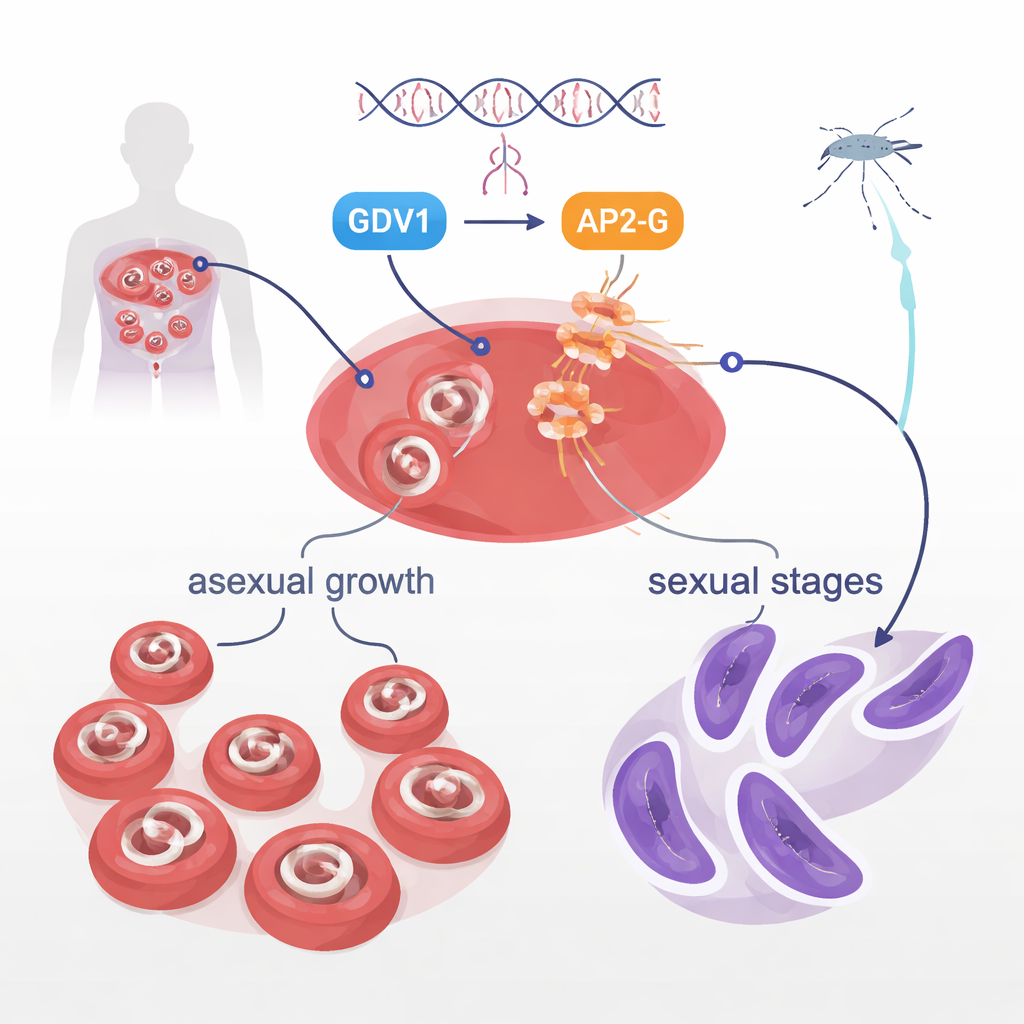
Bulaşımı Durduran Tek Bir Amino Asit
Araştırmacılar bir laboratuvar parazit suşunda stk2 genini sildiklerinde, bu parazitlerin tamamen gametosit üretme yeteneklerini kaybettiklerini, ancak eşeysiz çoğalmanın normal seyrettiğini fark ettiler. İlginç bir şekilde, benzer müdahaleleri başka bir suşta tekrarladıklarında gametositler normal şekilde oluştu. Tüm genom dizilemesi gizli suçluyu ortaya çıkardı: ap2‑g geninde tek bir “harf” değişimi—2163 pozisyonunda valinin yerine çok benzer bir amino asit olan lösinin geçmesi. Bu pozisyon, AP2‑G’nin DNA‑bağlama bölgesinin hemen başlangıcında yer alır; bu bölge, belirli DNA motiflerini fiziksel olarak kavrayarak genleri açan kısımdır. Bu küçük valin‑ten lösin değişimi tek başına gametosit oluşumunu ortadan kaldırmaya yetti. Bilim insanları bu mutasyonu normal parazitlere mühendislik ile eklediklerinde gametositler kayboldu; geri valine çevrildiklerinde ise cinsel gelişim tamamen geri döndü.
Bu Değişiklik Moleküler Kilidi Nasıl Bozuyor
Bu ince değişikliğin neden bu kadar yıkıcı olduğunu anlamak için ekip bilgisayar modellemesini laboratuvar deneyleriyle birleştirdi. Yapı tahminleri, valinin lösine dönüşmesinin AP2 DNA‑bağlama domaininin hassas şeklini kaydırıp kararsızlaştırdığını öne sürdü. Saflaştırılmış proteinlerle yapılan test tüpü deneylerinde normal AP2‑G tercih ettiği kısa DNA dizisine, içinde “GnGTAC” motifini barındıran koda güçlü biçimde bağlandı. Buna karşın 2163 pozisyonunda lösin taşıyan mutant AP2‑G bu diziye hiç bağlanamadı. Kararlı DNA bağlaması olmadan AP2‑G artık kendi genini açan pozitif geri besleme döngüsünü (otoregülasyon) kuramıyor ve parazitleri cinsel yola itmek için gereken onlarca aşağı akış geni aktive edemiyordu. İşlevsel olarak, mutant parazitler “kısır” hale geldi: alyuvarlarda hâlâ çoğalıyorlardı ama sivrisinekleri enfekte eden formları üretemediler.
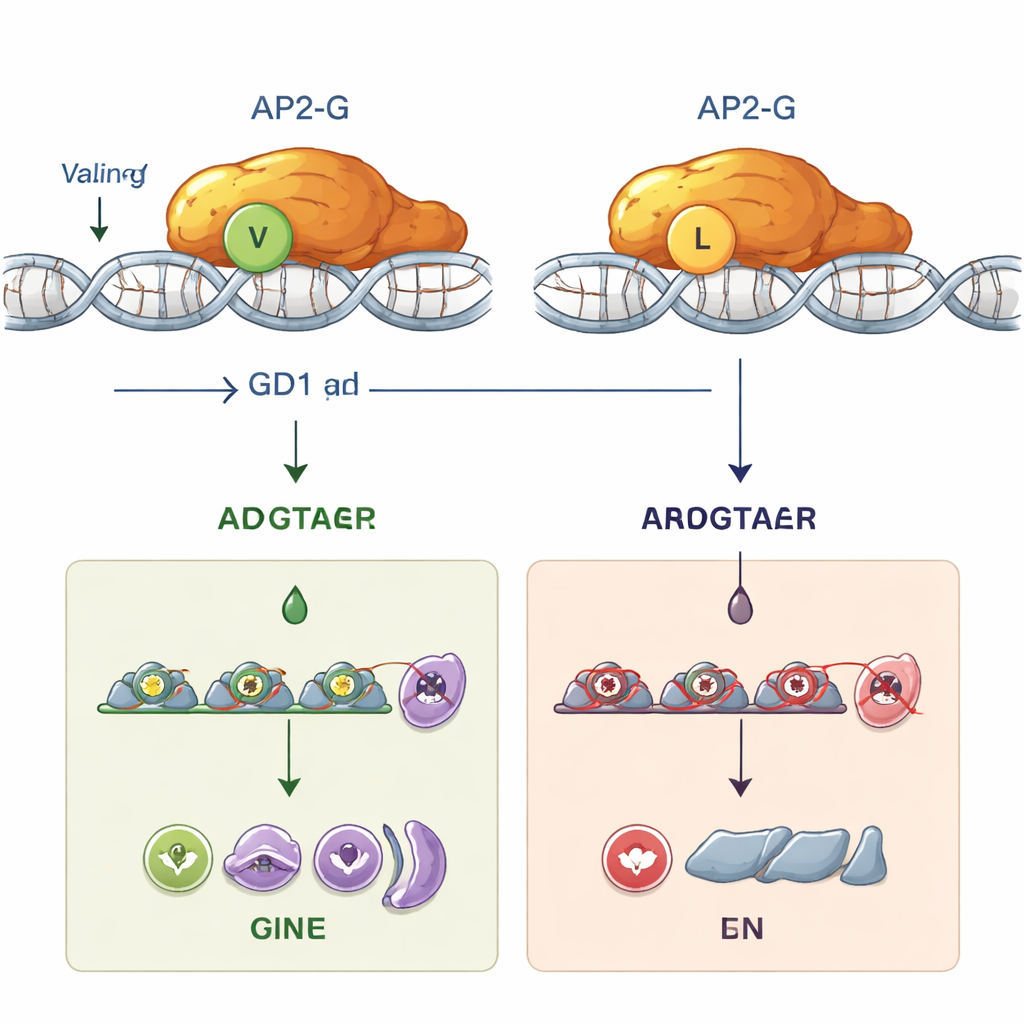
AP2‑G Devralmadan Önceki GDV1’in Gizli Rolü
Mutasyon araştırmacılara benzersiz bir araç da sağladı: ap2‑g geninin açılabildiği ama AP2‑G’nin DNA’ya bağlanamadığı parazit hatları. Işıma ve floresan raporlayıcıları kullanarak, kırmızı kan hücrelerindeki 48 saatlik döngü sırasında farklı aktörlerin ne zaman göreve girdiğini izlediler. GDV1 proteininin, şizogoni adı verilen erken bir evrede ilk ortaya çıktığını ve sessiz ap2‑g geninin aktif hale gelmesi için gerekli olduğunu buldular. Bu erken aktivasyon ap2‑g normal AP2‑G kodlasa da mutant versiyonunu kodlasa da gerçekleşiyordu. Sadece daha sonra, yeterli miktarda normal AP2‑G biriktiğinde güçlü oto‑güçlendirme döngüsü ve diğer “cinsel” genlerin aktivasyonu ortaya çıktı. MSRP1 adlı belirgin bir işaretçi yalnızca fonksiyonel AP2‑G taşıyan parazitlerde ışık verdi; bu da cinsel adanmışlığın erken ve geç evrelerini ayırt etmek için kullanışlı bir yol sağladı. Lösin geçişi taşıyan mutant çizgilerde, GDV1 yine ap2‑g’yi uyandırabiliyordu, fakat bozulmuş AP2‑G süreçleri ilerletemediğinden cinsel gelişim tıkandı.
Sıtma Yayılımını Durdurmaya Yönelik Çıkarımlar
Genel okuyucu için sonuç basit: sıtma parazitleri bulaşıp bulaşmayacaklarına karar vermek için son derece hassas bir moleküler kilide dayanır. Bu çalışma, kilitteki tek bir “dişiğin”—AP2‑G’nin DNA’yı kavrayan bölgesindeki tek bir valinin—değişmesinin parazitin asla sivrisinekleri enfekte eden aşamaları üretememesine yol açtığını gösteriyor. Aynı zamanda GDV1’in, AP2‑G kendi üretimini güçlendirip daha geniş bir cinsel programı başlatmadan önce sessiz ap2‑g geninin kilidini ilk açan anahtar olarak davrandığını netleştiriyor. Bu olaylar dizisini haritalandırarak ve her adımın gerçekleştiğini gösteren raporlayıcı parazit hatları yaratarak çalışma, cinsel adanmışlığı bozan ilaçları veya insan faktörlerini taramak için güçlü araçlar sağlıyor. Uzun vadede AP2‑G’nin DNA‑bağlama bölgesini veya GDV1 kaynaklı aktivasyon adımını hedeflemek, sadece bir hastadaki sıtmayı tedavi etmekle kalmayıp bulaş zincirini tamamen kesmeye yönelik yeni stratejilerin temelini oluşturabilir.
Atıf: Prajapati, S.K., Dong, J.X., Morahan, B.J. et al. A single valine to leucine switch disrupts Plasmodium falciparum AP2-G DNA binding and reveals GDV1’s role in ap2-g activation. Nat Commun 17, 1719 (2026). https://doi.org/10.1038/s41467-026-68416-1
Anahtar kelimeler: sıtma bulaşması, Plasmodium falciparum, gametosit gelişimi, AP2‑G, GDV1