Clear Sky Science · tr
Hiyerarşik mekanizmalar DNA lezyonu nedeniyle duraklayan RNA polimeraz II’nin temizlenmesini kontrol eder
Gen Kopyalama Makineleri Bir Engel ile Karşılaştığında
Her saniye, RNA polimeraz II adı verilen milyonlarca küçük moleküler makine DNA boyunca hareket eder ve genleri RNA’ya kopyalar. Ancak DNA hasar gördüğünde — örneğin güneşten gelen ultraviyole (UV) ışığıyla — bu makineler takılır. Eğer takılan polimerazlar birikirse, hücreler genlerini doğru okuyamaz; bu özellikle beyin hücreleri için tehlikelidir ve Cockayne sendromu gibi nadir hastalıklara yol açabilir. Bu çalışma, hücrelerin bu bloklanan makineleri nasıl algıladığını ve kalıcı zarar oluşmadan önce nasıl yeniden başlattıklarını veya çıkardıklarını ayrıntılarıyla ortaya koyuyor.
Hücresel Trafik Sıkışmalarını İzlemenin Yeni Bir Yolu
Araştırmacılar, takılan polimerazları nasıl temizlediklerini anlamak için zaman çözünürlüklü bir “trafik kamerası” kurdular. Mevcut RNA polimeraz II moleküllerinin hareket etmeye devam etmesine izin veren, ancak yenilerinin başlamasını engelleyen bir ilaç kullandılar ve ardından her hücre çekirdeğinin içinde küçük bir UV hasar bölgesi oluşturdular. Polimerazın aktif formundaki belirli bir kimyasal etiketi izleyerek, hasarlı bölgede genoma göre ne kadar hızlı kaybolduğunu görebildiler. Paralel olarak, hücre özütlerindeki toplam aktif polimeraz miktarını ölçen bir test geliştirdiler; bu test yalnızca polimerazların DNA’dan ne zaman ayrıldığını değil, hücrenin bertaraf sistemi tarafından ne zaman yıkıldıklarını da ortaya koydu.
Takılan Makineleri Kaldırmak İçin Etiketleme
Araştırma ekibi, aktif olarak okunan genlerdeki lezyonları onaran özel bir onarım sistemi olan transkripsiyona eşlik eden onarıma odaklandı. Her biri farklı bir onarım faktöründen yoksun eşleştirilmiş insan hücre dizileri kullandılar. CSB ve CSA adlı iki protein belirleyici bekçi rolünde ortaya çıktı. Bu proteinlerden biri yok olduğunda, polimeraz II hasar bölgelerinde birikti ve inatla kaldı; hücre onu parçalayıp ortadan kaldıramadı. Biyokimyasal olarak bu hücreler aynı zamanda polimerazdaki kritik bir noktaya küçük ubikuitin etiketleri ekleyemiyordu. Buna karşılık, hasarlı DNA’yı kesip değiştiren daha sonraki onarım proteinlerinden yoksun hücreler polimerazı normal şekilde temizledi. Bu, takılan polimerazın ilk ubikuitin etiketlenmesinin onun kaderini belirleyen kritik tetik olduğunu gösterdi.
İki Temizlik Ekibi: Biri Hızlı, Biri Yedek
Polimeraz etiketlendiğinde, hücre onu temizlemek için iki yoldan birini seçebilir. Birincil, hızlı yol TFIIH adlı büyük bir onarım kompleksine ve özellikle DNA’yı açmak için enerji kullanan XPD helikaz alt birimine dayanır. ELOF1, UVSSA ve STK19 gibi yardımcı proteinler TFIIH’yi takılan polimeraza getirir ve XPD’yi polimerazın hemen önündeki DNA’ya konumlandırır. Helikaz-ölü XPD mutasyonuna sahip hasta hücrelerinde yapılan yeni testlerle, XPD DNA’yı açamazsa polimeraz temizlenmesinin dramatik şekilde yavaşladığı gösterildi; oysa onarımın geri kalanı mevcuttu. Bu, XPD’nin mekanik çekme hareketinin normalde polimerazı lezyondan “sallanıp” serbest bırakan ve onarım enzimlerinin hasarlı bölgeye erişmesini sağlayan etki olduğunu gösterir.
Yavaş ama Hayati Bir Plan B
Çalışma ayrıca takılan polimerazı temizlemek için daha yavaş, acil bir yolu ortaya koydu. Bu yol, ubikuitin etiketlerini tanıyan ve proteinleri kromatinden zorla çıkarabilen VCP (p97 olarak da bilinir) adlı bir proteine dayanır. Tam işleyen TFIIH’ye sahip sağlıklı hücrelerde VCP’yi engellemek yalnızca küçük bir etki yaptı. Ancak TFIIH eksik, yanlış konumlanmış veya helikaz-ölü olduğunda, polimeraz temizlenmesi neredeyse tamamen VCP’ye bağımlı hale geldi. Bu durumlarda VCP, normal onarım ilerleyemese bile etiketli polimerazı DNA’dan çekip uzaklaştırabiliyordu. Önemli olarak, bu yedek yolun da bazı ubikuitin etiketlemelerini gerektirdiği görüldü; bu da CSB veya CSA eksikliği nedeniyle ubikuitin işaretlerinden yoksun olan hücrelerin hem ana hem de yedek yollarda başarısız olmasını açıklıyor.
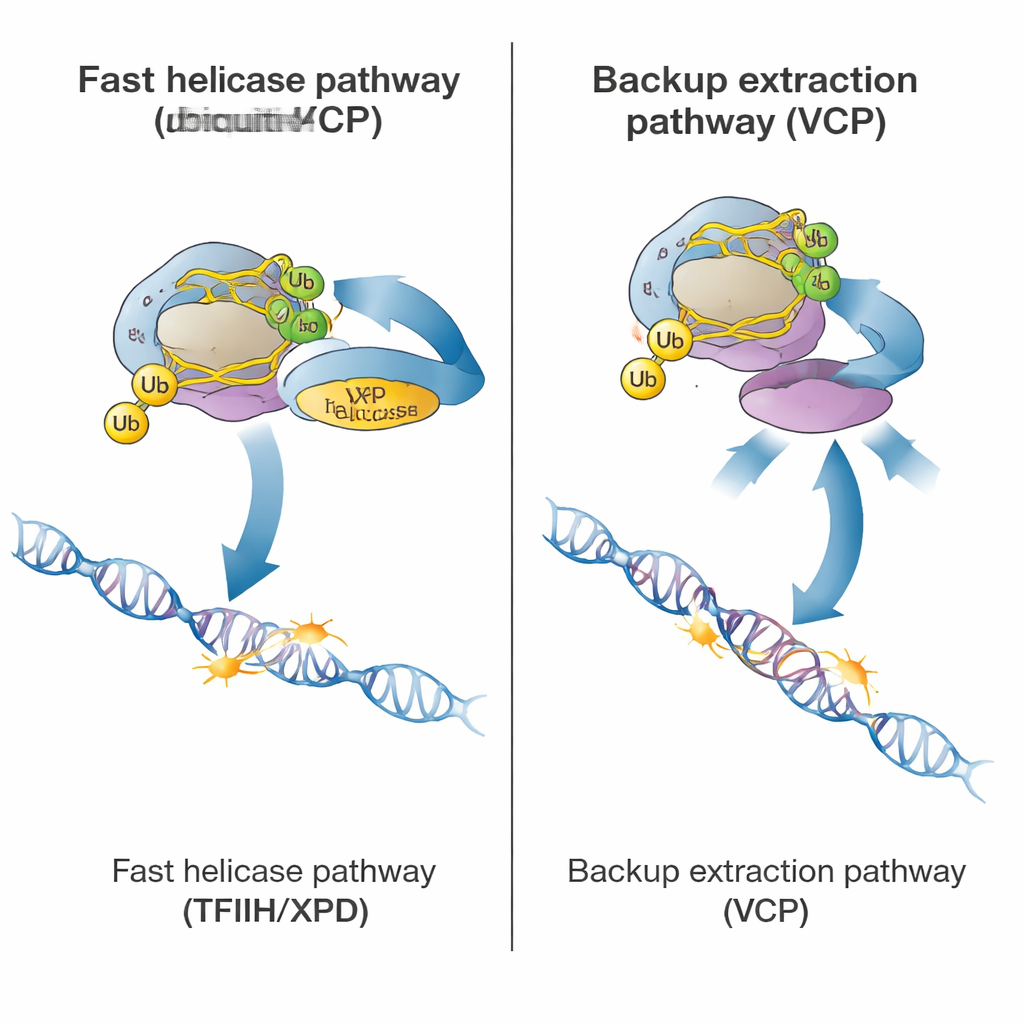
Sağlık ve Hastalık Açısından Önemi
Bir araya getirildiğinde, çalışma RNA polimeraz II DNA hasarıyla karşılaştığında hücrelerin kullandığı hiyerarşik bir güvenlik programını özetliyor. Önce CSB ve CSA takılan makineyi ubikuitinle işaretler. Her şey düzgün çalışıyorsa, TFIIH ve XPD helikazı polimerazı hızla yerinden çıkarır ve lezyon kesilip onarılabilir. TFIIH işini yapamazsa, VCP devreye girer, polimerazı çıkarır ve yıkım için gönderir; böylece DNA hasarı kendisi kalmaya devam etse bile gen ifadesinin tıkanmasının önüne geçilmiş olur. Bu çerçeve, CSB veya CSA’daki kalıtsal kusurların özellikle şiddetli nörolojik problemlere neden olmasını açıklamaya yardımcı olur: ubikuitin etiketlemesi olmadan hücreler hem birincil onarım kaynaklı yolu hem de yedek çıkarma yolunu kaybeder ve takılan polimerazlar hasarlı genler üzerinde sıkışıp kalır, transkripsiyon kronik olarak engellenir.
Atıf: van der Meer, P.J., Yakoub, G., Tsukada, K. et al. Hierarchical mechanisms control the clearance of DNA lesion–stalled RNA polymerase II. Nat Commun 17, 1647 (2026). https://doi.org/10.1038/s41467-026-68413-4
Anahtar kelimeler: transkripsiyona eşlik eden DNA onarımı, RNA polimeraz II, UV kaynaklı DNA hasarı, protein ubikuitinlenmesi, Cockayne sendromu