Clear Sky Science · tr
Sürekli mekansal‑zamansal idiyopatik pulmoner fibrozis tedavisi için doku metalloproteinaz inhibitörü‑1 hedefleyen bir nanosistem
Neden inatçı akciğer skarlaşması önemli?
Idiyopatik pulmoner fibrozis (IPF), normal, süngerimsi akciğer dokusunun yavaşça sert skar dokusuyla yer değiştirdiği amansız bir akciğer hastalığıdır. IPF hastaları günlük aktiviteleri yaparken nefes darlığı çeker ve tanıdan sonra çoğunlukla sadece birkaç yıl yaşarlar. Günümüzdeki ilaçlar bazı hastalarda hastalığın ilerlemesini yavaşlatabiliyor, ancak mevcut skarları nadiren geri döndürürler ve sıklıkla yan etkilere yol açarlar. Bu çalışma, sadece IPF’yi yavaşlatmakla kalmayıp aynı zamanda skar dokusunu aktif olarak temizlemeyi ve akciğerlerin kendini onarmasına yardımcı olmayı hedefleyen akıllı, inhalasyon yoluyla verilen bir “nano‑terapi”yi araştırıyor.
Sorun: yapışkan skarlar ve kimyasal stres
IPF’de oksijenin normalde kana geçtiği boşluklar kolajen gibi fazla proteinlerle dolar ve esnek hava kesecikleri sert lekeler haline gelir. Araştırmacılar, normalde fazla kolajeni parçalayan enzimleri frenleyen TIMP‑1 adlı bir proteine odaklandılar. Hasta ve skar oluşturulmuş fare akciğerlerinden alınan örnekleri inceleyerek, TIMP‑1 seviyelerinin sağlıklı akciğerlere göre birkaç kat daha yüksek olduğunu ve kolajen birikimiyle paralel olarak arttığını buldular. Aynı zamanda hasarlı akciğerlerde reaktif oksijen türlerinin (ROS) — hücrelere zarar veren kimyasal “kıvılcımlar” — yükseldiği ve sağlıklı hava‑keseciği örtücü hücrelerin belirteçlerinin kaybolduğu görüldü. Bu bulgular birlikte, fazla TIMP‑1’in skarın parçalanmasını yavaşlattığı ve oksidatif stresin akciğer yapısını daha da zedeleyerek kısır bir döngü oluşturduğu yönünde işaret etti.
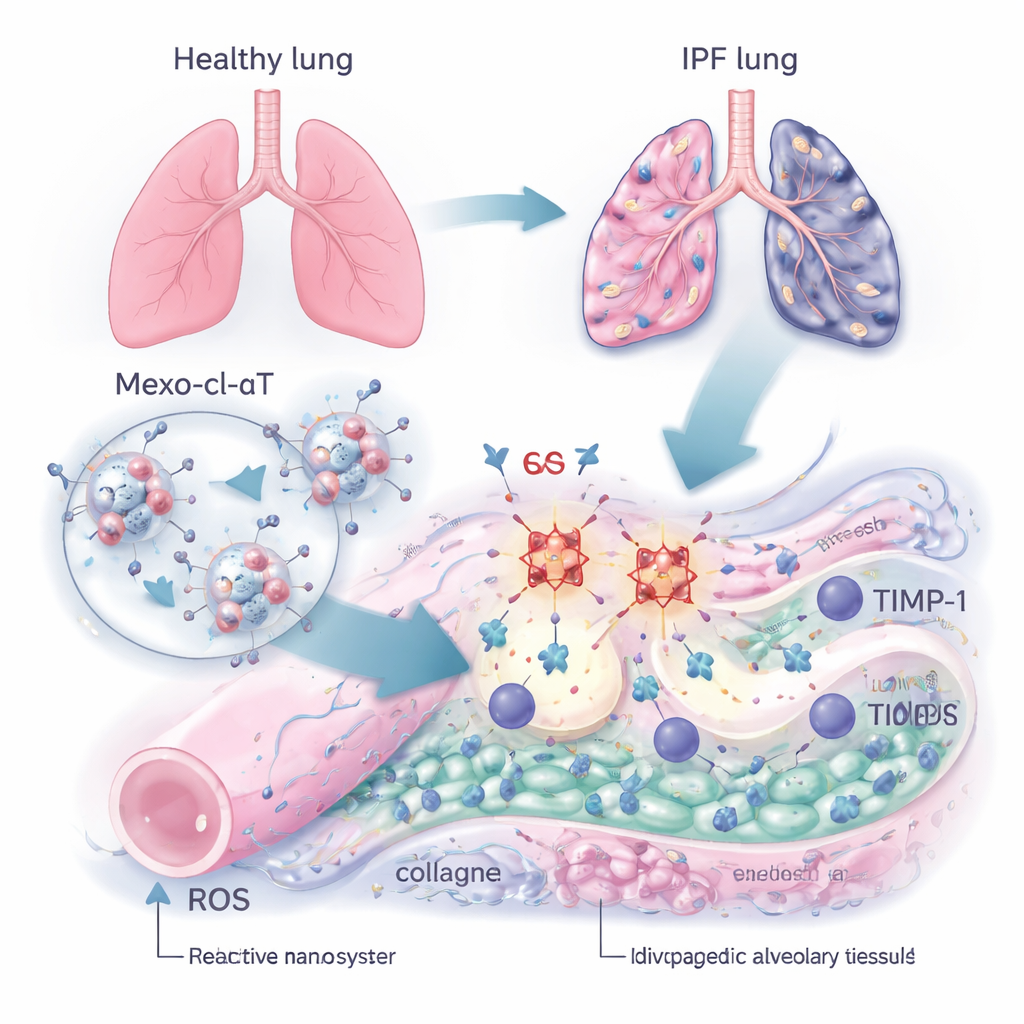
Akıllı taşıyıcı: mikroskobik onarım paketleri
Bu döngüyü kırmak için ekip Mexo‑cl‑aT adlı nanoskalalı bir terapi geliştirdi. Başlangıç olarak, yaralanmış dokulara yönelme ve onarımı destekleme yeteneği zaten bilinen kök hücre kaynaklı doğal, kabarcık benzeri partiküller olan ekzosomlar kullanıldı. Bu ekzosomların yüzeyine özellikle TIMP‑1’e bağlanan antikorlar eklendi. Ekzosom ile antikor arasındaki bağlantı, ROS tarafından kesilebilen özel bir kimyasal bağlayıcı ile oluşturuldu. Yani skarlı akciğerin sert kimyasal ortamı bir sinyal olarak kullanılıyor: ekzosom hasarlı, ROS açısından zengin bir bölgeye ulaştığında bağlayıcı kırılıyor, bir miktar ROS’yi nötralize ederek antikoru TIMP‑1’in yoğun olduğu yerde açığa çıkarıyor ve ekzosomun kendisi de doku onarımını desteklemeye devam ediyor.
Nanosistemin davranışı ve çalışma şekli
Hücre çalışmaları, Mexo‑cl‑aT’nin sıvıda kararlı kaldığını ancak hastalıklı akciğerlerdekiye benzer hidrojen peroksit seviyelerine maruz kaldığında antikorlarını hızla bıraktığını gösterdi. Aynı zamanda peroksit miktarını keskin şekilde azalttı ve ROS temizleme rolünü doğruladı. Skar‑benzeri hücre modellerinde açığa çıkan antikorlar TIMP‑1 seviyelerini düşürdü ve kolajeni parçalayan enzimlerin serbest kalmasını sağladı; ekzosom bileşeni ise hücre ölümünü azalttı, hücre büyümesini artırdı ve hem akciğer hem de kan‑damar hücrelerinde yara kapanmasını hızlandırdı. Bağlayıcının kesilemediği versiyonlarla karşılaştırıldığında, ROS‑yanıtlı tasarım daha fazla kolajeni ortadan kaldırdı ve kimyasal stresi daha etkili biçimde azalttı; bu da kontrollü salımın önemini vurguluyor.
Ağır bir akciğer skarlaşması modelinde test
Ekip daha sonra terapinin, ileri düzey akciğer fibrozisini taklit etmek için seçilen bleomisin ile tetiklenen fare modelinde testini yaptı. Tek bir inhalasyon dozunu takiben Mexo‑cl‑aT akciğerlerde günlerce kaldı ve bileşenlerinin basit bir karışımına göre daha fazla antikor tuttu. Tedavi edilen akciğerler çıplak gözle ve mikroskop altında daha sağlıklı görünüyordu: hava boşlukları yeniden açıldı, skar kalınlığı düştü ve toplam kolajen içeriği neredeyse normale döndü. Aktif skar oluşturan hücrelerin belirteçleri azaldı, sağlıklı hava‑keseciği ve kan‑damar örtü hücreleriyle ilişkili proteinler yükseldi. Kimyasal ölçümler tedavinin TIMP‑1 seviyelerini keskin şekilde düşürdüğünü, kolajen temizleyen enzimlerin dengesini yeniden sağladığını ve fazla ROS’un yaklaşık dörtte üçünü ortadan kaldırdığını gösterdi. Önemli olarak, inflamasyon ölçümleri azaldı ve kan testleri ile organ incelemeleri belirgin bir toksisite göstermedi.
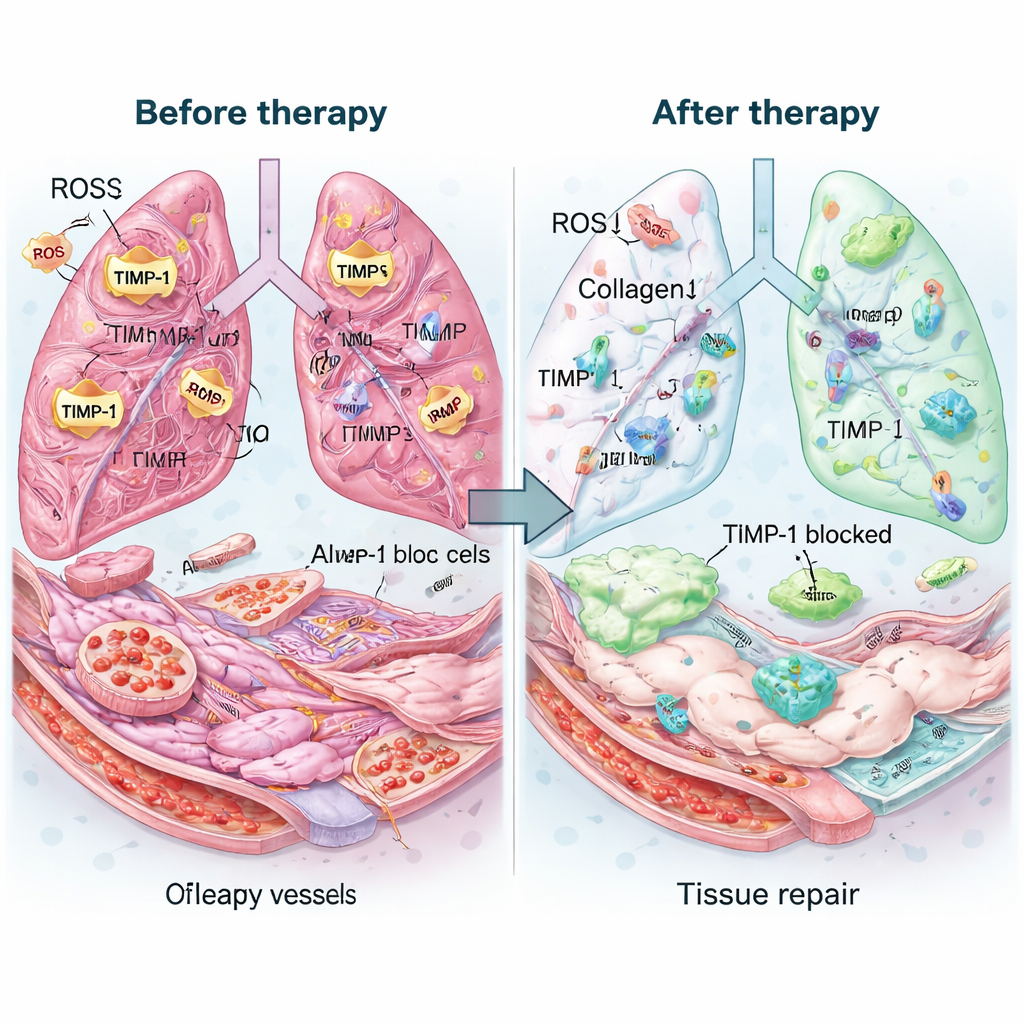
Bu hastalar için ne anlama gelebilir?
IPF ile yaşayan insanlar için bu çalışma henüz hemen uygulanabilecek bir kür sunmuyor, ancak umut verici bir strateji ortaya koyuyor. Yeni hasarı sadece yavaşlatmak yerine, Mexo‑cl‑aT nanosistemi mevcut skarları aktif olarak geri almaya, zararlı kimyasal stresi yatıştırmaya ve kırılgan akciğer dokusunun yeniden inşasını desteklemeye—tüm bunları tedavinin en çok gerektiği yerde yoğunlaşan hedefli, inhalasyon yoluyla bir formda—çalışmayı amaçlıyor. Büyük ölçekli ekzosom üretimi ve insanlarda test edilmesi gibi zorluklar sürse de, çalışma hastalıklı ortama uyarlanmış hassas nano‑tedavilerin bir gün inatçı akciğer skarlaşması ve belki diğer fibrotik hastalıkların tedavisini dönüştürebileceğini öne sürüyor.
Atıf: Li, C., Lu, G., Chen, H. et al. A nanosystem targeting tissue inhibitor of metalloproteinase-1 for continuous spatiotemporal idiopathic pulmonary fibrosis therapy. Nat Commun 17, 1694 (2026). https://doi.org/10.1038/s41467-026-68398-0
Anahtar kelimeler: idiyopatik pulmoner fibrozis, akciğer skarlaşması, nanomedisin, ekzosom terapisi, TIMP‑1